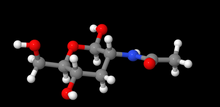
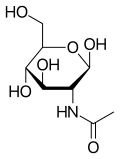
N- ацетилглюкозамин - N-Acetylglucosamine

|
|
 |
|
| Имена | |
|---|---|
|
Название ИЮПАК
β- D - (Ацетиламино) -2-дезоксиглюкопираноза
|
|
| Другие названия
N- ацетил- D- глюкозамин
GlcNAc NAG |
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| 1247660 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard |
100.028.517 |
| Номер ЕС | |
| 721281 | |
| КЕГГ | |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| C 8 H 15 N O 6 | |
| Молярная масса | 221,21 |
| Температура плавления | 211 |
| Родственные соединения | |
|
Родственные моносахариды
|
N-ацетилгалактозамин |
|
Родственные соединения
|
Глюкозамин Глюкоза |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
N- ацетилглюкозамин (GlcNAc) представляет собой амидное производное моносахарида глюкозы . Это вторичный амид между глюкозамином и уксусной кислотой . Это важно в нескольких биологических системах.
Он является частью биополимера в стенке бактериальной клетки , который состоит из чередующихся единиц GlcNAc и N- ацетилмурамовой кислоты (MurNAc), сшитых с олигопептидами по остатку молочной кислоты MurNAc. Эта слоистая структура называется пептидогликаном (ранее называвшимся муреином).
GlcNAc представляет собой мономерное звено из полимера хитина , который образует экзоскелет из членистоногих , таких как насекомые и ракообразные . Это является главным компонентом radulas из моллюсков , в клювах из головоногих , и основного компонента клеточных стенок большинства грибов .
Полимеризованный с глюкуроновой кислотой , он образует гиалуронан .
Сообщалось, что GlcNAc является ингибитором высвобождения эластазы из полиморфно-ядерных лейкоцитов человека (диапазон ингибирования 8-17%), однако это намного слабее, чем ингибирование, наблюдаемое с N- ацетилгалактозамином (диапазон 92-100%).
Медицинское использование
Он был предложен для лечения аутоиммунных заболеваний, и недавние испытания показали некоторый успех.
O-GlcNAцилирование
O-GlcNAcylation - это процесс добавления одного сахара N- ацетилглюкозамина к серину или треонину белка. По сравнению с фосфорилированием , добавление или удаление N- ацетилглюкозамина является средством активации или деактивации ферментов или факторов транскрипции . Фактически, O-GlcNAцилирование и фосфорилирование часто конкурируют за одни и те же сайты серина / треонина. O-GlcNAcylation чаще всего происходит на белках хроматина и часто рассматривается как ответ на стресс.
Гипергликемия увеличивает O-GlcNAcylation, что приводит к инсулинорезистентности . Повышенное O-GlcNA-цилирование из-за гипергликемии, очевидно, является дисфункциональной формой O-GlcNA-цилирования. Снижение O-GlcNAцилирования в головном мозге с возрастом связано со снижением когнитивных функций. Когда O-GlcNAcylation увеличивалось в гиппокампе старых мышей, улучшалось пространственное обучение и память.
Смотрите также
- Кератансульфат
- N- ацетилгалактозамин (GalNAc)
- N- ацетиллактозаминсинтаза
- Агглютинин зародышей пшеницы , растительный лектин, который связывается с этим субстратом.
Рекомендации
- ^ Камель, М .; Ханафи, М .; Бассиуни, М. (1991). «Ингибирование высвобождения фермента эластазы из полиморфноядерных лейкоцитов человека с помощью N- ацетил-галактозамина и N- ацетил-глюкозамина». Клиническая и экспериментальная ревматология . 9 (1): 17–21. PMID 2054963 .
- Перейти ↑ Grigorian A, Araujo L, Naidu NN, Place DJ, Choudhury B, Demetriou M (2011). «N-ацетилглюкозамин ингибирует клеточные реакции Т-хелперов 1 (Th1) / Т-хелперов 17 (Th17) и лечит экспериментальный аутоиммунный энцефаломиелит» . Журнал биологической химии . 286 (46): 40133–40141. DOI : 10.1074 / jbc.M111.277814 . PMC 3220534 . PMID 21965673 .
- ^ a b c d Харт GW, Slawson C, Ramirez-Correa G, Lagerlof O (2011). «Перекрестный разговор между O-GlcNAcylation и фосфорилированием: роли в передаче сигналов, транскрипции и хронических заболеваниях» . Ежегодный обзор биохимии . 80 : 825–858. DOI : 10.1146 / annurev-biochem-060608-102511 . PMC 3294376 . PMID 21391816 .
- Перейти ↑ Ma J, Hart GW (2013). «Белок O-GlcNAcylation при диабете и диабетических осложнениях» . Экспертный обзор протеомики . 10 (4): 365–380. DOI : 10.1586 / 14789450.2013.820536 . PMC 3985334 . PMID 23992419 .
- ^ Уитли EG, Альбарран E, Белый CW 3-й, Биери G, Санчес-Диас C, Пратт K, Snethlage CE, Ding JB, Villeda SA (2019). «Нейрональное O-GlcNAcylation улучшает когнитивные функции в мозге пожилых мышей» . Текущая биология . 29 (20): 3359–3369. DOI : 10.1016 / j.cub.2019.08.003 . PMC 7199460 . PMID 31588002 .