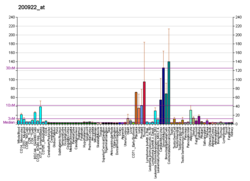
KDELR1 - KDELR1
KDEL (Lys-Asp-Glu-Leu) эндоплазматический ретикулум белок рецептора удерживания 1 , также известный как KDELR1 , является белком , который в организме человека кодируется KDELR1 гена .
Функция
Сохранение резидентных растворимых белков в просвет в эндоплазматический ретикулум (ER) достигается в обоих дрожжей и животных клеток путем их непрерывного извлечения из цис- Гольджи или отсека предварительно Гольджи. Сортировка этих белков зависит от С-концевого сигнала тетрапептида, как правило , лиз - осины - Glu - Leu ( KDEL клеток) в животных и его -Asp-Glu-Leu ( HDEL ) в S.cerevisiae , . Этот процесс опосредуется рецептором, который распознает и связывает тетрапептид-содержащий белок, а затем возвращает его в ER. У дрожжей сортирующий рецептор кодируется одним геном ERD2, который представляет собой семимембранный белок. В отличие от дрожжей, было описано несколько человеческих гомологов гена ERD2, составляющих семейство генов рецептора KDEL. Белок, кодируемый этим геном, был первым идентифицированным членом семейства, и он кодирует белок, структурно и функционально сходный с продуктом дрожжевого гена ERD2. Рецептор KDEL опосредует извлечение неправильно свернутых белков между ER и аппаратом Гольджи. Рецептор KDEL функционирует путем связывания с шаперонами эндоплазматического ретикулума. Эти шапероны распознаются рецептором KDEL в нижних отделах ER. После связывания они упаковываются в везикулы комплекса белков оболочки I для ретроградного транспорта в ER. Исследования in vitro на дрожжах показали, что этот рецептор регулирует мембранный транспорт на ранних стадиях секреторного пути от ER к Golgi. Ошибка или мутация в рецепторе KDEL нарушает контроль качества ER, и наблюдаются заболевания, связанные со стрессом ER.
Дилатационная кардиомиопатия
Рецепторы KDEL участвуют в развитии дилатационной кардиомиопатии (DCM). Для определения взаимосвязи между рецептором KDEL и дилатационной кардиомиопатией были получены трансгенные мыши с точечной мутацией (D193N). Мыши, экспрессирующие транспортный мутантный ген D193N, росли нормально, пока не достигли совершеннолетия. Мутантный рецептор KDEL не функционировал после 14-недельного возраста, и у этих мышей развился DCM. У них наблюдались расширенные камеры сердца, а также более высокое соотношение сердца к телу с увеличенным сердцем, а сердечные миоциты были больше по размеру. Не наблюдалось разницы в артериальном кровяном давлении между мышами дикого типа и мутантными мышами, таким образом, кардиомегалия не была связана с гипертензией. После анализа было обнаружено, что мутантные мыши KDEL имели пролиферацию в их саркоплазматическом ретикулуме (SR) и сужение поперечных канальцев по сравнению с мышами дикого типа и контрольной группой. Более того, в расширенном SR наблюдались агрегации дегенеративных мембранных белков. Это предполагает, что мутантный рецептор KDEL приводит к нарушению рециклинга и контроля качества ER, что приводит к агрегации неправильно свернутых белков в ER. Более того, трансгенные мыши KDEL D193N имели дефекты в токе Са ++ канала L-типа в миоцитах желудочков. Базальный ток этих каналов был значительно ниже, чем в контроле. Экспрессия каналов L-типа была ниже в плазматической мембране клеток сердца KDEL D193N из-за сужения поперечных канальцев. BiP, белок-шаперон, был неравномерно распределен и синтезировался в большей пропорции у трансгенных мутантных мышей, что предполагает увеличение концентрации неправильно свернутых белков. Они также наблюдали агрегаты системы убиквитин-протеасома (система деградации); это говорит о том, что произошло насыщение системы из-за высоких уровней неправильно свернутых белков, которые приводят к нарушению контроля качества ER. Исследователи пришли к выводу, что гиперубиквитинирование и насыщение протеасомной системы происходит из-за накопления неправильно свернутого белка, который вызывает стресс. Накопление неправильно свернутых белков, вызванное стрессом ER, также наблюдалось в DCM человека. Исследование DCM на мышах показало увеличение апоптоза из-за высоких уровней экспрессии CHOP. CHOP - это фактор транскрипции, который повышается во время стресса ER и вызывает апоптоз клеток во время процесса развернутого белкового ответа. Повышение давления / механического стресса у мышей KDEL D193N вызывало еще больший синтез BiP, CHOP и других белков, которые являются биомаркерами клеточного стресса и стресса ER, поскольку способность ER справляться с этим очень ограничена.
Лимфопения
KDELR1 также важен для развития лимфоцитов . Мыши с миссенс-мутацией Y158C в Kdelr1 имеют уменьшенное количество В- и Т-лимфоцитов и более восприимчивы к вирусной инфекции.
Взаимодействия
KDELR1 взаимодействует с ARFGAP1 .
Состав
Структура Gallus gallus KDELR2 (Uniprot Q5ZKX9 ) была решена в состоянии Apo, связанном с пептидом KDEL состоянии и связана с синтетическим нанотелом. Идентичность последовательностей KDELR1 человека и KDELR2 курицы составляет 84,4%.
Смотрите также
использованная литература
дальнейшее чтение
- Pelham HR (октябрь 1996 г.). «Динамическая организация секреторного пути» . Структура и функции клеток . 21 (5): 413–9. DOI : 10,1247 / csf.21.413 . PMID 9118249 .
- Льюис М.Дж., Пелхэм Х.Р. (январь 1992 г.). «Лиганд-индуцированное перераспределение человеческого рецептора KDEL из комплекса Гольджи в эндоплазматический ретикулум». Cell . 68 (2): 353–64. DOI : 10.1016 / 0092-8674 (92) 90476-S . PMID 1310258 . S2CID 43356178 .
- Льюис М.Дж., Пелхэм Х.Р. (ноябрь 1990 г.). «Человеческий гомолог дрожжевого рецептора HDEL». Природа . 348 (6297): 162–3. Bibcode : 1990Natur.348..162L . DOI : 10.1038 / 348162a0 . PMID 2172835 . S2CID 4356283 .
- Aoe T, Cukierman E, Lee A, Cassel D, Peters PJ, Hsu VW (декабрь 1997 г.). «Рецептор KDEL, ERD2, регулирует внутриклеточный трафик, рекрутируя белок, активирующий GTPase, для ARF1» . Журнал EMBO . 16 (24): 7305–16. DOI : 10.1093 / emboj / 16.24.7305 . PMC 1170331 . PMID 9405360 .
- Смит Дж. С., Тачибана И., Поль У, Ли Х. К., Танараджасингам У., Портье Б. П., Уэки К., Рамасвами С., Биллингс С. Дж., Моренвайзер Х. У., Луис Д. Н., Дженкинс Р. Б. (февраль 2000 г.). «Карта транскриптов области супрессора опухоли глиомы 19q-плеча хромосомы». Геномика . 64 (1): 44–50. DOI : 10.1006 / geno.1999.6101 . PMID 10708517 .
- Мацуда А., Сузуки Ю., Хонда Дж., Мурамацу С., Мацузаки О, Нагано И., Дои Т., Шимотохно К., Харада Т., Нисида Е., Хаяси Н., Сугано С. (май 2003 г.). «Крупномасштабная идентификация и характеристика человеческих генов, активирующих сигнальные пути NF-kappaB и MAPK» . Онкоген . 22 (21): 3307–18. DOI : 10.1038 / sj.onc.1206406 . PMID 12761501 .
- Ямамото К., Хамада Х, Синкай Х, Коно Й, Косеки Х, Аое Т. (сентябрь 2003 г.). «Рецептор KDEL модулирует стрессовую реакцию эндоплазматического ретикулума посредством сигнальных каскадов митоген-активируемой протеинкиназы» . Журнал биологической химии . 278 (36): 34525–32. DOI : 10.1074 / jbc.M304188200 . PMID 12821650 .
- Bard F, Mazelin L, Péchoux-Longin C, Malhotra V, Jurdic P (ноябрь 2003 г.). «Src регулирует структуру Гольджи и зависимый от рецептора KDEL ретроградный транспорт в эндоплазматический ретикулум» . Журнал биологической химии . 278 (47): 46601–6. DOI : 10.1074 / jbc.M302221200 . PMID 12975382 .
- Breuza L, Halbeisen R, Jenö P, Otte S, Barlowe C, Hong W., Hauri HP (ноябрь 2004 г.). «Протеомика мембран эндоплазматического ретикулума-промежуточного компартмента Гольджи (ERGIC) из клеток HepG2, обработанных брефельдином А, позволяет идентифицировать ERGIC-32, новый циклический белок, который взаимодействует с человеческим Erv46» . Журнал биологической химии . 279 (45): 47242–53. DOI : 10.1074 / jbc.M406644200 . PMID 15308636 .
- Юинг Р.М., Чу П., Элизма Ф, Ли Х, Тейлор П., Клими С., МакБрум-Цераевски Л., Робинсон, доктор медицины, О'Коннор Л., Ли М., Тейлор Р., Дхарси М., Хо Й, Хейлбут А., Мур Л., Чжан S, Орнатский O, Бухман YV, Ethier M, Sheng Y, Vasilescu J, Abu-Farha M, Lambert JP, Duewel HS, Stewart II, Kuehl B, Hogue K, Colwill K, Gladwish K, Muskat B, Kinach R, Adams С.Л., Моран М.Ф., Морин Г.Б., Топалоглоу Т., Фигейз Д. (2007). «Крупномасштабное картирование белок-белковых взаимодействий человека с помощью масс-спектрометрии» . Молекулярная системная биология . 3 (1): 89. DOI : 10.1038 / msb4100134 . PMC 1847948 . PMID 17353931 .