Глютаминовая кислота - Glutamic acid

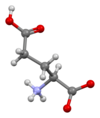
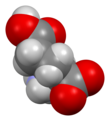
Скелетная формула из L глутаминовой кислоты
|
|||
|
|
|||

|
|||
| Имена | |||
|---|---|---|---|
|
Систематическое название ИЮПАК
2-аминопентандиовая кислота |
|||
| Другие имена
2-аминоглутаровая кислота
|
|||
| Идентификаторы | |||
|
3D модель ( JSmol )
|
|||
| 3DMet | |||
| 1723801 (L) 1723799 (rac) 1723800 (D) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard |
100.009.567 |
||
| Номер ЕС | |||
| Номер E | E620 (усилитель вкуса) | ||
| 3502 (л) 101971 (rac) 201189 (д) | |||
| КЕГГ | |||
|
PubChem CID
|
|||
| UNII | |||
|
Панель управления CompTox ( EPA )
|
|||
|
|||
|
|||
| Характеристики | |||
| C 5 H 9 N O 4 | |||
| Молярная масса | 147,130 г · моль -1 | ||
| Появление | белый кристаллический порошок | ||
| Плотность | 1,4601 (20 ° С) | ||
| Температура плавления | 199 ° С (390 ° F, 472 К) разлагается | ||
| 7,5 г / л (20 ° С) | |||
| Растворимость | 0,00035 г / 100 г этанола (25 ° C) |
||
| Кислотность (p K a ) | 2,10, 4,07, 9,47 | ||
| −78,5 · 10 −6 см 3 / моль | |||
| Опасности | |||
| Паспорт безопасности | См .: страницу данных | ||
| Пиктограммы GHS |

|
||
| Сигнальное слово GHS | Предупреждение | ||
| H315 , H319 , H335 | |||
| Р261 , Р264 , Р271 , Р280 , Р302 + 352 , Р304 + 340 , P305 + 351 + 338 , P312 , P321 , P332 + 313 , P337 + 313 , P362 , P403 + 233 , Р405 , Р501 | |||
| NFPA 704 (огненный алмаз) | |||
| Страница дополнительных данных | |||
|
Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. |
|||
|
Термодинамические
данные |
Фазовое поведение твердое тело – жидкость – газ |
||
| УФ , ИК , ЯМР , МС | |||
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|||
|
|
|||
| Ссылки на инфобоксы | |||
Глутаминовая кислота (символ Glu или Е ; ионная форма известна как глутамат ) представляет собой α- аминокислота , которая используется почти во всех живых существах в биосинтезе из белков . Для человека он несущественен, а это означает, что организм может его синтезировать. Это также возбуждающий нейротрансмиттер , фактически самый распространенный в нервной системе позвоночных . Он служит предшественником синтеза ингибирующей гамма-аминомасляной кислоты (ГАМК) в ГАМК-ергических нейронах.
Его молекулярная формула - C
5ЧАС
9НЕТ
4. Глутаминовая кислота существует в трех оптически изомерных формах; правовращающую L- форму обычно получают гидролизом глютена или из сточных вод производства свекловичного сахара или путем ферментации. Его молекулярную структуру можно было бы идеализировать как HOOC − CH ( NH
2) - ( CH
2) 2 -COOH, с двумя карбоксильными группами -COOH и одной аминогруппой - NH
2. Однако в твердом состоянии и слабокислых водных растворах молекула принимает электрически нейтральную цвиттерионную структуру - OOC − CH ( NH+
3) - ( CH
2) 2 -COOH. Он кодируется с помощью кодонов GAA или GAG.
Кислота может потерять один протон из своей второй карбоксильной группы с образованием конъюгированного основания , однозначно отрицательного аниона глутамата - OOC-CH ( NH+
3) - ( CH
2) 2 −COO - . Эта форма соединения преобладает в нейтральных растворах. Глутамат нейротрансмиттер играет главную роль в нервной активации . Этот анион придает пищу пикантный вкус умами и содержится в глутаматных ароматизаторах, таких как глутамат натрия . В Европе классифицируется как пищевая добавка E620 . В сильнощелочных растворах дважды отрицательный анион - OOC − CH ( NH
2) - ( CH
2) 2 −COO - преобладает. Радикал , соответствующий глутамата называется глутамил .
Химия
Ионизация
Когда глутаминовая кислота растворяется в воде, аминогруппа (- NH
2) может получить протон ( H+
), и / или карбоксильные группы могут терять протоны, в зависимости от кислотности среды.
В достаточно кислой среде аминогруппа приобретает протон, и молекула становится катионом с единственным положительным зарядом, HOOC-CH ( NH+
3) - ( CH
2) 2 -COOH.
При значениях pH от 2,5 до 4,1 карбоновая кислота, более близкая к амину, обычно теряет протон, и кислота становится нейтральным цвиттерионом - OOC-CH ( NH+
3) - ( CH
2) 2 -COOH. Это также форма соединения в твердом кристаллическом состоянии. Изменение состояния протонирования постепенное; две формы находятся в равных концентрациях при pH 2,10.
При еще более высоком pH другая группа карбоновой кислоты теряет свой протон, и кислота существует почти полностью в виде глутамат- аниона - OOC-CH ( NH+
3) - ( CH
2) 2 -COO - с одним отрицательным зарядом в целом. Изменение состояния протонирования происходит при pH 4,07. Эта форма, в которой оба карбоксилата лишены протонов, является доминирующей в физиологическом диапазоне pH (7,35–7,45).
При еще более высоком pH аминогруппа теряет лишний протон, и преобладающим видом является дважды отрицательный анион - OOC-CH ( NH
2) - ( CH
2) 2 −COO - . Изменение состояния протонирования происходит при pH 9,47.
Оптическая изомерия
Углерода атом прилегает к аминогруппе является хиральной (подключено к четырем различным группам). Глутаминовая кислота может существовать в трех оптических изомерах , включая правовращающую L- форму, d (-) и l (+). Л форма является одним из наиболее широко встречающихся в природе, но д форма встречается в некоторых специальных контекстах, например, клеточные стенки этих бактерий (которые могут его производство из л формы с ферментом глутаматом рацемазом ) и печенью из млекопитающих .
История
Хотя они естественным образом присутствуют во многих продуктах питания, вклад глутаминовой кислоты и других аминокислот во вкус был научно идентифицирован только в начале 20 века. Вещество было обнаружено и идентифицировано в 1866 году немецким химиком Карлом Генрихом Риттхаузеном , который обработал пшеничный глютен (в честь которого он был назван) серной кислотой . В 1908 году японский исследователь Кикунаэ Икеда из Токийского императорского университета идентифицировал коричневые кристаллы, оставшиеся после испарения большого количества бульона комбу, как глутаминовую кислоту. Эти кристаллы, когда их попробовали, воспроизводили невыразимый, но неоспоримый аромат, который он обнаруживал во многих продуктах, особенно в морских водорослях. Профессор Икеда назвал этот аромат умами . Затем он запатентовал метод массового производства кристаллической соли глутаминовой кислоты, глутамата натрия .
Синтез
Биосинтез
| Реагенты | Продукты | Ферменты |
|---|---|---|
| Глютамин + H 2 O | → Глу + NH 3 | GLS , GLS2 |
| NAcGlu + H 2 O | → Глю + ацетат | N- ацетил-глутамат-синтаза |
| α-кетоглутарат + НАДФ H + NH 4 + | → Глу + НАДФ + + Н 2 О | GLUD1 , GLUD2 |
| α-кетоглутарат + α-аминокислота | → Глу + α-кетокислота | трансаминаза |
| 1-пирролин-5-карбоксилат + НАД + + H 2 O | → Глу + НАДН | ALDH4A1 |
| N-формино-L-глутамат + FH 4 | → Glu + 5-формимино-FH 4 | FTCD |
| НААГ | → Глу + НАА | GCPII |
Промышленный синтез
Глутаминовая кислота производится в наибольших масштабах из всех аминокислот, с расчетным годовым производством около 1,5 миллиона тонн в 2006 году. На смену химическому синтезу пришла аэробная ферментация сахаров и аммиака в 1950-х годах с организмом Corynebacterium glutamicum (также известный as Brevibacterium flavum ), наиболее широко используемого в производстве. Выделение и очистка могут быть достигнуты путем концентрирования и кристаллизации ; он также широко доступен в виде гидрохлоридной соли.
Функция и использование
Метаболизм
Глутамат - ключевое соединение в клеточном метаболизме . У человека пищевые белки расщепляются на аминокислоты , которые служат метаболическим топливом для других функциональных ролей в организме. Ключевым процессом деградации аминокислот является трансаминирование , при котором аминогруппа аминокислоты переносится на α-кетокислоту, обычно катализируемую трансаминазой . Реакцию можно обобщить как таковую:
- R 1 -аминокислота + R 2 -α- кетокислота ⇌ R 1 -α-кетокислота + R 2 -аминокислота
Очень распространенной α-кетокислотой является α-кетоглутарат, промежуточное соединение в цикле лимонной кислоты . Трансаминирование α-кетоглутарата дает глутамат. Полученный продукт α-кетокислоты также часто является полезным, который может использоваться в качестве топлива или в качестве субстрата для дальнейших процессов метаболизма. Вот примеры:
- Аспартат + α-кетоглутарат ⇌ оксалоацетат + глутамат
И пируват, и оксалоацетат являются ключевыми компонентами клеточного метаболизма, участвуя в качестве субстратов или промежуточных продуктов в фундаментальных процессах, таких как гликолиз , глюконеогенез и цикл лимонной кислоты .
Глутамат также играет важную роль в избавлении организма от избыточного или отработанного азота . Глутамат подвергается дезаминированию , окислительной реакции, катализируемой глутаматдегидрогеназой , а именно:
Аммиак (в виде аммония ) выводится преимущественно в виде мочевины , синтезируемой в печени . Таким образом, трансаминирование может быть связано с дезаминированием, что позволяет эффективно удалять азот из аминогрупп аминокислот через глутамат в качестве промежуточного соединения и, наконец, выводиться из организма в форме мочевины.
Глутамат также является нейромедиатором (см. Ниже), что делает его одной из самых распространенных молекул в головном мозге. Злокачественные опухоли головного мозга, известные как глиома или глиобластома, используют это явление, используя глутамат в качестве источника энергии, особенно когда эти опухоли становятся более зависимыми от глутамата из-за мутаций в гене IDH1 .
Нейротрансмиттер
Глутамат является наиболее распространенным возбуждающим нейромедиатором в нервной системе позвоночных . В химических синапсах глутамат хранится в пузырьках . Нервные импульсы вызывают высвобождение глутамата из пресинаптической клетки. Глутамат действует на ионотропные и метаботропные (связанные с G-белком) рецепторы. В противоположной постсинаптической клетке рецепторы глутамата , такие как рецептор NMDA или рецептор AMPA , связывают глутамат и активируются. Из-за своей роли в синаптической пластичности глутамат участвует в когнитивных функциях, таких как обучение и память в головном мозге. Форма пластичности, известная как долговременная потенциация, имеет место в глутаматергических синапсах в гиппокампе , неокортексе и других частях мозга. Глутамат работает не только как двухточечный передатчик, но также через синаптические перекрестные помехи между синапсами, в которых сумма глутамата, высвобождаемого из соседнего синапса, создает внесинаптическую передачу сигналов / объемную передачу . Кроме того, глутамат играет важную роль в регуляции конусов роста и синаптогенеза во время развития мозга, как первоначально описано Марком Маттсоном .
Мозговые несинаптические глутаматергические сигнальные цепи
Было обнаружено, что внеклеточный глутамат в мозге дрозофилы регулирует кластеризацию постсинаптических рецепторов глутамата посредством процесса, включающего десенсибилизацию рецепторов. Ген, экспрессируемый в глиальных клетках, активно транспортирует глутамат во внеклеточное пространство , в то время как в ядре, стимулирующем метаботропные рецепторы глутамата II группы, этот ген, как было обнаружено, снижает уровни внеклеточного глутамата. Это повышает вероятность того, что этот внеклеточный глутамат играет «эндокринную» роль как часть более крупной гомеостатической системы.
Предшественник ГАМК
Глутамат также служит предшественником синтеза ингибирующей гамма-аминомасляной кислоты (ГАМК) в ГАМК-ергических нейронах. Эта реакция катализируется глутаматдекарбоксилазой (GAD), которая наиболее распространена в мозжечке и поджелудочной железе .
Синдром скованного человека - это неврологическое заболевание, вызываемое антителами против GAD, приводящее к снижению синтеза ГАМК и, следовательно, к нарушению двигательной функции, такой как жесткость мышц и спазм. Поскольку в поджелудочной железе много ГТР, в поджелудочной железе происходит прямое иммунологическое разрушение, и у пациентов возникает сахарный диабет.
Усилитель вкуса
Глутаминовая кислота, входящая в состав белка, присутствует в пищевых продуктах, содержащих белок, но ее можно попробовать только тогда, когда она присутствует в несвязанной форме. Значительные количества свободной глутаминовой кислоты присутствует в широком разнообразии продуктов, включая сыры и соевый соус , и глутаминовая кислота отвечает за умы , один из пяти основных вкусов человеческого чувства вкуса . Глутаминовая кислота часто используется в качестве пищевой добавки и усилителя вкуса в виде ее натриевой соли , известной как глутамат натрия ( глутамат натрия ).
Питательный
Все мясо, птица, рыба, яйца, молочные продукты и комбу являются отличными источниками глутаминовой кислоты. Некоторые богатые белком растительные продукты также служат его источниками. От 30% до 35% глютена (большая часть белка в пшенице) составляет глутаминовая кислота. Девяносто пять процентов пищевого глутамата метаболизируется клетками кишечника за первый проход.
Рост растений
Ауксигро - это препарат для выращивания растений, содержащий 30% глутаминовой кислоты.
ЯМР-спектроскопия
В последние годы было проведено много исследований по использованию остаточной диполярной связи (RDC) в спектроскопии ядерного магнитного резонанса (ЯМР). Производное глутаминовой кислоты, поли-γ-бензил-L-глутамат (PBLG), часто используется в качестве среды для выравнивания, чтобы контролировать масштаб наблюдаемых диполярных взаимодействий.
Фармакология
Препарат фенциклидин (более известный как PCP) неконкурентно противодействует глутаминовой кислоте в отношении рецептора NMDA . По тем же причинам декстрометорфан и кетамин также обладают сильным диссоциативным и галлюциногенным действием («Ангельская пыль», как наркотик). Острое вливание препарата LY354740 (также известный как eglumegad , с агонистом из метаботропных глутаматных рецепторов , 2 и 3 ) приводило к заметному уменьшению йохимбиной индуцированной стрессовой реакции в капоте макака ( Macaca Радиате ); хроническое пероральное введение LY354740 этим животным привело к заметному снижению исходных уровней кортизола (примерно на 50 процентов) по сравнению с необработанными контрольными субъектами. LY354740 также был продемонстрирован действовать на метаботропном глутаматном рецепторе 3 (GRM3) человеческих адренокортикальные клетки , понижающую регуляции альдостеронсинтаза , CYP11B1 и производство надпочечниковых стероидов (т.е. альдостерон и кортизол ). Глутамат нелегко проходит через гематоэнцефалический барьер , вместо этого он транспортируется высокоаффинной транспортной системой. Он также может превращаться в глютамин .
Смотрите также
использованная литература
дальнейшее чтение
- Нельсон, Дэвид Л .; Кокс, Майкл М. (2005). Принципы биохимии (4-е изд.). Нью-Йорк: В. Х. Фриман. ISBN 0-7167-4339-6.