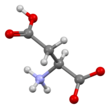
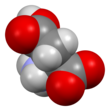
Аспарагиновая кислота - Aspartic acid

Скелетная формула из L -aspartic кислоты
|
|||
|
|
|||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК | |||
| Другие имена | |||
| Идентификаторы | |||
|
3D модель ( JSmol )
|
|||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard |
100.000.265 |
||
| Номер ЕС | |||
| КЕГГ | |||
|
PubChem CID
|
|||
| UNII | |||
|
Панель управления CompTox ( EPA )
|
|||
|
|||
|
|||
| Характеристики | |||
| C 4 H 7 N O 4 | |||
| Молярная масса | 133,103 г · моль -1 | ||
| Появление | бесцветные кристаллы | ||
| Плотность | 1,7 г / см 3 | ||
| Температура плавления | 270 ° С (518 ° F, 543 К) | ||
| Точка кипения | 324 ° С (615 ° F, 597 К) (разлагается) | ||
| 4,5 г / л | |||
| Кислотность (p K a ) | |||
| Основание конъюгата | Аспартат | ||
| -64,2 · 10 −6 см 3 / моль | |||
| Опасности | |||
| Паспорт безопасности | См .: страницу данных | ||
| NFPA 704 (огненный алмаз) | |||
| Страница дополнительных данных | |||
|
Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. |
|||
|
Термодинамические
данные |
Фазовое поведение твердое тело – жидкость – газ |
||
| УФ , ИК , ЯМР , МС | |||
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|||
|
|
|||
| Ссылки на инфобоксы | |||
Аспарагиновая кислота (символ Asp или D ; ионная форма известна как аспартат ) - это α-аминокислота, которая используется в биосинтезе белков. Как и все другие аминокислоты, он содержит аминогруппу и карбоновую кислоту. Его α-аминогруппа находится в протонированной –NH+
3образуются в физиологических условиях, в то время как его группа α-карбоновой кислоты депротонирована -COO - в физиологических условиях. Аспарагиновая кислота имеет кислотную боковую цепь (CH 2 COOH), которая реагирует с другими аминокислотами, ферментами и белками в организме. В физиологических условиях (pH 7,4) в белках боковая цепь обычно присутствует в виде отрицательно заряженной формы аспартата -COO - . Для человека это незаменимая аминокислота , а это значит, что организм может синтезировать ее по мере необходимости. Он кодируется с помощью кодонов GAT и GAC. В мРНК, CUA и CUG.
D- аспартат - одна из двух D- аминокислот, обычно встречающихся у млекопитающих. [3]
В белках аспартатные боковые цепи часто связаны водородными связями с образованием asx-витков или asx-мотивов , которые часто встречаются на N-концах альфа-спиралей .
Л -изомер Asp является одним из 22 протеиногенных аминокислот , то есть, строительные блоки белков . Аспарагиновая кислота, как и глутаминовая кислота , классифицируется как кислая аминокислота с pK a 3,9, однако в пептиде она сильно зависит от местной среды и может достигать 14. Asp широко участвует в биосинтезе.
Открытие
Аспарагиновая кислота была впервые обнаружена в 1827 году Огюстом-Артура Plisson и Étienne Ossian Генри путем гидролиза из аспарагина , который был выделен из спаржи сока в 1806. Их оригинальный метод использовали свинец гидроксид , но различные другие кислоты или основания, теперь более часто используется вместо .
Формы и номенклатура
Есть две формы или энантиомеры аспарагиновой кислоты. Название «аспарагиновая кислота» может относиться либо к энантиомеру, либо к их смеси. Из этих двух форм только одна, « L- аспарагиновая кислота», непосредственно включается в белки. Биологические роли его аналога, « D- аспарагиновой кислоты» более ограничены. В тех случаях, когда ферментативный синтез приводит к тому или иному, в большинстве химических синтезов образуются обе формы, DL- аспарагиновая кислота, известная как рацемическая смесь .
Синтез
Биосинтез
В человеческом теле, аспартаты наиболее часто синтезируют через переаминирование из оксалоацетата . Биосинтез аспартата облегчается ферментом аминотрансферазой : перенос аминогруппы от другой молекулы, такой как аланин или глутамин, дает аспартат и альфа-кетокислоту.
Аспартат также играет важную роль в цикле мочевины .
Химический синтез
В промышленности аспартат получают аминированием фумарата, катализируемым L- аспартатаммиаклиазой .
Рацемическая аспарагиновая кислота может быть синтезирована из фталимидомалоната диэтил натрия (C 6 H 4 (CO) 2 NC (CO 2 Et) 2 ).
Метаболизм
У растений и микроорганизмов аспартат является предшественником нескольких аминокислот, в том числе четырех незаменимых для человека: метионина , треонина , изолейцина и лизина . Превращение аспартата в эти другие аминокислоты начинается с восстановления аспартата до его «полуальдегида», O 2 CCH (NH 2 ) CH 2 CHO. Аспарагин получают из аспартата путем трансамидирования:
- -O 2 CCH (NH 2 ) CH 2 CO 2 - + G C (O) NH 3 + O 2 CCH (NH 2 ) CH 2 CONH 3 + + G C (O) O
(где G C (O) NH 2 и G C (O) OH - глутамин и глутаминовая кислота соответственно)
Участие в цикле мочевины
В цикле мочевины аспартат и аммиак отдают аминогруппы, что приводит к образованию мочевины .
Другие биохимические роли
Аспартат выполняет множество других биохимических ролей. Это метаболит в цикле мочевины и участвует в глюконеогенезе . Он несет восстанавливающие эквиваленты в челноке малат-аспартат , который использует готовое взаимное превращение аспартата и оксалоацетата , который является окисленным (дегидрированным) производным яблочной кислоты . Аспартат отдает один атом азота в биосинтезе инозина , предшественника пуриновых оснований. Кроме того, аспарагиновая кислота действует как акцептор водорода в цепи АТФ-синтазы. Диетический L-аспарагиновой кислоты , как было показано , чтобы действовать в качестве ингибитора бета-глюкуронидазы , который служит для регулирования энтерогепатической циркуляции из билирубина и желчных кислот.
Интерактивная карта проезда
Нажмите на гены, белки и метаболиты ниже, чтобы ссылки на соответствующие статьи.
Нейротрансмиттер
Аспартат ( конъюгированная основа аспарагиновой кислоты) стимулирует рецепторы NMDA , хотя и не так сильно, как аминокислотный нейромедиатор L-глутамат .
Приложения и рынок
В 2014 году мировой рынок аспарагиновой кислоты составлял 39,3 тысячи коротких тонн (35,7 тысячи тонн ) или около 117 миллионов долларов в год, при этом потенциальные области роста приходятся на адресный рынок в размере 8,78 миллиардов долларов (миллиардов). Три крупнейших рыночных сегмента включают США, Западную Европу и Китай. Текущие применения включают биоразлагаемые полимеры ( полиаспарагиновая кислота ), низкокалорийные подсластители ( аспартам ), ингибиторы образования накипи и коррозии, а также смолы.
Супервпитывающие полимеры
Одна из областей роста рынка аспарагиновой кислоты - это биоразлагаемые суперабсорбирующие полимеры (SAP) и гидрогели. Ожидается, что рынок супервпитывающих полимеров будет расти со среднегодовыми темпами роста 5,5% с 2014 по 2019 год и достигнет мировой величины в 8,78 млрд долларов. Около 75% супервпитывающих полимеров используется в одноразовых подгузниках, а еще 20% используются при недержании мочи у взрослых и предметах женской гигиены . Полиаспарагиновая кислота , продукт полимеризации аспарагиновой кислоты, представляет собой биоразлагаемый заменитель полиакрилата . Рынок полиаспартата составляет небольшую долю (примерно <1%) от общего рынка SAP.
Дополнительное использование
Помимо SAP, аспарагиновая кислота находит применение в производстве удобрений стоимостью 19 миллиардов долларов, где полиаспартат улучшает удержание воды и поглощение азота; рынок покрытий для бетонных полов стоимостью 1,1 миллиарда долларов (2020 г.), где полиаспарагиновая кислота представляет собой низкоэнергетическую альтернативу традиционным эпоксидным смолам с низким содержанием летучих органических соединений; и, наконец, рынок ингибиторов образования накипи и коррозии стоимостью более 5 миллиардов долларов.
Источники
Диетические источники
Аспарагиновая кислота не является незаменимой аминокислотой , что означает, что она может синтезироваться из промежуточных продуктов центрального метаболического пути у человека. Однако аспарагиновая кислота содержится в:
- Источники животного происхождения: устрицы, мясные закуски, колбасы, дичь.
- Растительные источники: проросшие семена, овсяные хлопья, авокадо , спаржа, молодой сахарный тростник и патока из сахарной свеклы .
- Пищевые добавки в виде самой аспарагиновой кислоты или солей (например, аспартата магния )
- Подсластитель аспартам , аспарагиновая кислота, фенилаланин , тример формальдегида (бренды: NutraSweet, Equal, Canderel и др.)
Смотрите также
- Аспартат трансаминаза
- Полиаспарагиновая кислота
- Поли (аспартат) натрия , синтетический полиамид
использованная литература
внешние ссылки
- GMD MS Spectrum
- Американское химическое общество (21 апреля 2010 г.). "Кристалл Евы предков может объяснить происхождение леворукости жизни" . ScienceDaily . Архивировано 23 апреля 2010 года . Проверено 21 апреля 2010 .