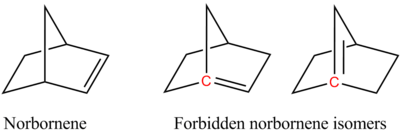
Кольцевая деформация - Ring strain
В области органической химии , кольцо штамм представляет собой тип нестабильности , которая существует , когда в молекуле углов формы , которые являются ненормальными. Деформация чаще всего обсуждается для небольших колец, таких как циклопропаны и циклобутаны, внутренние углы которых существенно меньше идеализированного значения приблизительно 109 °. Из-за их высокой деформации теплота сгорания этих маленьких колец повышена.
Кольцевая деформация является результатом комбинации угловой деформации , конформационной деформации или деформации Питцера (торсионные затменные взаимодействия) и трансаннулярной деформации , также известной как деформация Ван-дер-Ваальса или деформация Прелога . Простейшими примерами угловой деформации являются небольшие циклоалканы, такие как циклопропан и циклобутан.
Угловая деформация (деформация Байера)
Алканы
В алканах оптимальное перекрытие атомных орбиталей достигается при 109,5 °. Наиболее распространенные циклические соединения имеют в своем кольце пять или шесть атомов углерода. Адольф фон Байер получил Нобелевскую премию в 1905 году за открытие теории деформации Байера, которая объясняла относительную стабильность циклических молекул в 1885 году.
Угловая деформация возникает, когда валентные углы отклоняются от идеальных валентных углов для достижения максимальной прочности связи в определенной химической конформации . Угловая деформация обычно влияет на циклические молекулы, которым не хватает гибкости ациклических молекул.
Угловая деформация дестабилизирует молекулу, что проявляется в более высокой реакционной способности и повышенной теплоте сгорания . Максимальная прочность связи является результатом эффективного перекрытия атомных орбиталей в химической связи . Количественным показателем угловой деформации является энергия деформации . Угловая деформация и деформация кручения вместе создают кольцевую деформацию, которая влияет на циклические молекулы.
- C n H 2 n + 3/2n O 2 → n CO 2 + n H 2 O - Δ H горение
Нормированные энергии, которые позволяют сравнивать кольцевые деформации, получают путем измерения молярной теплоты сгорания циклоалканов на метиленовую группу (CH 2 ).
- Δ H горение на CH 2 - 658,6 кДж = деформация на CH 2
Значение 658,6 кДж на моль получено для недеформированного длинноцепочечного алкана.
| Размер кольца | Энергия деформации (ккал / моль) | Размер кольца | Энергия деформации (ккал / моль) | |
|---|---|---|---|---|
| 3 | 27,5 | 10 | 12,4 | |
| 4 | 26,3 | 11 | 11,3 | |
| 5 | 6.2 | 12 | 4.1 | |
| 6 | 0,1 | 13 | 5.2 | |
| 7 | 6.2 | 14 | 1.9 | |
| 8 | 9,7 | 15 | 1.9 | |
| 9 | 12,6 | 16 | 2.0 |
Угловая деформация в алкенах
Циклические алкены подвержены деформации в результате искажения sp 2 -гибридизованных углеродных центров. Иллюстративным является C 60, где углеродные центры пирамидализированы. Это искажение увеличивает реакционную способность этой молекулы. Угловая деформация также является основой правила Бредта, согласно которому углеродные центры-мосты не включаются в алкены, потому что образующийся алкен будет подвергаться экстремальной угловой деформации.
Примеры
В циклоалканах каждый углерод неполярно ковалентно связан с двумя атомами углерода и двумя атомами водорода. Углероды имеют гибридизацию sp 3 и должны иметь идеальные валентные углы 109,5 °. Однако из-за ограничений циклической структуры идеальный угол достигается только в шестиуглеродном кольце - циклогексан в конформации кресло . Для других циклоалканов валентные углы отклоняются от идеальных.
Молекулы с высокой степенью кольцевой деформации состоят из трех, четырех и нескольких пятичленных колец, включая: циклопропаны , циклопропены , циклобутаны , циклобутены , [1,1,1] пропелланы , [2,2,2] пропелланы , эпоксиды. , азиридины , циклопентены и норборнены . Эти молекулы имеют углы связи между кольцевыми атомами, которые являются более острыми, чем оптимальные тетраэдрические (109,5 °) и тригональные плоские (120 °) валентные углы, необходимые для их соответствующих связей sp 3 и sp 2 . Из-за меньших углов связи связи имеют более высокую энергию и принимают более p-характер, чтобы уменьшить энергию связей. Кроме того, кольцевые структуры циклопропанов / енов и циклобутанов / енов предлагают очень небольшую конформационную гибкость. Таким образом, заместители в кольцевых атомах существуют в закрытой конформации в циклопропанах и между гошем и закрытой в циклобутанах, внося вклад в более высокую энергию деформации кольца в форме отталкивания Ван-дер-Ваальса.
- циклопропан , C 3 H 6 - валентные углы CCC равны 60 °, тогда как тетраэдрические валентные углы 109,5 ° ожидаются. Сильная угловая деформация приводит к нелинейному орбитальному перекрытию его sp 3 -орбиталей. Из-за нестабильности связи циклопропан более реакционноспособен, чем другие алканы. Поскольку любые три точки составляют плоскость, а циклопропан имеет только три атома углерода, циклопропан плоский. Угол связи HCH составляет 115 °, тогда как ожидается 106 °, как и в группах CH 2 пропана.
- циклобутан , C 4 H 8 - если бы он был полностью квадратным, его валентные углы были бы 90 °, тогда как тетраэдрические валентные углы 109,5 ° ожидались бы. Однако фактический угол скрепления CCC составляет 88 °, потому что он имеет слегка загнутую форму, чтобы уменьшить некоторую скручивающую деформацию за счет немного большей угловой деформации. Высокая энергия деформации циклобутана обусловлена главным образом угловой деформацией.
- циклопентан , C 5 H 10 - если бы это был полностью правильный плоский пятиугольник, его валентные углы были бы 108 °, но ожидаются тетраэдрические валентные углы 109,5 °. Однако он имеет незакрепленную морщинистую форму, которая волнообразно движется вверх и вниз.
- циклогексан, C 6 H 12 - Хотя конформация кресла способна достигать идеальных углов, нестабильная конформация полукресла имеет угловую деформацию в углах CCC, которые находятся в диапазоне от 109,86 ° до 119,07 °.
- оксид этилена , CH 2 OCH 2
- кубан , C 8 H 8
Кольцевая деформация может быть значительно выше в бициклических системах . Например, бициклобутан , C 4 H 6 , известен как одно из наиболее напряженных соединений, которые можно выделить в больших масштабах; его энергия деформации оценивается в 63,9 ккал моль -1 (267 кДж моль -1 ).
заявка
Потенциальная энергия и уникальная структура связи, содержащаяся в связях молекул с напряжением кольца, могут использоваться для управления реакциями в органическом синтезе . Примерами таких реакций являются метатезис-полимеризация с раскрытием цикла , фотоиндуцированное раскрытие цикла циклобутенов и нуклеофильное раскрытие цикла эпоксидов и азиридинов .