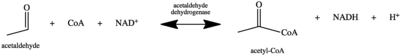Ацетальдегиддегидрогеназа - Acetaldehyde dehydrogenase
| Ацетальдегиддегидрогеназа (ацетилирование) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
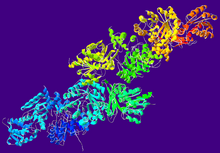 Кристаллографическая структура ацетальдегиддегидрогеназы из Pseudomonas sp .
| |||||||||
| Идентификаторы | |||||||||
| ЕС нет. | 1.2.1.10 | ||||||||
| № CAS | 9028-91-5 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | Amigo / QuickGO | ||||||||
| |||||||||
Дегидрогеназы ацетальдегида ( EC 1.2.1.10 ) представляют собой ферменты дегидрогеназы, которые катализируют превращение ацетальдегида в уксусную кислоту . Окисление ацетальдегида до ацетата можно резюмировать следующим образом:
Ацетальдегид + НАД + + Коэнзим А ↔ Ацетил-КоА + НАДН + H +
У человека есть три известных гена, кодирующих эту ферментативную активность: ALDH1A1 , ALDH2 и недавно обнаруженный ALDH1B1 (также известный как ALDH5 ). Эти ферменты являются членами более широкого класса альдегиддегидрогеназ .
Номер CAS для этого типа фермента [9028-91-5].
Состав
Цистеин- 302 является одним из трех последовательных остатков Cys и имеет решающее значение для каталитической функции фермента . Остаток алкилируется йодацетамидом как в цитозольном, так и в митохондриальном изоферментах, с модификациями Cys-302, указывающими на каталитическую активность по отношению к другим остаткам. Кроме того, предыдущая последовательность Gln-Gly-Gln-Cys консервативна в обоих изоферментах как для человека, так и для лошади, что согласуется с тем, что Cys-302 имеет решающее значение для каталитической функции.
Как было обнаружено с помощью сайт-направленного мутагенеза , глутамат- 268 является ключевым компонентом ацетальдегиддегидрогеназы печени и также имеет решающее значение для каталитической активности. Поскольку активность мутантов не может быть восстановлена добавлением общих оснований, предполагается, что остаток функционирует как общее основание для активации существенного остатка Cys-302.
У бактерий ацилирующая ацетальдегиддегидрогеназа образует бифункциональный гетеродимер с металл-зависимой 4-гидрокси-2-кетовалерат альдолазой . Используемый в бактериальной деградации токсичных ароматических соединений, кристаллическая структура фермента указывает на то, что промежуточные соединения перемещаются непосредственно между активными центрами через гидрофобный промежуточный канал, обеспечивая инертную среду, в которой реактивный промежуточный ацетальдегид перемещается из активного центра альдолазы в ацетальдегиддегидрогеназу. активный сайт. Такая связь между белками позволяет эффективно переносить субстраты с одного активного сайта на другой.
Эволюция
Хотя два изофермента (ALDH1 и ALDH2) не имеют общей субъединицы, гомология между белками ALDH1 и ALDH2 человека составляет 66% на уровне кодирующих нуклеотидов и 69% на уровне аминокислот , что ниже, чем у 91% гомологии между человеческим ALDH1 и лошадиным ALDH1. Такое открытие согласуется с доказательствами, свидетельствующими о раннем эволюционном расхождении между цитозольными и митохондриальными изоферментами, как видно из 50% гомологии между митохондриальной и цитозольной аспаратат-аминотрансферазами свиней.
Роль в метаболизме алкоголя
В печени , этанол превращается в безвредную уксусную кислоту (основная кислота в уксусе ) с помощью двухстадийного процесса. На первом этапе этанол превращается в ацетальдегид алкогольдегидрогеназой . На втором этапе ацетальдегид превращается в уксусную кислоту под действием ацетальдегиддегидрогеназы. Ацетальдегид более токсичен, чем алкоголь, и вызывает многие симптомы похмелья .
Около 50% людей Northeast азиатского происхождения имеют доминирующую мутацию в их ацетальдегид дегидрогеназы гена , что делает этот фермент менее эффективным, который вызывает реакцию флеш алкоголя , также известный как синдром азиатского смыва. Подобная мутация обнаруживается примерно у 5–10% светловолосых голубоглазых людей североевропейского происхождения. У этих людей ацетальдегид накапливается после употребления алкоголя, что приводит к симптомам отравления ацетальдегидом, включая характерное покраснение кожи и учащенное сердцебиение и частоту дыхания. Другие симптомы могут включать сильные спазмы в животе и мочевыводящих путях, приливы жара и холода, обильное потоотделение и глубокое недомогание . Люди с недостаточной активностью ацетальдегиддегидрогеназы гораздо реже становятся алкоголиками , но, по-видимому, они подвергаются большему риску повреждения печени, алкогольной астмы и рака ротоглотки и пищевода из-за чрезмерного воздействия ацетальдегида.
Это демонстрирует, что многие из токсических эффектов этанола опосредуются метаболитом ацетальдегида и поэтому могут быть смягчены такими веществами, как фомепизол, который эффективно снижает скорость превращения этанола в ацетальдегид in vivo .
ALDH2, который имеет более низкую K M для ацетальдегидов , чем ALDH1 и действует преимущественно в митохондриях, является основным ферментом в ацетальдегид метаболизма и имеет три генотипа. Одноточечная мутация (G → A) в экзоне 12 гена ALDH2 вызывает замену глутамина лизином по остатку 487, в результате чего образуется фермент ALDH2K. ALDH2K имеет повышенный K M для NAD + , что делает его практически неактивным при клеточных концентрациях NAD + . Поскольку ALDH2 представляет собой рандомизированный тетрамер, активность гетеро-мутированного генотипа снижена до 6% по сравнению с диким типом, в то время как гомомутантные генотипы обладают практически нулевой ферментативной активностью. Субъединица с дефицитом ALDH2 является доминирующей при гибридизации с субъединицей дикого типа, что приводит к инактивации изофермента за счет нарушения каталитической активности и увеличения оборота. Генетическая изменчивость ALDH2 тесно связана с алкогольной зависимостью , при этом гетерозиготы имеют меньший риск по сравнению с гомозиготами дикого типа и отдельные гомозиготы по ALDH2-дефициту с очень низким риском алкоголизма.
Препарат дисульфирам (Антабус) предотвращает окисление ацетальдегида до уксусной кислоты и используется при лечении алкоголизма. ALDH1 сильно ингибируется дисульфирамом, в то время как ALDH2 устойчив к его действию. Остаток цистеина 302 в ALDH1 и 200 в ALDH2 участвует в качестве сайта связывания дисульфирама на ферменте и служит сайтом тиола, чувствительным к дисульфираму. Ковалентное связывание дисульфирама с тиолом блокирует связывание одного из остатков цистеина с йодацетамидом, тем самым инактивируя фермент и значительно снижая каталитическую активность. Активность можно восстановить обработкой 2-меркаптоэтанолом , но не глутатионом .
Метронидазол (Флагил), который используется для лечения некоторых паразитарных инфекций, а также псевдомембранозного колита, вызывает эффекты, аналогичные дисульфираму. Коприн (который является аминокислотой, содержащейся в некоторых коприноидных грибах) метаболизируется in vivo до 1-аминоциклопропанола, который также вызывает аналогичные эффекты.
Роль в метаболизме жиров
ALDH1 участвует в метаболизме витамина А. Модели на животных предполагают, что отсутствие гена связано с защитой от висцерального ожирения ( PMC 2233696 ).
Смотрите также
использованная литература
внешние ссылки
- ацетальдегид + дегидрогеназа в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)