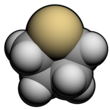
Тетрагидротиофен - Tetrahydrothiophene
|
|
|||
| Имена | |||
|---|---|---|---|
|
Предпочтительное название IUPAC
Тиолан |
|||
| Другие названия
Тетрагидротиофен,
тиофан, сульфид тетраметилена |
|||
| Идентификаторы | |||
|
3D модель ( JSmol )
|
|||
| Сокращения | THT | ||
| 102392 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard |
100.003.391 |
||
| Номер ЕС | |||
|
PubChem CID
|
|||
| Номер RTECS | |||
| UNII | |||
| Номер ООН | 2412 | ||
|
Панель управления CompTox ( EPA )
|
|||
|
|||
|
|||
| Характеристики | |||
| C 4 H 8 S | |||
| Молярная масса | 88,17 г · моль -1 | ||
| Плотность | 0,997 г / мл | ||
| Температура плавления | -96 ° С (-141 ° F, 177 К) | ||
| Точка кипения | 119 ° С (246 ° F, 392 К) | ||
| Опасности | |||
| Основные опасности | Зловоние, легковоспламеняющийся, раздражающий | ||
| Паспорт безопасности | Дуб | ||
| Пиктограммы GHS |
 
|
||
| Сигнальное слово GHS | Опасность | ||
| H225 , H302 , H312 , H315 , H319 , H332 , H412 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P261 , P264 , P270 , P271 , P273 , P280 , P301 + 312 , P302 + 352 , P303 + 361 + 353 , P304 + 312 , P304 + 340 , P305 + 351 + 338 , P312 , P321 , P322 , P330 , P332 + 313 , P337 + 313 , P362 | |||
| точка возгорания | 12 ° С (54 ° F, 285 К) | ||
| 200 ° С (392 ° F, 473 К) | |||
| Родственные соединения | |||
|
Родственные соединения
|
Tetrahydrofuran , тиофен , Selenolane , тиазолидин , дитиолан , Thiane | ||
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|||
|
|
|||
| Ссылки на инфобоксы | |||
Тетрагидротиофен представляет собой сероорганическое соединение с формулой (CH 2 ) 4 S. Он содержит пятичленное кольцо, состоящее из четырех атомов углерода и атома серы . Это насыщенный аналог из тиофен . Это летучая бесцветная жидкость с очень неприятным запахом . Он также известен как тиофан , тиолан или THT .
Синтез и реакции
Тетрагидротиофен получают реакцией тетрагидрофурана с сероводородом . Эта парофазная реакция катализируется оксидом алюминия и другими гетерогенными кислотными катализаторами.
Это соединение является лигандом в координационной химии , примером является комплексный хлор (тетрагидротиофен) золото (I) .
Окисление THT дает растворитель, называемый сульфоланом , полярный растворитель почти без запаха. Сульфолан обычно получают из бутадиена.
Естественное явление
Сообщается, что в природе встречаются как незамещенные, так и замещенные тетрагидротиофены. Например, тетрагидротиофен встречается в виде летучего вещества из Eruca sativa Mill. (салатная ракета), в то время как моноциклические замещенные тетрагидротиофены были выделены из Allium fistulosum 'Kujou', Allium sativum (чеснок), Allium cepa (лук), Allium schoenoprasum ( чеснок) и Salacia prinoides. Альбомицины представляют собой группу содержащих тетрагидротиофеновое кольцо антибиотиков из стрептомицетов, в то время как биотин и неотиобинуфаридин (и другие алкалоиды нуфара ) являются примерами природных продуктов, содержащих бициклическое и полициклическое тетрагидротиофеновое кольцо, соответственно.
Приложения
Из-за своего запаха тетрагидротиофен использовался в качестве одоранта в сжиженном нефтяном газе , хотя больше не в Северной Америке. Он также используется в качестве одоранта для природного газа , обычно в смесях, содержащих трет-бутилтиол .
Тетрагидротиофен представляет собой основание Льюиса, классифицируемое как мягкое основание, и его донорные свойства обсуждаются в модели ECW .