Фактор 1 из стромальных клеток - Stromal cell-derived factor 1
Стромальных клеток , полученных фактор 1 ( SDF - 1 ), также известный как СХС мотив хемокинов 12 (CXCL12), представляет собой хемокин белок , который у человека кодируется CXCL12 гена на хромосоме 10 . Он повсеместно экспрессируется во многих тканях и типах клеток. Факторы 1-альфа и 1-бета, происходящие из стромальных клеток, представляют собой небольшие цитокины, принадлежащие к семейству хемокинов , члены которого активируют лейкоциты и часто индуцируются провоспалительными стимулами, такими как липополисахарид , TNF или IL1 . Хемокины характеризуются наличием 4 консервативных цистеинов, которые образуют 2 дисульфидные связи . Их можно разделить на 2 подсемейства. В подсемействе СС остатки цистеина примыкают друг к другу. В подсемействе CXC они разделены промежуточной аминокислотой. Белки SDF1 относятся к последней группе. Передача сигналов CXCL12 наблюдалась при нескольких видах рака. Ген CXCL12 также содержит один из 27 SNP, связанных с повышенным риском ишемической болезни сердца .
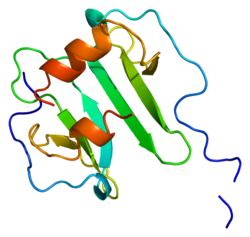
Состав
Ген
Ген CXCL12 расположен на 10-й хромосоме в полосе 10q11.1 и содержит 9 экзонов . Этот ген продуцирует 7 изоформ посредством альтернативного сплайсинга .
Протеин
Этот белок принадлежит к семейству интеркринных альфа ( хемокинов CXC). SDF-1 продуцируется в двух формах, SDF-1α / CXCL12a и SDF-1β / CXCL12b, путем попеременного сплайсинга одного и того же гена. Хемокины характеризуются наличием четырех консервативных цистеинов , которые образуют две дисульфидные связи . Белки CXCL12 принадлежат к группе хемокинов CXC, чья начальная пара цистеинов разделена одной промежуточной аминокислотой . Кроме того, первые 8 остатков N-конца CXCL12 служат сайтом связывания рецептора , хотя только Lys-1 и Pro-2 непосредственно участвуют в активации рецептора. Между тем, мотив RFFESH (остатки 12-17) в области петли функционирует как стыковочный сайт для связывания рецептора CXCL12.
Функция
CXCL12 экспрессируется во многих тканях мышей, включая мозг , тимус , сердце , легкие , печень , почки , селезенку и костный мозг . CXCL12 оказывает сильное хемотаксическое действие на лимфоциты . Во время эмбриогенеза он направляет миграцию кроветворных клеток из печени плода в костный мозг и образование крупных кровеносных сосудов. Также было показано, что передача сигналов CXCL12 регулирует экспрессию CD20 на В-клетках. CXCL12 также является хемотаксиком для мезенхимальных стволовых клеток и экспрессируется в области воспалительной деструкции кости, где опосредует их подавляющее действие на остеокластогенез .
Во взрослом возрасте CXCL12 играет важную роль в ангиогенезе , рекрутируя эндотелиальные клетки-предшественники (EPCs) из костного мозга посредством механизма, зависимого от CXCR4.
CXCR4 , ранее называвшийся LESTR или фузин, является рецептором для CXCL12. Это взаимодействие CXCL12-CXCR4 раньше считалось исключительным (в отличие от других хемокинов и их рецепторов), но недавно было высказано предположение, что CXCL12 может также связываться с рецептором CXCR7 (теперь называемым ACKR3). Блокируя CXCR4, главный корецептор для проникновения ВИЧ-1, CXCL12 действует как эндогенный ингибитор CXCR4-тропных штаммов ВИЧ-1.
ЦНС
Во время эмбрионального развития CXCL12 играет роль в формировании мозжечка посредством миграции нейронов. В ЦНС CXCL12 способствует пролиферации клеток, нейрогенезу (развитию и росту нервной ткани), а также нейровоспалению. Клетки-предшественники нейронов (NPC) - это стволовые клетки, которые дифференцируются в глиальные и нейрональные клетки. CXCL12 способствует их миграции к участкам поражения в головном мозге, особенно в обширных диапазонах. Оказавшись в месте повреждения, NPC могут начать восстановление ткани на основе стволовых клеток. Ось CXCL12 / CXCR4 обеспечивает ориентиры для аксонов и нейритов, тем самым способствуя разрастанию нейритов (нейроны, образующие выступы) и нейрогенезу. Как и другие хемокины, CXCL12 участвует в миграции клеток, что способствует воспалению. Что касается ЦНС, CXCL12 играет роль в нейровоспалении, привлекая лейкоциты через гематоэнцефалический барьер. однако чрезмерное производство и накопление CXCL12 может стать токсичным, а вызванное воспаление может привести к серьезным последствиям.
Клиническое значение
У людей CXCL12 вовлечен в широкий спектр биомедицинских состояний, вовлекающих несколько систем органов. Более того, передача сигналов CXCL12 в сочетании с передачей сигналов CXCR7 участвует в прогрессировании рака поджелудочной железы. В системе мочевыводящих путей метилирование промотора CXCL12 и экспрессия PD-L1 могут быть мощными прогностическими биомаркерами биохимического рецидива у пациентов с карциномой простаты после радикальной простатэктомии, и продолжаются дальнейшие исследования, чтобы подтвердить, может ли метилирование CXCL12 помочь в стратегиях активного наблюдения. В области онкологии фибробласты, ассоциированные с меланомой, стимулируются стимуляцией аденозинового рецептора A2B с последующей стимуляцией фактора роста фибробластов и повышенной экспрессией CXCL12.
Клинический маркер
Мультилокусное исследование генетической шкалы риска, основанное на комбинации 27 локусов, включая ген CXCL12, выявило лиц с повышенным риском как эпизодов, так и рецидивов ИБС, а также усиление клинической пользы от терапии статинами. Исследование было основано на когортном исследовании сообщества (исследование Malmo Diet and Cancer) и четырех дополнительных рандомизированных контролируемых исследованиях когорт первичной профилактики (JUPITER и ASCOT) и когорт вторичной профилактики (CARE и PROVE IT-TIMI 22).
Рассеянный склероз
Неврологическое заболевание, возникающее в результате неправильного взаимодействия иммунной и нервной систем при рассеянном склерозе . РС характеризуется демиелинизацией нервов из-за того, что иммунная система организма атакует ЦНС. Повышенные уровни CXCL12 наблюдаются в спинномозговой жидкости пациентов с рассеянным склерозом. CXCL12 проникает через гематоэнцефалический барьер и вызывает нейровоспаление, которое способствует повреждению аксонов и, следовательно, прогрессированию рассеянного склероза.
Болезнь Альцгеймера
Хотя CXCL12 может быть вредным для людей с рассеянным склерозом, недавние исследования показывают, что этот хемокин может быть полезным для уменьшения прогрессирования пациентов с болезнью Альцгеймера. Болезнь Альцгеймера - еще одно неврологическое заболевание и наиболее распространенная форма деменции, при которой когнитивные способности значительно ухудшаются. Одной из основных характеристик болезни Альцгеймера является накопление бляшки в головном мозге, известной как бета-амилоид. Нейрозащитные аспекты CXCL12 у мышей с этими бляшками / болезнью Альцгеймера. PAK - это белок, связанный с поддержанием дендритных шипов, которые необходимы в синапсах для получения информации от аксонов. Неверная локализация PAK происходит у пациентов с болезнью Альцгеймера, однако предварительная обработка нейронов мышей CXCL12 показала подавление этой неправильной локализации. Кроме того, эта предварительная обработка CXCL уменьшала распространенность апоптоза и окислительного повреждения, обычно вызываемого присутствием бета-амилоидных бляшек.
Как мишень для наркотиков
Хемокины и рецепторы хемокинов, из которых выделяется CXCR, регулируют множество процессов, таких как морфогенез, ангиогенез и иммунные ответы, и считаются потенциальными мишенями для разработки лекарств. В системе желудочно-кишечного тракта ось CXCL12-CXCR4 исследуется в качестве противофиброзной терапии при лечении хронического панкреатита. Например, блокирование CXCR4 , рецептора для CXCL12, с помощью Plerixafor (AMD-3100) увеличивало эффективность комбретастатина на мышиной модели рака груди, предположительно за счет предотвращения рекрутирования макрофагов в опухоли. [15] [16] AMD-3100 также широко используется в комбинации с G-CSF для мобилизации гемопоэтических стволовых клеток в кровоток, что позволяет собирать их для трансплантации костного мозга .
использованная литература
дальнейшее чтение
- Куча М., Река Р., Миекус К., Ванцек Дж., Вояковски В., Яновска-Вечорек А., Ратайчак Дж., Ратайчак М.З. (август 2005 г.). «Торговля нормальными стволовыми клетками и метастазирование раковых стволовых клеток включает сходные механизмы: центральная роль оси SDF-1-CXCR4» . Стволовые клетки . 23 (7): 879–94. DOI : 10.1634 / стволовые клетки.2004-0342 . PMID 15888687 . S2CID 22504846 .
- Kryczek I, Wei S, Keller E, Liu R, Zou W. (март 2007 г.). «Фактор стромы (SDF-1 / CXCL12) и патогенез опухолей человека» . Американский журнал физиологии. Клеточная физиология . 292 (3): C987–95. DOI : 10,1152 / ajpcell.00406.2006 . PMID 16943240 . S2CID 7423893 .
- Стеллос К., Гаваз М. (март 2007 г.). «Тромбоциты и фактор-1, производный от стромальных клеток, в рекрутинге клеток-предшественников». Семинары по тромбозу и гемостазу . 33 (2): 159–64. DOI : 10,1055 / с-2007-969029 . PMID 17340464 .
- Ван Дж, Лю Х, Лу Х, Цзян Ц., Цуй Х, Ю Л, Фу Х, Ли Кью, Ван Дж (март 2015 г.). «Субпопуляция CXCR4 (+) CD45 (-) BMMNC превосходит нефракционированные BMMNC по защите после ишемического инсульта у мышей» . Мозг, поведение и иммунитет . 45 : 98–108. DOI : 10.1016 / j.bbi.2014.12.015 . PMC 4342301 . PMID 25526817 .
- Арья М., Ахмед Х., Силхи Н., Уильямсон М., Пател Х.Р. (2007). «Клиническое значение и терапевтические последствия основного взаимодействия CXCL12-CXCR4 (хемокиновый лиганд-рецептор) в миграции раковых клеток». Биология опухоли . 28 (3): 123–31. DOI : 10.1159 / 000102979 . PMID 17510563 . S2CID 44356923 .