Ценность - A value

A-значения - это числовые значения, используемые для определения наиболее стабильной ориентации атомов в молекуле ( конформационный анализ ), а также для общего представления стерического объема . A-значения получены из измерений энергии различных циклогексановых конформаций монозамещенного циклогексанового химического вещества. Заместители в циклогексановом кольце предпочитают находиться в экваториальном положении, а не в осевом. Разница в свободной энергии Гиббса (ΔG) между конформацией с более высокой энергией (осевое замещение) и конформацией с более низкой энергией (экваториальное замещение) является значением A для этого конкретного заместителя.
Полезность
А-значения помогают предсказать конформацию циклогексановых колец. Наиболее стабильной будет конформация, в которой заместитель или заместители экваториальны. Когда принимают во внимание несколько заместителей, предпочтительна конформация, в которой заместитель с наибольшим значением A является экваториальным.
Полезность значений A может быть обобщена для использования вне конформаций циклогексана. A-значения могут помочь предсказать стерический эффект заместителя. В общем, чем больше значение A заместителя, тем больше стерический эффект этого заместителя. Метильная группа имеет A-значение 1,74 в то время как трет - бутильна группа имеет A-значение \ 5. Поскольку значение А трет- бутила выше, трет- бутил имеет больший стерический эффект, чем метил. Это различие в стерических эффектах можно использовать для предсказания реакционной способности в химических реакциях.
Соображения о бесплатной энергии
Стерические эффекты играют главную роль в назначении конфигураций циклогексанов. Можно использовать стерические препятствия для определения склонности заместителя находиться в аксиальной или экваториальной плоскости. Известно, что осевые связи более затруднены, чем соответствующие экваториальные связи. Это связано с тем, что заместители в аксиальном положении относительно близки к двум другим осевым заместителям. Это делает его очень тесным, когда объемные заместители ориентированы в осевом положении. Эти типы стерических взаимодействий широко известны как 1,3-диаксиальные взаимодействия . Эти типы взаимодействий отсутствуют с заместителями в экваториальном положении.
Обычно рассматриваются три основных вклада в конформационную свободную энергию :
- Деформация Байера , определяемая как деформация, возникающая в результате деформации валентных углов.
- Деформация Питцера , определяемая как деформация кручения, возникающая в результате 1,2-взаимодействий между группами, присоединенными к смежным атомам углерода,
- Ван-дер-Ваальсовы взаимодействия , подобные 1,3-диаксиальным взаимодействиям.
Энтальпические компоненты
При сравнении относительной стабильности 6- и 7-атомные взаимодействия могут использоваться для аппроксимации различий в энтальпии между конформациями. Каждое 6-атомное взаимодействие стоит 0,9 ккал / моль (3,8 кДж / моль), а каждое 7-атомное взаимодействие стоит 4 ккал / моль (17 кДж / моль).
Энтропические компоненты
Энтропия также играет роль в предпочтении заместителем экваториального положения. Энтропийная составляющая определяется по следующей формуле:
Где σ равно количеству микросостояний, доступных для каждой конформации.
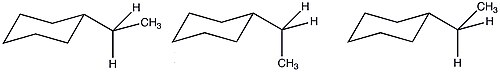
Из-за большего числа возможных конформаций этилциклогексана значение A уменьшается по сравнению с тем, что можно было бы спрогнозировать исключительно на основе энтальпии. Благодаря этим благоприятным энтропийным условиям стерическая значимость этильной группы аналогична значимости метильного заместителя.
Таблица A-значений
| Заместитель | Ценность | Заместитель | Ценность | Заместитель | Ценность | ||
|---|---|---|---|---|---|---|---|
| D | 0,006 | CH 2 Br | 1,79 | OSi (CH 3 ) 3 | 0,74 | ||
| F | 0,15 | CH (CH 3 ) 2 | 2,15 | ОЙ | 0,87 | ||
| Cl | 0,43 | куб.см 6 H 11 | 2,15 | ОСН 3 | 0,6 | ||
| Br | 0,38 | С (СН 3 ) 3 | > 4 | ОКР 3 | 0,56 | ||
| я | 0,43 | Ph | 3 | ОСН 2 СН 3 | 0,9 | ||
| CN | 0,17 | CO 2 H | 1,35 | O-Ac | 0,6 | ||
| NC | 0,21 | CO 2 - | 1,92 | O-TFA | 0,68 | ||
| Унтер-офицер | 0,51 | CO 2 CH 3 | 1,27 | OCHO | 0,27 | ||
| NCS | 0,28 | CO 2 Et | 1.2 | О-Ц | 0,5 | ||
| N = C = NR | 1 | CO 2 i Pr | 0,96 | ONO 2 | 0,59 | ||
| CH 3 | 1,7 | COCl | 1,25 | NH 2 | 1.6 | ||
| CF 3 | 2.1 | COCH 3 | 1.17 | NHCH 3 | 1 | ||
| Канал 2 Кан 3 | 1,75 | SH | 0,9 | N (CH 3 ) 2 | 2.1 | ||
| CH = CH 2 | 1,35 | SMe | 0,7 | NH 3 + | 1.9 | ||
| CCH | 0,41 | SPh | 0,8 | НЕТ 2 | 1.1 | ||
| CH 2 т Bu | 2 | S - | 1.3 | HgBr | ~ 0 | ||
| CH 2 OTs | 1,75 | СОФ | 1.9 | HgCl | 0,3 | ||
| SO 2 Ph | 2,5 | Si (CH 3 ) 3 | 2,5 |
Приложения
Прогнозирование реактивности
Один из оригинальных экспериментов, проведенных Уинстоном и Холнессом, заключался в измерении скорости окисления в транс- и цис-замещенных кольцах с использованием хромового катализатора. Используемая большая трет- бутильная группа фиксирует конформацию каждой молекулы, размещая ее экваториально (показано цис-соединение).
Было обнаружено, что цис-соединение подвергалось окислению с гораздо большей скоростью, чем транс-соединение. Предполагалось, что большая гидроксильная группа в аксиальном положении является неблагоприятной и образует карбонил с большей готовностью для снятия этого напряжения. Скорость транс-соединения идентична скорости, обнаруженной в монозамещенном циклогексаноле.
Приблизительное значение силы внутримолекулярной силы с использованием значений A
Используя значения A гидроксильной и изопропильной субъединиц, можно рассчитать энергетическое значение благоприятной внутримолекулярной водородной связи.
Ограничения
A-значения измеряются с использованием монозамещенного циклогексанового кольца и являются показателем только стерических свойств, которые конкретный заместитель придает молекуле. Это приводит к проблеме, когда есть возможные стабилизирующие электронные факторы в другой системе. Кислоты карбоновый заместитель , показанный ниже , аксиален в основном состоянии, несмотря на положительное A-Value. Из этого наблюдения ясно, что существуют и другие возможные электронные взаимодействия, которые стабилизируют осевую конформацию.
Прочие соображения
Важно отметить, что A-значения не предсказывают физический размер молекулы, а только стерический эффект. Например, трет- бутильная группа (значение A = 4,9) имеет большее значение A, чем триметилсилильная группа (значение A = 2,5), однако на самом деле трет- бутильная группа занимает меньше места. Это различие может быть связано с более длинной длины углерод-кремний связи по сравнению с углерод-углеродной связи в трет группы бутиловым. Более длинная связь позволяет меньше взаимодействовать с соседними заместителями, что эффективно делает триметилсилильную группу менее стерически затруднительной, таким образом, понижая ее A-значение. Это также можно увидеть при сравнении галогенов . Бром, йод и хлор имеют одинаковые значения A, хотя их атомные радиусы различаются. Значения A затем предсказывают кажущийся размер заместителя, а относительные кажущиеся размеры определяют различия в стерических эффектах между соединениями. Таким образом, значения A являются полезными инструментами для определения реакционной способности соединения в химических реакциях.