Триметилалюминий - Trimethylaluminium
|
|
|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Триметилалуман
|
|
| Другие имена
Триметилалюминий; триметил алюминия; триметил алюминия
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.000.776 |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
| Характеристики | |
| C 6 H 18 Al 2 | |
| Молярная масса | 144,17 г / моль 72,09 г / моль (C 3 H 9 Al) |
| Появление | Бесцветная жидкость |
| Плотность | 0,752 г / см 3 |
| Температура плавления | 15 ° С (59 ° F, 288 К) |
| Точка кипения | 125–130 ° C (257–266 ° F, 398–403 К) |
| Реагирует | |
| Давление газа | |
| Вязкость | |
| Термохимия | |
|
Теплоемкость ( C )
|
155,6 Дж / моль · К |
|
Стандартная мольная
энтропия ( S |
209,4 Дж / моль · К |
|
Std энтальпия
формации (Δ F H ⦵ 298 ) |
-136,4 кДж / моль |
|
Свободная энергия Гиббса (Δ f G ˚)
|
-9,9 кДж / моль |
| Опасности | |
| Основные опасности | Пирофорный |
| Пиктограммы GHS |
 
|
| Сигнальное слово GHS | Опасность |
| H250 , H260 , H314 | |
| P222 , P223 , P231 + 232 , P280 , P370 + 378 , P422 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | -17,0 ° С (1,4 ° F, 256,1 К) |
| Родственные соединения | |
|
Родственные соединения
|
Триэтилалюминий |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
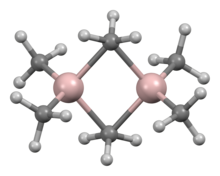
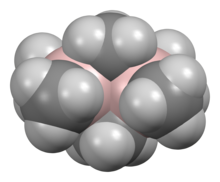
Триметилалюминий - один из простейших примеров алюмоорганического соединения. Несмотря на свое название, он имеет формулу Al 2 ( CH 3 ) 6 (сокращенно Al 2 Me 6 или TMA), поскольку он существует в виде димера . Эта бесцветная жидкость пирофорна . Это промышленно важное соединение, тесно связанное с триэтилалюминием .
Структура и склеивание
Структура и связи в Al 2 R 6 и диборане аналогичны (R = алкил). В Al 2 Me 6 расстояния Al-C (терминал) и Al-C (мостик) составляют 1,97 и 2,14 Å соответственно. Центр Al четырехгранный. Каждый атом углерода мостиковой метильной группы окружен пятью соседями: тремя атомами водорода и двумя атомами алюминия. Метильные группы легко меняются внутримолекулярно. При более высоких температурах, димер трещин в мономерной AlMe 3 .
Синтез
АПМ готовится с помощью двухэтапного процесса, который можно резюмировать следующим образом:
- 2 Al + 6 CH 3 Cl + 6 Na → Al 2 (CH 3 ) 6 + 6 NaCl
Приложения
Катализ
Начиная с изобретения катализатора Циглера-Натта , алюминийорганические соединения играют важную роль в производстве полиолефинов , таких как полиэтилен и полипропилен . Метилалюмоксан , производимый из ТМА, является активатором многих катализаторов на основе переходных металлов.
Полупроводниковые приложения
ТМА также используется в производстве полупроводников для осаждения тонких пленок диэлектриков с высоким k, таких как Al 2 O 3, посредством процессов химического осаждения из паровой фазы или осаждения атомных слоев . ТМА является предпочтительным прекурсором для металлоорганической парофазной эпитаксии ( MOVPE ) алюминийсодержащих полупроводниковых соединений , таких как AlAs , AlN , AlP , AlSb , AlGaAs , AlInGaAs , AlInGaP , AlGaN , AlInGaN , AlInGaNP и т. Д. (а) элементарные примеси, (б) кислородсодержащие и органические примеси.
Фотоэлектрические приложения
В процессах осаждения, очень похожих на обработку полупроводников, ТМА используется для осаждения пакетов тонких пленок с низким k (непоглощающих) диэлектрических слоев с Al 2 O 3 посредством процессов химического осаждения из паровой фазы или осаждения атомных слоев . Al 2 O 3 обеспечивает отличную пассивацию поверхностей кремния, легированного p-примесью. Слой Al 2 O 3 обычно представляет собой нижний слой с несколькими слоями нитрида кремния (Si x N y ) для покрытия.
Реакции
Триметилалюминий легко и даже опасно гидролизуется:
- AlMe 3 + 1,5 H 2 O → 0,5 Al 2 O 3 + 3 CH 4
В контролируемых условиях реакцию можно остановить с получением метилалюмоксана:
- AlMe 3 + H 2 O → 1 / n [AlMeO] n + 2 CH 4
Аналогично протекают реакции алкоголиза и аминолиза. Например, диметиламин дает димер диамида диалюминия:
- 2 AlMe 3 + 2 HNMe 2 → [AlMe 2 NMe 2 ] 2 + 2 CH 4
Реакции с хлоридами металлов
ТМА реагирует со многими галогенидами металлов с образованием алкильных групп. В сочетании с трихлоридом галлия дает триметилгаллий . Al 2 Me 6 реагирует с трихлоридом алюминия с образованием (AlMe 2 Cl) 2 .
Реакции ТМА / галогенидов металлов появились как реагенты в органическом синтезе . Реагент Теббе , который используется для метиленирования сложных эфиров и кетонов , получают из ТМА и дихлорида титаноцена . В сочетании с 20-100 мол.% Cp 2 ZrCl 2 ( дихлорид цирконоцена ), (CH 3 ) 2 Al-CH 3 добавляет «поперечные» алкины с образованием форм винилалюминия , которые используются в органическом синтезе в реакции, известной как карбоалюминирование.
Аддукты
Что касается других «электронно-дефицитных соединений», триметилалюминий дает аддукты R 3 N . AlMe 3 . Кислотные свойства Льюиса AlMe 3 были определены количественно. Данные по энтальпии показывают, что AlMe 3 является твердой кислотой, и его кислотные параметры в модели ECW равны E A = 8,66 и C A = 3,68.
Эти аддукты, например комплекс с третичным амином DABCO , более безопасны в обращении, чем сам ТМА.
Миссия НАСА ATREX ( Эксперимент с аномальной транспортной ракетой ) использовала белый дым, который ТМА образует при контакте с воздухом, для изучения высотного реактивного потока.
Синтетический реагент
ТМА является источником метилнуклеофилов, подобных метиллитию , но менее реакционноспособным. Он реагирует с кетонами, давая после гидролитической обработки третичные спирты.
Безопасность
Триметилалюминий пирофорен, бурно реагирует с воздухом и водой.

