Триэтилалюминий - Triethylaluminium

|
|
|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Триэтилалуман
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| Сокращения | ЧАЙ, ЧАЙ, ЧАЙ |
| ChemSpider | |
| ECHA InfoCard |
100,002,382 |
| Номер ЕС | |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
| Характеристики | |
| C 12 H 30 Al 2 | |
| Молярная масса | 228,335 г · моль -1 |
| Появление | Бесцветная жидкость |
| Плотность | 0,8324 г / мл при 25 ° C |
| Температура плавления | -46 ° С (-51 ° F, 227 К) |
| Точка кипения | От 128 до 130 ° C (от 262 до 266 ° F, от 401 до 403 K) при 50 мм рт. |
| Опасности | |
| Основные опасности | пирофорный |
| R-фразы (устаревшие) | R14 R17 R34 |
| S-фразы (устаревшие) | S16 S43 S45 |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | -18 ° С (0 ° F, 255 К) |
| Родственные соединения | |
|
Родственные соединения
|
Триметилалюминий |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Триэтилалюминий - один из простейших примеров алюмоорганического соединения. Несмотря на свое название, он имеет формулу Al 2 ( C 2 H 5 ) 6 (сокращенно Al 2 Et 6 или TEA), поскольку он существует в виде димера . Эта бесцветная жидкость пирофорна . Это промышленно важное соединение, тесно связанное с триметилалюмием .
Структура и склеивание
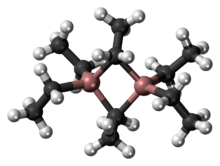
Структура и связи в Al 2 R 6 и диборане аналогичны (R = алкил). Что касается Al 2 Me 6 , то расстояния Al-C (терминал) и Al-C (мостик) составляют 1,97 и 2,14 Å соответственно. Центр Al четырехгранный. Каждый атом углерода мостиковой этильной группы окружен пятью соседями: углеродом, двумя атомами водорода и двумя атомами алюминия. Этильные группы легко меняются внутримолекулярно. При более высоких температурах, димер трещин в мономерный AlEt 3 .
Синтез и реакции
Триэтилалюминий может быть образован несколькими путями. Открытие эффективного маршрута было значительным технологическим достижением. В многоступенчатом процессе используются металлический алюминий, газообразный водород и этилен , кратко изложенные ниже:
- 2 Al + 3 H 2 + 6 C 2 H 4 → Al 2 Et 6
Благодаря такому эффективному синтезу триэтилалюминий является одним из наиболее доступных алюминийорганических соединений.
Триэтилалюминий также может быть получен из полуторного хлорида этилалюминия (Al 2 Cl 3 Et 3 ), который образуется при обработке алюминиевого порошка хлорэтаном . Восстановление полуторного хлорида этилалюминия щелочным металлом, таким как натрий, дает триэтилалюминий:
- 3 Al 2 Cl 3 Et 3 + 9 Na → 2 Al 2 Et 6 + 2 Al + 9 NaCl
Реактивность
Связи Al – C триэтилалюминия поляризованы до такой степени, что углерод легко протонируется с выделением этана:
- Al 2 Et 6 + 6 HX → 2 AlX 3 + 6 EtH
Для этой реакции можно использовать даже слабые кислоты, такие как концевые ацетилены и спирты.
Связь между парой алюминиевых центров относительно слабая и может быть расщеплена основаниями Льюиса (L) с образованием аддуктов с формулой AlEt 3 L:
- Al 2 Et 6 + 2 L → 2 LAlEt 3
Приложения
Предшественники жирных спиртов
Триэтилалюминий используется в промышленности в качестве промежуточного продукта при производстве жирных спиртов , которые превращаются в детергенты . Первый этап включает олигомеризацию этилена по реакции Ауфбау , которая дает смесь соединений триалкилалюминия (здесь упрощенно - октильные группы):
- Al 2 (C 2 H 5 ) 6 + 18 C 2 H 4 → Al 2 (C 8 H 17 ) 6
Впоследствии эти триалкильные соединения окисляются до алкоксидов алюминия , которые затем гидролизуются:
- Al 2 (C 8 H 17 ) 6 + 3 O 2 → Al 2 (OC 8 H 17 ) 6
- Al 2 (OC 8 H 17 ) 6 + 6 H 2 O → 6 C 8 H 17 OH + 2 "Al (OH) 3 "
Сокатализаторы полимеризации олефинов
В катализе Циглера-Натта используется большое количество TEAL и родственных алкилалюминия . Они служат для активации катализатора на основе переходного металла как в качестве восстанавливающего агента, так и в качестве алкилирующего агента . TEAL также предназначен для удаления воды и кислорода.
Реагент в органической и металлоорганической химии
Триэтилалюминий имеет нишевое использование в качестве предшественника других алюминийорганических соединений, таких как цианид диэтилалюминия :
Пирофорный агент
Триэтилалюминий воспламеняется при контакте с воздухом и воспламеняется и / или разлагается при контакте с водой и с любым другим окислителем - это одно из немногих веществ, обладающих достаточной пирофорностью, чтобы воспламениться при контакте с криогенным жидким кислородом . Энтальпия сгорания , Δ с H °, составляет -5105,70 ± 2,90 к Дж / моль (-22,36 кДж / г ). Его легкое зажигание делает его особенно востребованным в качестве воспламенителя ракетного двигателя . SpaceX 9 Фалькон ракета использует triethylaluminium- триэтилбораном смеси в качестве первой ступени воспламенитель.
Триэтилалюминий утолщен с полиизобутиленом используются в качестве зажигательного оружия , в качестве альтернативы пирофорном напалма ; например, в обойме M74 с четырьмя ракетами для пусковых установок M202A1 . В этом приложении он известен как TPA, загущенный пиротехнический агент или загущенный пирофорный агент . Обычное количество загустителя - 6%. Количество загустителя может быть уменьшено до 1%, если добавлены другие разбавители. Например, н-гексан можно использовать с повышенной безопасностью, делая соединение непирофорным до тех пор, пока разбавитель не испарится, после чего объединенный огненный шар образуется как из паров триэтилалюминия, так и из паров гексана. M202 был выведен из эксплуатации в середине 1980-х годов из-за проблем с безопасностью, транспортировкой и хранением. Некоторые видели ограниченное использование в войне в Афганистане против пещер и укрепленных соединений.
Смотрите также
- Триэтилборан , используемый в качестве воспламенителя в турбореактивных / прямоточных двигателях Pratt & Whitney J58 .
- Триметилалюминий


![{\ displaystyle {\ ce {{1 / 2Al2Et6} + HCN ->}} \ {\ tfrac {1} {n}} {\ ce {[Et2AlCN]}} _ {n} + {\ ce {C2H6}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/b73bebe835386dae4e699b7a9b65a76a0f6853f3)