Тетраэдрическое карбонильное аддитивное соединение - Tetrahedral carbonyl addition compound
Тетраэдрической промежуточного является промежуточным продуктом реакции , в которой расположение связей вокруг первоначально двойной связью атома углерода был преобразован из тригональной к тетраэдрической. Тетраэдрические промежуточные продукты образуются в результате нуклеофильного присоединения к карбонильной группе. Стабильность тетраэдрического промежуточного соединения зависит от способности групп, присоединенных к новому тетраэдрическому атому углерода, уходить с отрицательным зарядом. Тетраэдрические промежуточные соединения очень важны в органических синтезах и биологических системах в качестве ключевого промежуточного продукта при этерификации , переэтерификации , гидролизе сложного эфира, образовании и гидролизе амидов и пептидов , восстановлении гидридов и других химических реакциях.
История
Одно из первых сообщений о тетраэдрическом промежуточном соединении было сделано Райнером Людвигом Клайзеном в 1887 году. В реакции бензилбензоата с метоксидом натрия и метилбензоата с бензилоксидом натрия он наблюдал белый осадок, который в кислых условиях дает бензилбензоат, метилбензоат, метанол и бензиловый спирт. Он назвал вероятный общий промежуточный продукт «additionalelle Verbindung».
Виктор Гриньяр предположил существование нестабильного тетраэдрического промежуточного соединения в 1901 году, исследуя реакцию сложных эфиров с магнийорганическими реагентами.
Первое свидетельство существования тетраэдрических промежуточных соединений в реакциях замещения производных карбоновых кислот было предоставлено Майроном Л. Бендером в 1951 году. Он меченел производные карбоновой кислоты изотопом кислорода O18 и реагировал на эти производные с водой с образованием меченых карбоновых кислот. В конце реакции он обнаружил, что оставшийся исходный материал имел пониженную долю меченого кислорода, что согласуется с существованием тетраэдрического промежуточного соединения.
Механизм реакции
Нуклеофильная атака на карбонильную группу происходит по траектории Бюрги-Дуница . Угол между линией нуклеофильной атаки и связью CO больше 90 ° из-за лучшего перекрытия орбиталей между HOMO нуклеофила и π * LUMO двойной связи CO.
Структура тетраэдрических интермедиатов
Общие особенности
Хотя тетраэдрические интермедиаты обычно являются переходными интермедиатами, многие соединения этой общей структуры известны. Реакции альдегидов, кетонов и их производных часто имеют обнаруживаемый тетраэдрический промежуточный продукт, в то время как для реакций производных карбоновых кислот это не так. На уровне окисления производных карбоновой кислоты такие группы, как OR, OAr, NR 2 или Cl, сопряжены с карбонильной группой, что означает, что добавление к карбонильной группе термодинамически менее благоприятно, чем добавление к соответствующему альдегиду или кетону. Стабильные тетраэдрические промежуточные соединения производных карбоновой кислоты действительно существуют, и они обычно обладают по крайней мере одной из следующих четырех структурных особенностей:
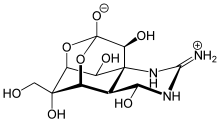
- полициклические структуры (например, тетродотоксин )
- соединения с сильной электроноакцепторной группой, присоединенной к ацильному углероду (например, N , N- диметилтрифторацетамид)
- соединения с донорными группами, которые плохо конъюгированы с потенциальной карбонильной группой (например, циклол )
- соединения с атомами серы, связанными с аномерным центром (например, S-ацилированный-1,8-нафталиндитиол)
Эти соединения использовали для изучения кинетики разложения тетраэдрического промежуточного соединения на соответствующие карбонильные соединения и для измерения ИК-, УФ- и ЯМР-спектров тетраэдрического аддукта.
Рентгеновское определение кристаллической структуры
Первые рентгеновские кристаллические структуры тетраэдрических промежуточных соединений были получены в 1973 году из бычьего трипсина, кристаллизованного с помощью ингибитора бычьего панкреатического трипсина, а в 1974 году из свиного трипсина, кристаллизованного с помощью ингибитора трипсина сои. В обоих случаях тетраэдрический интермедиат стабилизируется в активных центрах ферментов, которые эволюционировали для стабилизации переходного состояния пептидного гидролиза.
Некоторое представление о структуре тетраэдрического промежуточного соединения можно получить из кристаллической структуры N -брозилмитомицина A, кристаллизованного в 1967 году. Тетраэдрический углерод C17 образует связь 136,54 мкм с O3, которая короче связи C8-O3 (142,31 мкм). Напротив, связь C17-N2 (149,06 пм) длиннее, чем связь N1-C1 (148,75 пм) и связь N1-C11 (147,85 пм) из-за пожертвования неподеленной пары O3 на σ * орбиталь C17-N2. Эта модель, однако, находится в тетрациклическом скелете, а тетраэдрический O3 метилирован, что в целом делает ее плохой моделью.
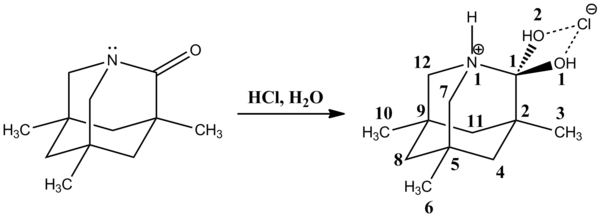
Более поздняя рентгеновская кристаллическая структура 1-аза-3,5,7-триметиладамантан-2-она является хорошей моделью для катионного тетраэдрического промежуточного соединения. Связь C1-N1 довольно длинная [155,2 (4) пм], а связи C1-O1 (2) укорачиваются [138,2 (4) пм]. Протонированный атом азота N1 представляет собой отличную уходящую аминогруппу.
В 2002 году Дэвид Эванс и др. наблюдали очень стабильный нейтральный тетраэдрический промежуточный продукт в реакции N- ацилпирролов с металлоорганическими соединениями с последующим протонированием хлоридом аммония с образованием карбинола. Связь C1-N1 [147,84 (14) пм] длиннее, чем обычная связь пиррола C sp3 -N, которая находится в диапазоне 141,2-145,8 пм. Напротив, связь C1-O1 [141,15 (13) мкм] короче, чем средняя связь C sp3 -OH, которая составляет около 143,2 мкм. Удлиненные связи C1-N1 и укороченные связи C1-O1 объясняются аномерным эффектом, возникающим в результате взаимодействия неподеленных пар кислорода с орбиталью σ * CN . Точно так же взаимодействие неподеленной пары кислорода с σ * CC- орбиталью должно быть ответственным за удлинение связи C1-C2 [152,75 (15) пм] по сравнению со средними связями C sp2 -C sp2, которые составляют 151,3 пм. Кроме того, связь C1-C11 [152,16 (17) пм] немного короче, чем средняя связь C sp3 -C sp3, которая составляет около 153,0 пм.
Стабильность тетраэдрических интермедиатов
Ацетали и полуацетали
Гемиацетали и ацетали представляют собой тетраэдрические промежуточные соединения. Они образуются, когда нуклеофилы присоединяются к карбонильной группе, но в отличие от тетраэдрических промежуточных соединений они могут быть очень стабильными и использоваться в качестве защитных групп в синтетической химии. Очень хорошо известная реакция происходит, когда ацетальдегид растворяется в метаноле, образуя полуацеталь. Большинство полуацеталей нестабильны по отношению к своим родительским альдегидам и спиртам. Например, константа равновесия для реакции ацетальдегида с простыми спиртами составляет около 0,5, где константа равновесия определяется как K = [гемиацеталь] / [альдегид] [спирт]. Гемиацетали кетонов (иногда называемые гемикеталами) даже менее стабильны, чем альдегиды. Однако циклические полуацетали и полуацетали, несущие электроноакцепторные группы, стабильны. Электроноакцепторные группы, присоединенные к карбонильному атому, смещают константу равновесия в сторону полуацеталя. Они увеличивают поляризацию карбонильной группы, которая уже имеет положительно поляризованный карбонильный углерод, и делают ее еще более склонной к атаке со стороны нуклеофила. На диаграмме ниже показана степень гидратации некоторых карбонильных соединений. Гексафторацетон , вероятно, является наиболее гидратированным карбонильным соединением. Формальдегид так легко реагирует с водой, потому что его заместители очень малы - чисто стерический эффект.
Циклопропаноны - кетоны с трехчленным кольцом - также в значительной степени гидратированы. Поскольку трехчленные кольца очень напряжены (валентные углы вынуждены составлять 60 °), гибридизация sp 3 более благоприятна, чем гибридизация sp 2 . Для sp 3- гибридизированного гидрата связи должны быть искажены примерно на 49 °, в то время как для sp 2- гибридизированного кетона искажение угла связи составляет примерно 60 °. Таким образом, добавление к карбонильной группе позволяет высвободить часть напряжения, присущего маленькому кольцу, поэтому циклопропанон и циклобутанон являются очень реактивными электрофилами. Для более крупных колец, где валентные углы не так искажены, стабильность полуацеталей обусловлена энтропией и близостью нуклеофила к карбонильной группе. Образование ациклического ацеталя влечет за собой уменьшение энтропии, поскольку на каждую произведенную молекулу расходуются две молекулы. Напротив, образование циклических полуацеталей включает реакцию одной молекулы с самой собой, что делает реакцию более благоприятной. Другой способ понять стабильность циклических полуацеталей - это посмотреть на константу равновесия как на отношение скорости прямой и обратной реакции. Для циклического полуацеталя реакция является внутримолекулярной, поэтому нуклеофил всегда удерживается близко к карбонильной группе, готовой к атаке, поэтому прямая скорость реакции намного выше, чем обратная скорость. Многие биологически релевантные сахара, такие как глюкоза , являются циклическими полуацеталами.
В присутствии кислоты полуацетали могут подвергаться реакции элиминирования, теряя атом кислорода, который когда-то принадлежал карбонильной группе исходного альдегида. Эти ионы оксония являются мощными электрофилами и быстро реагируют со второй молекулой спирта с образованием новых стабильных соединений, называемых ацеталями. Ниже представлен весь механизм образования ацеталя из полуацеталя.
Ацетали, как уже указывалось, являются стабильными тетраэдрическими промежуточными продуктами, поэтому их можно использовать в качестве защитных групп в органическом синтезе. Ацетали стабильны в основных условиях, поэтому их можно использовать для защиты кетонов от основания. Ацетальная группа гидролизуется в кислых условиях. Пример с защитной группой диоксолана приведен ниже.
Амиды Вайнреба
Вайнреб амиды являются N - метокси - N амиды кислот -methylcarboxylic. Амиды Вайнреба реагируют с металлоорганическими соединениями с образованием при протонировании кетонов (см. Синтез кетонов Вайнреба ). Принято считать, что высокие выходы кетонов обусловлены высокой стабильностью хелатированного пятичленного кольцевого промежуточного соединения. Квантово-механические расчеты показали, что тетраэдрический аддукт образуется легко и достаточно устойчив, что согласуется с экспериментальными результатами. Очень легкая реакция амидов Вайнреба с литийорганическим реагентом и реагентами Гриньяра является результатом хелатной стабилизации в тетраэдрическом аддукте и, что более важно, переходного состояния, приводящего к аддукту. Тетраэдрические аддукты показаны ниже.
Приложения в биомедицине
Дизайн лекарств
Сольватированный лиганд, связывающий интересующий белок, вероятно, существует в виде равновесной смеси нескольких конформеров. Подобным образом сольватированный белок также существует в виде нескольких равновесных конформеров. Образование комплекса белок-лиганд включает замещение молекул растворителя, которые занимают сайт связывания лиганда, с образованием сольватированного комплекса. Поскольку это обязательно означает, что взаимодействие является энтропийно неблагоприятным, очень благоприятные энтальпийные контакты между белком и лигандом должны компенсировать энтропийную потерю. Дизайн новых лигандов обычно основан на модификации известных лигандов целевых белков. Протеазы - это ферменты, катализирующие гидролиз пептидной связи. Эти белки эволюционировали, чтобы распознавать и связывать переходное состояние реакции гидролиза пептидов, которое является тетраэдрическим промежуточным соединением. Следовательно, основные ингибиторы протеаз представляют собой тетраэдрические промежуточные имитаторы, содержащие спиртовую или фосфатную группу. Примеры: саквинавир , ритонавир , пепстатин и т. Д.
Ферментативная активность
Стабилизация тетраэдрических промежуточных соединений внутри активного центра фермента была исследована с использованием тетраэдрических промежуточных миметиков. Специфические связывающие силы, участвующие в стабилизации переходного состояния, были описаны кристаллографически. В сериновых протеазах, трипсине и химотрипсине млекопитающих две пептидные NH-группы основной цепи полипептида образуют так называемую оксианионную дыру, отдавая водородные связи отрицательно заряженному атому кислорода тетраэдрического промежуточного соединения. Ниже представлена простая диаграмма, описывающая взаимодействие.