Оксид серебра - Silver oxide
|
|

|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Оксид серебра (I)
|
|
| Другие имена
Серебряная ржавчина, оксид серебра, оксид серебра
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.039.946 |
| Номер ЕС | |
| MeSH | серебро + оксид |
|
PubChem CID
|
|
| Номер RTECS | |
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| Ag 2 O | |
| Молярная масса | 231,735 г · моль -1 |
| Появление | Черные / коричневые кубические кристаллы |
| Запах | Без запаха |
| Плотность | 7,14 г / см 3 |
| Температура плавления | 300 ° C (572 ° F; 573 K) разлагается от ≥200 ° C |
| 0,013 г / л (20 ° C) 0,025 г / л (25 ° C) 0,053 г / л (80 ° C) |
|
|
Произведение растворимости ( K уд. ) AgOH
|
1,52 · 10 -8 (20 ° С) |
| Растворимость | Растворим в кислоте , щелочи Нерастворим в этаноле |
| −134,0 · 10 −6 см 3 / моль | |
| Состав | |
| Кубический | |
| Пн 3 м, 224 | |
| Термохимия | |
|
Теплоемкость ( C )
|
65,9 Дж / моль · К |
|
Стандартная мольная
энтропия ( S |
122 Дж / моль · К |
|
Std энтальпия
формации (Δ F H ⦵ 298 ) |
−31 кДж / моль |
|
Свободная энергия Гиббса (Δ f G ˚)
|
−11,3 кДж / моль |
| Опасности | |
| Пиктограммы GHS |
 
|
| Сигнальное слово GHS | Опасность |
| H272 , H315 , H319 , H335 | |
| P220 , P261 , P305 + 351 + 338 | |
| NFPA 704 (огненный алмаз) | |
| Смертельная доза или концентрация (LD, LC): | |
|
LD 50 ( средняя доза )
|
2,82 г / кг (крысы, перорально) |
| Родственные соединения | |
|
Родственные соединения
|
Оксид серебра (I, III) |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Оксид серебра (I) представляет собой химическое соединение с формулой Ag 2 O. Это мелкий черный или темно-коричневый порошок, который используется для получения других соединений серебра .
Подготовка

Оксид серебра можно получить путем объединения водных растворов нитрата серебра и гидроксида щелочного металла . Эта реакция не дает заметных количеств гидроксида серебра из-за благоприятной энергетики для следующей реакции:
- 2 AgOH → Ag 2 O + H 2 O ( p K = 2,875)
При надлежащим образом контролируемых условиях эту реакцию можно использовать для приготовления порошка Ag 2 O со свойствами, подходящими для нескольких применений, в том числе в качестве мелкозернистого проводящего пастообразного наполнителя.
Структура и свойства
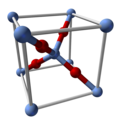
Ag 2 O имеет линейные двухкоординатные центры Ag, связанные тетраэдрическими оксидами. Это изоструктурно с Cu 2 O . Он «растворяется» в растворителях, которые его разлагают. Он слабо растворяется в воде из-за образования иона Ag (OH)-
2и, возможно, родственные продукты гидролиза. Растворим в растворе аммиака , образуя активное соединение реактива Толленса . Суспензия из Ag 2 O легко атакована кислотой :
- Ag 2 O + 2 HX → 2 AgX + H 2 O
где HX = HF , HCl , HBr , HI или CF 3 COOH . Он также будет реагировать с растворами хлоридов щелочных металлов с осаждением хлорида серебра , оставляя раствор соответствующего гидроксида щелочного металла.
Как и многие соединения серебра, оксид серебра светочувствителен. Он также разлагается при температуре выше 280 ° C.
Приложения
Этот оксид используется в батареях из оксида серебра . В органической химии оксид серебра используется как мягкий окислитель . Например, он окисляет альдегиды до карбоновых кислот . Такие реакции часто работают лучше всего, когда оксид серебра получают на месте из нитрата серебра и гидроксида щелочного металла .
использованная литература
внешние ссылки
- Отжиг оксида серебра - Демонстрационный эксперимент: Инструкция и видео

