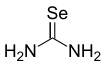
Селеномочевина - Selenourea
|
|
|||
| Идентификаторы | |||
|---|---|---|---|
|
3D модель ( JSmol )
|
|||
| 1734744 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard |
100.010.119 |
||
| Номер ЕС | |||
| 239756 | |||
| MeSH | C081959 | ||
|
PubChem CID
|
|||
| Номер RTECS | |||
| UNII | |||
| Номер ООН | 3283 3077 | ||
|
Панель управления CompTox ( EPA )
|
|||
|
|||
|
|||
| Характеристики | |||
| CH 4 N 2 Se | |||
| Молярная масса | 123,02 г / моль | ||
| Появление | Розовый / серый твердый | ||
| Температура плавления | 200 ° С (392 ° F, 473 К) | ||
| Точка кипения | 214 ° С (417 ° F, 487 К) | ||
| Опасности | |||
| Пиктограммы GHS |
  
|
||
| Сигнальное слово GHS | Опасность | ||
| H301 , H331 , H373 , H400 , H410 | |||
| Р260 , Р261 , Р264 , Р270 , Р271 , Р273 , Р301 + 310 , Р304 + 340 , P311 , P314 , P321 , P330 , P391 , P403 + 233 , Р405 , Р501 | |||
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|||
|
|
|||
| Ссылки на инфобоксы | |||
Селеномочевина представляет собой селенорганическое соединение с формулой SeC (NH 2 ) 2 . Это белое твердое вещество. Это соединение представляет собой редкий пример стабильной, беспрепятственной двойной связи углерод-селен. Соединение используется в синтезе гетероциклов селена . По сравнению с мочевиной , оксо-аналогом селеномочевины, было проведено мало исследований этого соединения из-за нестабильности и токсичности соединений селена . Селеномочевина токсична при вдыхании или употреблении.
Синтез
Соединение было впервые синтезировано в 1884 году Огюстом Вернейем путем реакции селенида водорода и цианамида :
- H 2 Se + NCNH 2 → SeC (NH 2 ) 2
Хотя эта реакция даже нашла применение в промышленном синтезе селеномочевины, более современные методы связаны с синтезом замещенных селеномочевин. Их можно синтезировать с использованием органических изоселеноцианатов и вторичных аминов:
- RN = C = Se + NHR′R ″ → Se = C (NRH) (NR′R ″ H)
В качестве альтернативы можно использовать замещенный карбодиимид следующим образом:
- RN = C = NR ′ Se = C (NRH) (NR'H)
Характеристики
Рентгеновские кристаллографические измерения кристаллов при -100 ° C дают среднюю длину связи C = Se 1,86 Å и 1,37 Å для C-N. Как углы Se-C-N, так и N-C-N были измерены при 120 °, как и ожидалось для sp 2 -гибридизированного углерода. В ходе этих же исследований было подтверждено существование водородных связей Se-H в кристаллической решетке, предположительно из водородных связей O-H и S-H, обнаруженных в кристаллах мочевины и тиомочевины .
Как укороченная длина связи N-C, так и более длинная связь Se = C предполагают делокализацию неподеленной пары на аминах; π-связывающие электроны Se = C тянутся к атому селена, в то время как неподеленная пара азота тянется к карбонильному углероду. Аналогичный эффект наблюдается у мочевины и тиомочевины. При переходе от мочевины к тиомочевине к селеномочевине двойная связь более делокализована и длиннее, в то время как σ-связь C-N более прочная и короче. Что касается резонансных структур , селенольная форма (структуры II, III) более распространена по сравнению с аналогами мочевины и тиомочевины; однако неподеленная пара азот селеномочевины делокализует лишь немного больше, чем неподеленная пара на тиомочевине (в отличие от гораздо большей делокализации при переходе от мочевины к тиомочевине). Эти незначительные различия предполагают, что свойства, возникающие из делокализованной неподеленной пары азота и дестабилизации π-связи C = S и C = Se в тиомочевине и селеномочевине, также будут аналогичными.
В отличие от мочевины и тиомочевины, которые были широко исследованы, относительно небольшое количество исследований количественно характеризует селеномочевину. Хотя было показано, что таутомер селона (I) является более стабильной формой, в основном доступна качественная и сравнительная информация о таутомеризации селеномочевины .
Аналогично кетонам селоны также таутомеризуются:
Поскольку большая делокализация электронов неподеленной пары коррелирует с продуктом селона, положение равновесия селеномочевины, вероятно, имеет положение равновесия, сравнимое с положением тиомочевины (которое находится правее, чем положение мочевины). Было показано , что тиомочевина существует преимущественно в тионовой форме при 42 ° C в разбавленном метаноле , при этом тионоловый таутомер практически отсутствует при нейтральном pH .
Реактивность
Важный класс реакций селеномочевины - образование гетероциклов . Некоторые селенсодержащие гетероциклы проявляют противовоспалительную и противоопухолевую активность, помимо прочего, в медицине. Использование селеномочевины в качестве прекурсора считается наиболее эффективным способом селенсодержащего гетероциклического синтеза.
Другой класс реакций - это комплексообразование селеномочевины с переходными металлами и металлоидами . Его способность действовать как эффективный лиганд объясняется электронодонорным эффектом аминогрупп и последующей стабилизацией π-связи селен-металл . В комплексах селеномочевины наблюдалась только связь селен-металл, в отличие от аналогов мочевины и тиомочевины, которые также связываются через атом азота.