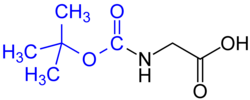
Охраняющая группа - Protecting group

Защитная группа или защитная группа вводит в молекулу путем химической модификацией функциональной группы для получения хемоселективности в последующей химической реакции. Он играет важную роль в многоступенчатом органическом синтезе .
Во многих приготовлениях тонких органических соединений некоторые определенные части их молекул не могут выжить в необходимых реагентах или химической среде. Затем эти части или группы должны быть защищены . Например, алюмогидрид лития является высокореактивным, но полезным реагентом, способным восстанавливать сложные эфиры до спиртов . Он всегда будет реагировать с карбонильными группами, и этого нельзя ни в коем случае препятствовать. Когда требуется восстановление сложного эфира в присутствии карбонила, необходимо предотвратить атаку гидрида карбонила. Например, карбонил превращается в ацеталь , который не реагирует с гидридами. Затем ацеталь называютзащитная группа для карбонила. После завершения стадии с участием гидрида ацеталь удаляют (путем его реакции с водной кислотой), возвращая исходный карбонил. Этот шаг называется снятием защиты .
Защитные группы чаще используются в небольших лабораторных работах и на начальных этапах разработки, чем в процессах промышленного производства, потому что их использование добавляет дополнительные этапы и материальные затраты к процессу. Однако наличие дешевого хирального строительного блока может преодолеть эти дополнительные затраты (например, шикимовая кислота для осельтамивира ).
Общие защитные группы
Алкогольные защитные группы
Защита спиртов :
- Ацетил (Ас) - удаляется кислотой или основанием (см. Ацетоксигруппа ).
- Бензоил (Bz) - удаляется кислотой или основанием, более стабилен, чем группа Ас.
- Бензил (Bn) - удаляется гидрогенолизом . Группа Bn широко используется в химии сахаров и нуклеозидов.
- β-Метоксиэтоксиметиловый эфир (МЕМ) - удаляется кислотой.
- Диметокситритил, [бис- (4-метоксифенил) фенилметил] (DMT) - удаляется слабой кислотой. Группа DMT широко используется для защиты 5'-гидроксигруппы в нуклеозидах, особенно при синтезе олигонуклеотидов .
- Метоксиметиловый эфир (МОМ) - удаляется кислотой.
- Метокситритил [(4-метоксифенил) дифенилметил] (ММТ) - удаляется кислотой и гидрогенолизом.
- п- Метоксибензиловый эфир (PMB) - удаляется кислотой, гидрогенолизом или окислением - обычно с DDQ .
- п- Метоксифениловый эфир (PMP) - удаляется окислением.
- Метилтиометиловый эфир - удаляется кислотой.
- Пивалоил ( Piv ) - удаляется кислотными, щелочными или восстановителями. Он значительно более стабилен, чем другие защитные группы ацила.
- Тетрагидропиранил (THP) - удаляется кислотой.
- Тетрагидрофуран (THF) - удаляется кислотой.
- Тритил (трифенилметил, Tr) - удаляется кислотой и гидрогенолизом.
- Силиловый эфир (к наиболее популярным относятся триметилсилил (ТМС), трет- бутилдиметилсилил (TBDMS или TBS),три- изо -propylsilyloxymethyl (ТОМ) и триизопропилсилил (TIPS) простые эфиры) - Удалены кислотой или фторид - иона. (например, NaF, TBAF ( фторид тетра- н- бутиламмония , HF-Py или HF-NEt 3 )). Группы TBDMS и TOM используются для защиты 2'-гидроксильной функции в нуклеозидах, особенно при синтезе олигонуклеотидов .
- Метиловые эфиры - расщепление осуществляется TMSI в дихлорметане, ацетонитриле или хлороформе. Альтернативный метод расщепления метиловых эфиров - BBr 3 в DCM.
- Этоксиэтиловые эфиры (ЭЭ) - расщепление более тривиально, чем простые эфиры, например 1 н. Соляная кислота.
Защитные группы амина
Защита аминов :
- Карбобензилокси (Cbz) группа - удаляется гидрогенолизом
- п- Метоксибензилкарбонильная (Moz или MeOZ) группа - удаляется гидрогенолизом , более лабильна, чем Cbz
- трет- Бутилоксикарбонильная (BOC) группа (обычная для твердофазного пептидного синтеза ) - удаляется концентрированной сильной кислотой (такой как HCl или CF 3 COOH) или нагреванием до> 80 ° C.
- 9-Флуоренилметилоксикарбонильная ( Fmoc ) группа ( часто используется в твердофазном синтезе пептидов ) - удаляется основанием, таким как пиперидин
- Ацетил (Ас)Группа является обычной в синтезе олигонуклеотидов для защиты N4 в цитозине и N6 в нуклеиновых основаниях аденина и удаляется обработкой основанием, чаще всего водным или газообразным аммиаком или метиламином . Ас слишком стабилен, чтобы его можно было легко удалить из алифатических амидов.
- Бензоил (Bz)Группа является обычной в синтезе олигонуклеотидов для защиты N4 в цитозине и N6 в нуклеиновых основаниях аденина и удаляется обработкой основанием, чаще всего водным или газообразным аммиаком или метиламином. Bz слишком стабилен, чтобы его можно было легко удалить из алифатических амидов.
- Бензильная (Bn) группа - удаляется гидрогенолизом
- Карбаматная группа - удаляется кислотой и мягким нагреванием.
- п- метоксибензил (PMB) - удаляется гидрогенолизом , более лабильн, чем бензил
- 3,4-Диметоксибензил (DMPM) - удаляется гидрогенолизом , более лабильн, чем п- метоксибензил
- п- Метоксифенильная (PMP) группа - удаляется нитратом церия (IV) аммония (CAN)
- Тозильная (Ts) группа - удаляется концентрированной кислотой (HBr, H 2 SO 4 ) и сильными восстановителями ( натрий в жидком аммиаке или нафталинид натрия )
- Группа Troc (трихлорэтилхлорформиат) - удаляется введением Zn в присутствии уксусной кислоты
- Другие сульфаниламидные (нозильные и Nps) группы - удаляются йодидом самария , тиофенолом или другими мягкими тиоловыми нуклеофилами или гидридом трибутилолова.
Карбонильные защитные группы
Защита карбонильных групп:
- Ацетали и кетали - удаляются кислотой. Обычно ациклические ацетали расщепляются легче, чем циклические ацетали.
- Ацилалы - удаляются кислотами Льюиса .
- Дитианы - удаляются солями металлов или окислителями.
Защитные группы карбоновых кислот
Защита карбоновых кислот :
- Метиловые эфиры - удаляются кислотой или щелочью.
- Бензиловые эфиры - удаляются гидрогенолизом.
- трет- Бутиловые эфиры - удаляются кислотой, основанием и некоторыми восстановителями.
- Сложные эфиры 2,6-дизамещенных фенолов (например, 2,6-диметилфенол , 2,6-диизопропилфенол , 2,6-ди- трет- бутилфенол ) - удаляются при комнатной температуре метанолизом, катализируемым DBU, в условиях высокого давления.
- Силиловые эфиры - удаляются кислотными, щелочными и металлоорганическими реагентами.
- Ортоэфиры - удаляются слабой водной кислотой с образованием сложного эфира, который удаляется в соответствии со свойствами сложного эфира.
- Оксазолин - удаляется сильной горячей кислотой (pH <1, T> 100 ° C) или щелочью (pH> 12, T> 100 ° C), но не, например, LiAlH 4 , литийорганическими реагентами или реагентами Гриньяра (магнийорганические).
Фосфатные защитные группы
- 2-цианоэтил- снято мягкой базой. Группа широко используется в синтезе олигонуклеотидов .
- Метил (Me)- удаляется сильными нуклеофилами ec . тиофенол / TEA.
Терминальные защитные группы алкинов
- Пропаргиловые спирты в реакции Фаворского ,
- Силильные группы, особенно в защите самого ацетилена .
Другой
Ортогональная защита

Ортогональная защита - это стратегия, позволяющая специфически снять защиту с одной защитной группы в многократно защищенной структуре, не затрагивая другие. Например, тирозин аминокислоты может быть защищен в виде сложного бензилового эфира по карбоксильной группе, флуоренилметиленоксикарбамата по аминогруппе и трет- бутилового эфира по фенольной группе. Бензиловый эфир можно удалить гидрогенолизом, флуоренилметиленоксигруппу (Fmoc) - основаниями (такими как пиперидин) и фенольным трет- бутиловым эфиром, расщепленным кислотами (например, трифторуксусной кислотой).
Типичный пример для этого применения, синтез Fmoc-пептида, в котором пептиды выращивают в растворе и на твердой фазе, очень важен. Защитные группы в твердофазном синтезе в отношении условий реакции, таких как время реакции, температура и реагенты, могут быть стандартизованы так, чтобы они выполнялись с помощью машины, при этом выходы могут быть намного выше 99%. В противном случае разделение полученной смеси продуктов реакции практически невозможно.
Техника была введена в области синтеза пептидов с помощью Роберта Брюсом Merrifield в 1977 г. В качестве доказательства концепции ортогонального снятия защиты демонстрируется в фотохимической реакции переэтерификации с помощью триметилсилилдиазометана , использующего кинетического изотопного эффект :
Благодаря этому эффекту квантовый выход для снятия защиты правой сложноэфирной группы снижается, и она остается неизменной. Существенно, что при размещении атомов дейтерия рядом с левой сложноэфирной группой или путем изменения длины волны до 254 нм получается другой моноарен.
Критика
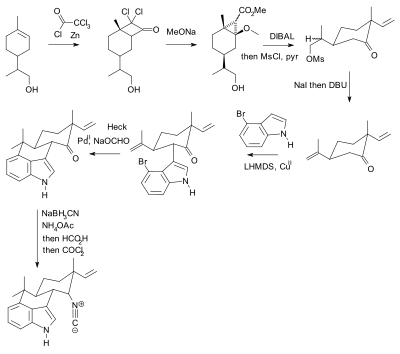
Использование защитных групп повсеместно, но не без критики. На практике их использование добавляет к синтезу две стадии (последовательность защиты-снятия защиты), одна или обе из которых могут значительно снизить химический выход . Крайне важно, что дополнительная сложность препятствует использованию полного синтетического синтеза при открытии лекарств . Напротив, в биомиметическом синтезе защитные группы не используются. В качестве альтернативы Баран представил новый синтез соединения гапалиндола U без защитных групп. Ранее опубликованный синтез по Барану содержал 20 стадий с множественными манипуляциями с защитными группами (два подтвержденных):
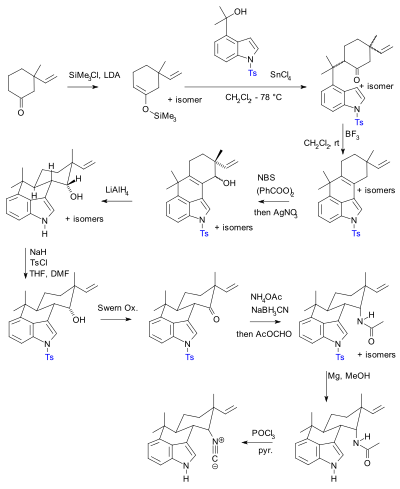
Синтез Хидеаки Муратаке 1990 года с использованием тозильных защитных групп (показаны синим).
|
Промышленное применение
Хотя использование защитных групп не является предпочтительным в промышленном синтезе, они все еще используются в промышленных условиях, например:
- Осельтамивир (противовирусный препарат Тамифлю) синтез компании Рош
- Сукралоза (подсластитель)
использованная литература
внешние ссылки
- Введение защитной группы и механизма снятия защиты
- Заметки по этому предмету для старших курсов бакалавриата от профессора Риццо.
- Еще один набор учебных примечаний в виде учебника с рекомендациями и комментариями от проф. Гроссман и Каммерс.
- Обзор профессора Коциенского.
- Сайт пользователя, на котором приводится классический текст Грина и Ватса о стабильности нескольких ключевых групп из обширных таблиц этого справочника.
- Защита группы от organic-reaction.com