Период - Periodate
 Метапериодат-ион
|
|
 Ортопериодат-ион
|
|
| Имена | |
|---|---|
|
Систематическое название ИЮПАК
тетраоксойодат (1-) гексаоксойодат (5-) |
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
| UNII | |
|
|
|
|
| Характеристики | |
| IO 4 - или IO 6 5- | |
| Конъюгированная кислота | Периодическая кислота |
| Родственные соединения | |
|
Другие анионы
|
Перхлорат пербромат перманганат |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
| Ссылки на инфобоксы | |
Периодатное / р ə г aɪ . ə d eɪ t / - анион, состоящий из йода и кислорода . Это один из ряда оксианионов йода и самый высокий в ряду, причем йод существует в степени окисления +7. В отличие от других пергалогенатов, таких как перхлорат , он может существовать в двух формах: метапериодат IO.-
4и ортопериодат IO5-
6. В этом отношении он сопоставим с теллурат- ионом из соседней группы . Он может объединяться с рядом противоионов с образованием периодатов , которые также можно рассматривать как соли периодной кислоты .
Периодаты были открыты Генрихом Густавом Магнусом и К.Ф. Аммермюллером; кто первым синтезировал периодическую кислоту в 1833 году.
Синтез
Классически периодат чаще всего производился в форме гидроперидата натрия (Na 3 H 2 IO 6 ). Это является коммерчески доступным, но также может быть получено при окислении иодатов с хлором и гидроксидом натрия . Или, аналогично, из йодидов путем окисления бромом и гидроксидом натрия:
- NaIO 3 + Cl 2 + 4 NaOH → Na 3 H 2 IO 6 + 2 NaCl + H 2 O
- NaI + 4 Br 2 + 10 NaOH → Na 3 H 2 IO 6 + 8 NaBr + 4 H 2 O
Современное промышленное производство включает электрохимическое окисление йодатов на аноде из PbO 2 со следующим стандартным электродным потенциалом :
Метапериодаты обычно получают дегидратацией гидропериодата натрия азотной кислотой или дегидратацией ортопериодной кислоты путем ее нагревания до 100 ° C в вакууме.
- Na 3 H 2 IO 6 + 2 HNO 3 → NaIO 4 + 2 NaNO 3 + 2 H 2 O
- H 5 IO 6 → HIO 4 + 2 H 2 O
Они также могут быть получены непосредственно из йодатов при обработке другими сильными окислителями, такими как гипохлориты :
Формы и взаимопревращение
Периодат может существовать в различных формах в водной среде, при этом pH является контролирующим фактором. Ортопериодат имеет ряд констант диссоциации кислоты .
H 5 IO 6 ⇌ ЧАС
4IO-
6+ H + p K a = 3,29 ЧАС
4IO-
6⇌ ЧАС
3IO2-
6+ H + p K a = 8,31 ЧАС
3IO2-
6⇌ ЧАС
2IO3-
6+ H + p K a = 11,60
Орто- и метапериодатные формы также существуют в равновесии.
-
ЧАС
4IO-
6⇌ IO-
4+ 2 Н 2 О, К = 29
По этой причине orthoperiodate иногда упоминается как ди гидрата метапериодата, написанный И.О.-
4· 2H 2 O ; однако это описание не является строго точным, поскольку рентгеновская кристаллография H 5 IO 6 показывает 5 эквивалентных групп I – OH.
При экстремальных значениях pH могут образовываться дополнительные виды. В основных условиях может происходить реакция дегидратации с образованием дипериодата (иногда называемого мезопериодатом).
- 2 ч
3IO2-
6⇌ H
2я
2О4-
10+ 2 Н 2 О, К = 820
В сильнокислых условиях периодическая кислота может быть протонирована с образованием катиона ортопериодония .
-
ЧАС
6IO+
6⇌ H 5 IO 6 + H + , p K a = −0,8
Структура и склеивание
Как в орто-, так и в метапериодате йод является гипервалентным , так как он образует больше связей, чем обычно допускается. Это было объяснено с точки зрения дативных связей , подтверждающих отсутствие двойной связи в этих молекулах.
Точные структуры различаются в зависимости от противоионов, однако в среднем ортопериодаты принимают слегка деформированную октаэдрическую геометрию с дифракцией рентгеновских лучей, показывающей длину связи I – O 1,89 Å . Метапериодаты имеют искаженную тетраэдрическую геометрию со средним расстоянием I – O 1,78 Å.
Реакции
Реакции расщепления
Периодаты могут расщеплять углерод-углеродные связи на различных 1,2-дифункциональных алканах. Наиболее распространенным примером этого является расщепление диола , которое также было обнаружено первым ( реакция Малапрада ). Помимо диолов , периодаты могут расщеплять 1,2-гидроксикетоны , 1,2-дикетоны , α-кетокислоты , α-гидроксикислоты , аминокислоты , 1,2-аминоспирты , 1,2-диамины и эпоксиды с образованием дают альдегиды, кетоны и карбоновые кислоты.
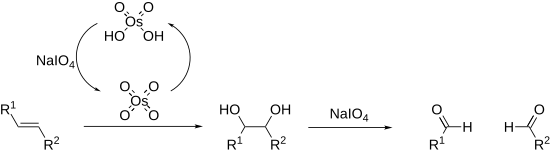
Алкены также могут окисляться и расщепляться при окислении Лемье-Джонсона . При этом используется каталитическая загрузка четырехокиси осмия, которая регенерируется периодатом in situ. Общий процесс эквивалентен озонолизу .
Реакции расщепления протекают через циклический промежуточный продукт, называемый сложным эфиром периодата. На его образование могут влиять pH и температура, но наиболее сильно на него влияет геометрия субстрата, при этом цис- диолы реагируют значительно быстрее, чем транс- диолы. Реакции экзотермические и обычно проводятся при 0 ° C. Поскольку соли периодата легко растворяются в воде, реакции обычно проводят в водной среде. Если растворимость является проблемой, может использоваться периодическая кислота, поскольку она растворима в спиртах; катализаторы межфазного переноса также эффективны в двухфазных реакционных смесях. В крайних случаях периодат можно заменить на тетраацетат свинца, который реагирует аналогичным образом и растворим в органических растворителях ( окисление Криджи ).
Расщепление периодатом часто используется в молекулярной биохимии для модификации сахаридных колец, поскольку многие пяти- и шестичленные сахара содержат вицинальные диолы . Исторически его также использовали для определения структуры моносахаридов.
Расщепление периодатом можно проводить в промышленном масштабе с образованием диальдегидного крахмала, который используется в производстве бумаги .
Реакции окисления
Периодаты - сильные окислители . Они могут окислять катехол до 1,2-бензохинона и гидрохинон до 1,4-бензохинона . Сульфиды можно эффективно окислять до сульфоксидов . Периодаты являются достаточно мощными для образования других сильных неорганических окислителей, таких как перманганат , четырехокись осмия и четырехокись рутения .
Ниша использует
Периодаты являются высокоселективными травителями для некоторых оксидов на основе рутения .
Несколько окрашивания агенты используют в микроскопии основаны вокруг периодат (например , периодической кислотно-Шиффа пятна и пятна Джонса )
Периодаты также использовались в качестве окислителей в пиротехнике . В 2013 году армия США объявила , что она могла бы заменить экологически вредные химические вещества , нитрат бария и перхлората калия с метапериодат натрия для использования в их трассирующих боеприпасов.
Другие оксианионы
Периодат является частью ряда оксианионов, в которых йод может принимать степени окисления -1, +1, +3, +5 или +7. Также известен ряд нейтральных оксидов йода .
| Степень окисления йода | −1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| Имя | йодид | гипойодит | йодит | йодат | периодировать |
| Формула | Я - | IO - |
IO- 2 |
IO- 3 |
IO- 4или IO5- 6 |
| Состав |

|
|
|