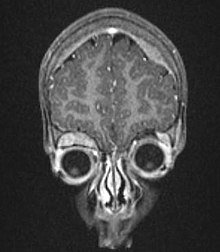
Нейробластома - Neuroblastoma
| Нейробластома | |
|---|---|
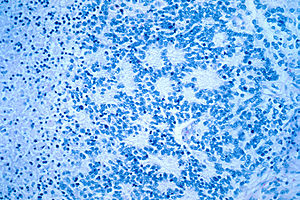 | |
| Микроскопический вид типичной нейробластомы с образованием розетки | |
| Специальность | Нейроонкология |
| Симптомы | Боль в костях, уплотнения |
| Обычное начало | До 5 лет |
| Причины | Генетическая мутация |
| Диагностический метод | Биопсия ткани |
| Уход | Наблюдение, хирургия, радиация , химиотерапия , трансплантация стволовых клеток |
| Прогноз | США пятилетняя выживаемость ~ 95% (<1 года), 68% (1-14 лет) |
| Частота | 1 из 7000 детей |
| Летальные исходы | 15% смертей от рака у детей |
Нейробластома ( NB ) - это тип рака, который формируется в определенных типах нервной ткани . Чаще всего он начинается с одного из надпочечников, но также может развиваться в шее , груди , животе или позвоночнике . Симптомы могут включать боль в костях , уплотнение в брюшной полости, шее или груди или безболезненное синюшное уплотнение под кожей.
Обычно нейробластома возникает из-за генетической мутации, происходящей на раннем этапе развития . В редких случаях это может быть связано с мутацией, унаследованной от родителей . Факторов окружающей среды не обнаружено. Диагноз ставится на основании биопсии ткани . Иногда его можно обнаружить у ребенка при УЗИ во время беременности . На момент постановки диагноза рак обычно уже распространился . Рак делится на группы низкого, среднего и высокого риска в зависимости от возраста ребенка, стадии рака и внешнего вида рака.
Лечение и исходы зависят от группы риски людей находятся. Лечение может включать в себя наблюдение, хирургию, радиацию , химиотерапию или трансплантацию стволовых клеток . Заболевание с низким уровнем риска у младенцев обычно имеет хороший исход при хирургическом вмешательстве или простом наблюдении. Однако при заболевании высокого риска шансы на долгосрочное выживание составляют менее 40%, несмотря на агрессивное лечение.
Нейробластома является наиболее распространенным раком у младенцев и третьим по распространенности раком у детей после лейкемии и рака мозга . Около одного из 7000 детей когда-либо страдает. Около 90% случаев возникают у детей младше 5 лет и редко у взрослых. Около 15% случаев смерти детей от рака вызваны нейробластомой. Заболевание впервые было описано в 1800-х годах.
Признаки и симптомы
Первые симптомы нейробластомы часто расплывчаты, что затрудняет диагностику. Часто наблюдаются утомляемость , потеря аппетита , лихорадка и боли в суставах. Симптомы зависят от локализации первичной опухоли и наличия метастазов:
- В брюшной полости опухоль может вызвать вздутие живота и запор .
- Опухоль в груди может вызвать проблемы с дыханием .
- Опухоль, давящая на спинной мозг, может вызвать слабость , которая приводит к неспособности стоять, ползать или ходить.
- Поражения костей ног и бедер могут вызывать боль и хромоту.
- Опухоль в костях вокруг глаз или орбит может вызвать явный синяк и отек.
- Проникновение в костный мозг может вызвать бледность от анемии .
Нейробластома часто распространяется на другие части тела до того, как проявляются какие-либо симптомы, и от 50 до 60% всех случаев нейробластомы имеют метастазы .
Чаще всего возникает нейробластома (т.е. первичная опухоль) в надпочечниках. Это происходит в 40% локализованных опухолей и в 60% случаев широко распространенного заболевания. Нейробластома также может развиваться в любом месте цепочки симпатической нервной системы от шеи до таза. Частота в разных местах включает: шею (1%), грудь (19%), живот (30% непочечников) или таз (1%). В редких случаях первичная опухоль не определяется.
Редкие, но характерные проявления включают поперечную миелопатию (сдавление спинного мозга опухолью, 5% случаев), резистентную к лечению диарею ( секреция вазоактивных кишечных пептидов опухолью , 4% случаев), синдром Хорнера (опухоль шейки матки, 2,4% случаев), миоклонус опсоклонуса. синдром и атаксия (подозрение на паранеопластическую причину, 1,3% случаев) и артериальная гипертензия ( секреция катехоламинов или компрессия почечной артерии, 1,3% случаев).
Причина
Причина нейробластомы до конца не изучена. Подавляющее большинство случаев носят спорадический и несемейный характер. Около 1-2% случаев передаются в семьях и связаны с конкретными генными мутациями. Семейная нейробластома в некоторых случаях вызвана редкими мутациями зародышевой линии в гене киназы анапластической лимфомы ( ALK ). Мутации зародышевой линии в генах PHOX2B или KIF1B также вовлечены в семейную нейробластому. Нейробластома также является признаком нейрофиброматоза 1 типа и синдрома Беквита-Видемана .
Амплификация онкогена MYCN в опухоли - частая находка при нейробластоме. Степень амплификации показывает бимодальное распределение: от 3 до 10 или от 100 до 300 раз. Наличие этой мутации тесно связано с поздними стадиями заболевания.
Было показано, что дублированные сегменты гена LMO1 в опухолевых клетках нейробластомы увеличивают риск развития агрессивной формы рака.
Нейробластома связана с изменением числа копий в гене NBPF10 , что приводит к синдрому делеции 1q21.1 или синдрому дупликации 1q21.1 .
Было предложено несколько факторов риска, которые являются предметом текущих исследований. Из-за характерного раннего начала многие исследования были сосредоточены на родительских факторах, связанных с зачатием и во время беременности . Исследованные факторы включали род занятий (т.е. воздействие химических веществ в определенных отраслях), курение, употребление алкоголя, использование лекарственных препаратов во время беременности и факторы рождения; однако результаты были неубедительными.
В других исследованиях изучались возможные связи с атопией и подверженностью инфекциям в раннем возрасте, с использованием гормонов и препаратов для лечения бесплодия, а также с использованием красок для волос матерями.
Диагностика
Диагноз обычно подтверждает хирург-патолог с учетом клинической картины, результатов микроскопии и других лабораторных исследований. Он может возникать из любого элемента нервного гребня симпатической нервной системы (СНС).
Считается , что эстезионейробластома , также известная как обонятельная нейробластома, возникает из обонятельного эпителия, и ее классификация остается спорной. Однако, поскольку это не злокачественное новообразование симпатической нервной системы, эстезионейробластома представляет собой отдельную клиническую сущность, и ее не следует путать с нейробластомой.
Биохимия
Примерно в 90% случаев нейробластомы повышенный уровень катехоламинов или их метаболитов обнаруживается в моче или крови. Катехоламины и их метаболиты включают дофамин , гомованилиновую кислоту (HVA) и / или ваниллилминдельную кислоту (VMA).
Визуализация
Другим способом обнаружения нейробластомы является сканирование мета-йодобензилгуанидином , которым занимаются от 90 до 95% всех нейробластом, часто называемых «mIBG-авидными». Механизм заключается в том, что mIBG захватывается симпатическими нейронами и является функциональным аналогом нейромедиатора норадреналина . Когда он радиоактивно йодирован I-131 или I-123 (радиоактивные изотопы йода ), он является очень хорошим радиофармацевтическим препаратом для диагностики и мониторинга реакции на лечение этого заболевания. I-123 с периодом полураспада 13 часов является предпочтительным изотопом с точки зрения чувствительности и качества изображения. I-131 имеет период полураспада 8 дней, и в более высоких дозах он является эффективным направленным облучением против рецидивирующей и рефрактерной нейробластомы. Поскольку mIBG не всегда используется нейробластомами, исследователи изучали у детей с нейробластомой, может ли быть полезным другой тип ядерной визуализации, фтордезоксиглюкозо-позитронно-эмиссионная томография, часто называемая F-FDG-PET. Имеющиеся данные свидетельствуют о том, что это может быть целесообразно использовать у детей с нейробластомой, для которых mIBG не работает, но в этой области необходимы дополнительные исследования.
Гистология
При микроскопии опухолевые клетки обычно описываются как маленькие, круглые и синие, и можно увидеть узоры в виде розеток ( псевдорозетки Гомера Райта ). Псевдорозетки Гомера Райта - это опухолевые клетки вокруг нейропиля , не путать с настоящими розетками, которые представляют собой опухолевые клетки вокруг пустого просвета. Они также отличаются от псевдорозеток эпендимомы, которые состоят из опухолевых клеток с глиальным фибриллярным кислым белком (GFAP) - положительными процессами, сужающимися к кровеносному сосуду (таким образом, комбинация этих двух). Патологоанатомы используют различные иммуногистохимические окрашивания, чтобы отличить нейробластомы от гистологических имитаторов, таких как рабдомиосаркома , саркома Юинга , лимфома и опухоль Вильмса .
Нейробластома - одна из периферических нейробластических опухолей (pNT), которые имеют схожее происхождение и демонстрируют широкий спектр дифференцировки, начиная от доброкачественной ганглионевромы и заканчивая ганглионейробластомой с высоким содержанием стромы со смешанными нейробластическими клетками или узелками, а также высокозлокачественной нейробластомой. Это различие в опухолевой патологии до лечения является важным прогностическим фактором, наряду с возрастом и митозом - индексом кариорексиса ( MKI ). Эта система классификации патологий (система Шимада) описывает «благоприятные» и «неблагоприятные» опухоли Международным комитетом по патологии нейробластомы (INPC), который был создан в 1999 году и пересмотрен в 2003 году.
Постановка
«Международная система стадирования нейробластомы» (INSS), созданная в 1986 г. и пересмотренная в 1988 г., разделяет нейробластому в соответствии с ее анатомическим наличием при постановке диагноза:
- Стадия 1: локализованная опухоль, ограниченная областью происхождения.
- Стадия 2А: односторонняя опухоль с неполной грубой резекцией; идентифицируемые ипсилатеральные и контралатеральные лимфатические узлы отрицательны на опухоль.
- Стадия 2B: односторонняя опухоль с полной или неполной грубой резекцией; с положительным на опухоль ипсилатеральным лимфатическим узлом; идентифицируемый контралатеральный лимфатический узел отрицательный на опухоль.
- Стадия 3: инфильтрация опухоли по средней линии с вовлечением регионарных лимфатических узлов или без них; или односторонняя опухоль с поражением контралатеральных лимфатических узлов; или срединная опухоль с двусторонним поражением лимфатических узлов.
- Стадия 4: распространение опухоли на отдаленные лимфатические узлы, костный мозг, кости, печень или другие органы, за исключением случаев, определенных стадией 4S.
- Стадия 4S: возраст <1 года с локализованной первичной опухолью, как определено на стадии 1 или 2, с диссеминацией, ограниченной печенью, кожей или костным мозгом (менее 10 процентов ядерных клеток костного мозга являются опухолями).
Хотя использовалось международное соглашение о стадиях (INSS), также была признана необходимость международного консенсуса по определению риска для сравнения аналогичных когорт по результатам исследований. Начиная с 2005 года, представители основных кооперативных групп педиатрической онкологии встретились, чтобы рассмотреть данные о 8 800 людях с нейробластомой, пролеченных в Европе, Японии, США, Канаде и Австралии в период с 1990 по 2002 год. Эта целевая группа предложила Международную группу риска нейробластомы ( INRG) система классификации. Ретроспективные исследования выявили высокую выживаемость в возрастной группе 12–18 месяцев, ранее отнесенной к группе высокого риска, и побудили к решению переквалифицировать детей в возрасте 12–18 месяцев без амплификации N- myc (также обычно называемой MYCN ) на промежуточную. категория риска.
Новое определение риска INRG будет классифицировать нейробластому при постановке диагноза на основе новой Международной системы стадирования риска нейробластомы (INRGSS):
- Стадия L1: локализованное заболевание без определенных факторов риска.
- Стадия L2: локализованное заболевание с определенными визуальными факторами риска.
- Стадия M: метастатическое заболевание.
- Стадия РС: метастатическое заболевание «особенное», где РС эквивалентна стадии 4S.
Новая стратификация риска будет основана на новой системе стадирования INRGSS, возрасте (дихотомия через 18 месяцев), степени опухоли, амплификации N-myc , несбалансированной аберрации 11q и плоидности на четыре группы риска до лечения: очень низкий, низкий, средний. , и высокий риск.
Скрининг
Уровень катехоламинов в моче может быть повышен при доклинической нейробластоме. Скрининг бессимптомных младенцев в возрасте трех недель, шести месяцев и одного года проводится в Японии, Канаде, Австрии и Германии с 1980-х годов. Япония начала скрининг шестимесячных детей на нейробластому посредством анализа уровней гомованилловой кислоты и ванилминдальной кислоты в 1984 году. Скрининг был остановлен в 2004 году после того, как исследования, проведенные в Канаде и Германии, не показали снижения смертности от нейробластомы, а скорее вызвали рост заболеваемости. диагнозы, которые исчезли бы без лечения, подвергая этих младенцев ненужной хирургии и химиотерапии.
Уход
Когда поражение локализовано, оно, как правило, излечимо. Однако, несмотря на агрессивную мультимодальную терапию (интенсивная химиотерапия , хирургическое вмешательство , лучевая терапия , трансплантация стволовых клеток , дифференцирующий агент изотретиноин, также называемый 13- цис- ретиноевой кислотой, и часто иммунотерапия с использованием моноклональных антител против GD2 - динутуксимаб ).
Были идентифицированы биологические и генетические характеристики, которые в сочетании с классической клинической стадией позволили отнести к группам риска для планирования интенсивности лечения. Эти критерии включают в себя возраст человека, степень распространения болезней, микроскопический внешний вид и генетических особенностей , включая ДНК плоидности и N-Myc онкогена усиления (N-Myc регулирует микроРНК ), в низкого, среднего и высокого риска заболевания. В недавнем биологическом исследовании (COG ANBL00B1) было проанализировано 2687 человек с нейробластомой, и был определен спектр распределения риска: 37% случаев нейробластомы относятся к низкому риску, 18% - к промежуточному риску и 45% - к высокому риску. (Есть некоторые свидетельства того, что типы высокого и низкого риска вызваны разными механизмами, а не просто двумя разными степенями выражения одного и того же механизма.)
Методы лечения для этих разных категорий риска очень разные.
- Заболевания низкого риска часто наблюдаются без какого-либо лечения или излечиваются только хирургическим вмешательством.
- Заболевания среднего риска лечат хирургическим вмешательством и химиотерапией .
- Нейробластома высокого риска лечится с помощью интенсивной химиотерапии, хирургии , лучевой терапии , трансплантации костного мозга / гемопоэтических стволовых клеток , биологической терапии 13- цис- ретиноевой кислотой ( изотретиноин или аккутан) и терапии антителами, обычно назначаемой с цитокинами GM-CSF. и Ил-2 . Мета-анализ обнаружил доказательства того, что у детей с нейробластомой высокого риска лечение миелоаблативной терапией улучшает бессобытийную выживаемость, но может увеличивать риск побочных эффектов, таких как проблемы с почками, по сравнению с традиционной химиотерапией.
У людей с заболеваниями низкого и среднего риска отличный прогноз с коэффициентом излечения выше 90% для низкого риска и 70–90% для среднего риска. Напротив, терапия нейробластомы высокого риска в течение последних двух десятилетий приводила к излечению только в 30% случаев. Добавление терапии антителами значительно повысило выживаемость при заболеваниях высокого риска. В марте 2009 года ранний анализ исследования Детской онкологической группы (COG) с 226 людьми из группы высокого риска показал, что через два года после трансплантации стволовых клеток 66% группы, рандомизированной для получения антитела ch14.18 с GM-CSF и IL. -2 были живы и не имели болезней по сравнению с 46% в группе, которая не получала антитела. Рандомизация была остановлена, поэтому все люди, участвующие в исследовании, получали терапию антителами.
Было обнаружено, что химиотерапевтические агенты, используемые в комбинации, эффективны против нейробластомы. Агентами, обычно используемыми для индукции и кондиционирования трансплантации стволовых клеток, являются соединения платины ( цисплатин , карбоплатин ), алкилирующие агенты ( циклофосфамид , ифосфамид , мелфалан ), ингибитор топоизомеразы II ( этопозид ), антрациклиновые антибиотики ( доксорубицин ) и алкалоиды винка ( винкристин ). Некоторые новые схемы включают индукцию ингибиторов топоизомеразы I ( топотекан и иринотекан ), которые оказались эффективными против рецидивов заболевания.
В ноябре 2020 года накситамаб был одобрен для медицинского применения в Соединенных Штатах в сочетании с гранулоцитарно-макрофагальным колониестимулирующим фактором (GM-CSF) для лечения людей в возрасте одного года и старше с нейробластомой высокого риска в костном или костном мозге, у которых опухоль не отреагировал на предыдущее лечение или вернулся после него и показал частичный ответ, незначительный ответ или стабильное заболевание на предыдущую терапию.
Прогноз
По данным из Англии , общая 5-летняя выживаемость нейробластомы составляет 67%. От 20% до 50% случаев высокого риска не отвечают должным образом на индукционную химиотерапию высокими дозами и являются прогрессирующими или резистентными. Рецидивы после завершения первичной терапии также распространены. Дальнейшее лечение доступно в клинических испытаниях фазы I и фазы II, в которых тестируются новые агенты и комбинации агентов против нейробластомы, но результат остается очень плохим для рецидивов заболевания высокого риска.
Большинство выживших в течение длительного периода времени, живущих сегодня, имели заболевание низкого или среднего риска и более мягкие курсы лечения по сравнению с заболеванием высокого риска. Большинство выживших имеют долгосрочные последствия лечения. Лица, пережившие лечение среднего и высокого риска, часто страдают потерей слуха, снижением роста, нарушениями функции щитовидной железы, трудностями в обучении и повышенным риском вторичного рака у выживших после болезни высокого риска. По оценкам, у двух из трех выживших после детского рака в конечном итоге разовьется по крайней мере одна хроническая, а иногда и опасная для жизни проблема со здоровьем в течение 20–30 лет после постановки диагноза рака.
Цитогенетические профили
На основе серии из 493 образцов нейробластомы было сообщено, что общий геномный паттерн, проверенный кариотипированием на основе массивов , является предиктором исхода при нейробластоме:
- Опухоли, представляющие исключительно изменения числа копий целой хромосомы, были связаны с отличной выживаемостью.
- Опухоли с любыми изменениями числа копий сегментных хромосом были связаны с высоким риском рецидива.
- В опухолях, показывающих сегментарные изменения, дополнительными независимыми предикторами снижения общей выживаемости были амплификация N-myc , делеции 1p и 11q и усиление 1q.
В более ранних публикациях нейробластомы были разделены на три основных подтипа на основе цитогенетических профилей:
- Подтип 1: благоприятная нейробластома с почти триплоидией и преобладанием численных прибылей и убытков, в основном представляющая неметастатические NB стадии 1, 2 и 4S.
- Подтипы 2A и 2B: обнаруживаются при неблагоприятной широко распространенной нейробластоме, стадии 3 и 4, с потерей 11q и увеличением 17q без амплификации N-myc (подтип 2A) или с амплификацией N-myc, часто вместе с делециями 1p и увеличением 17q (подтип 2B).
Виртуальное кариотипирование может быть выполнено на свежих или залитых парафином опухолях для оценки количества копий в этих локусах. Виртуальное кариотипирование массива SNP является предпочтительным для образцов опухолей, включая нейробластомы, потому что они могут обнаруживать потерю копии нейтральной гетерозиготности (приобретенная униородительская дисомия). Копионно-нейтральный LOH может быть биологически эквивалентен делеции и был обнаружен в ключевых локусах нейробластомы. ArrayCGH, FISH или обычная цитогенетика не могут обнаружить копийно-нейтральный LOH.
Эпидемиология

Нейробластома составляет 6–10% всех онкологических заболеваний у детей и 15% случаев смерти от рака у детей. Годовой уровень смертности составляет 10 на миллион детей в возрастной группе от 0 до 4 лет и 4 на миллион детей в возрастной группе от 4 до 9 лет.
Наибольшее количество случаев приходится на первый год жизни, а некоторые случаи являются врожденными . Возрастной диапазон широк, включая детей старшего возраста и взрослых, но только 10% случаев встречаются у людей старше 5 лет. Крупное европейское исследование показало, что менее 2% из более чем 4000 случаев нейробластомы были старше 18 лет.
История

В 1864 году немецкий врач Рудольф Вирхов первым описал опухоль брюшной полости у ребенка как «глиому». Характеристики опухолей симпатической нервной системы и мозгового вещества надпочечников были отмечены в 1891 году немецким патологом Феликсом Маршаном . В 1901 году Уильям Пеппер описал отчетливое проявление стадии 4S у младенцев (печень, но без метастазов в кости). В 1910 году Джеймс Гомер Райт понял, что опухоль возникла из примитивных нервных клеток, и назвал ее нейробластомой. Он также отметил круглые скопления клеток в образцах костного мозга, которые теперь называют «розетками Гомера Райта». Следует отметить, что «Гомер-Райт» с дефисом грамматически неверно, так как эпоним относится только к доктору Райту.
Общество и культура
Законодательные усилия
Представитель США Чет Эдвардс из Уэйко , штат Техас , успешно принял закон о выделении 150 миллионов долларов на лечение нейробластомы и других видов рака. Закон был подписан в июле 2008 года президентом США Джорджем Бушем . Эдвардс был вдохновлен болезнью и последующей смертью Эрин Ченнинг Бюнгер (1997–2009) Брайана , дочери одного из его избирателей Уолтера Л. Бюнгера , главы исторического факультета Техасского университета A&M .
Исследовать
Доклинические модели
Ксенотрансплантаты опухоли (PDX), полученные от пациента с нейробластомой , были созданы путем ортотопической имплантации образцов опухоли иммунодефицитным мышам. Модели PDX имеют несколько преимуществ перед обычными линиями раковых клеток (CCL) . PDX нейробластомы сохраняют генетические признаки соответствующих опухолей, а PDX демонстрируют инфильтративный рост и метастазы в отдаленные органы. Модели PDX более предсказуемы в отношении клинического исхода по сравнению с обычными ксенотрансплантатами линии раковых клеток. Таким образом, PDX нейробластомы могут служить клинически значимыми моделями для идентификации эффективных соединений против нейробластомы.
Лечение
В последнее время основное внимание уделялось сокращению терапии нейробластомы низкого и среднего риска при сохранении выживаемости на уровне 90%. Исследование 467 человек, относящихся к группе промежуточного риска, включенных в A3961 с 1997 по 2005 год, подтвердило гипотезу о том, что терапия может быть успешно снижена для этой группы риска. Пациенты с благоприятными характеристиками (степень опухоли и ответ) получали четыре цикла химиотерапии, а пациенты с неблагоприятными характеристиками - восемь циклов, с трехлетней выживаемостью без событий и общей выживаемостью, стабильной на уровне 90% для всей когорты. В планах на будущее - усиление лечения людей с аберрацией хромосом 1p36 или 11q23, а также тех, у кого нет раннего ответа на лечение.
Напротив, последние 20 или более лет основное внимание уделялось усилению лечения нейробластомы высокого риска. Продолжается изучение вариантов индукции химиотерапии, времени операции, режимов трансплантации стволовых клеток, различных схем доставки облучения и использования моноклональных антител и ретиноидов для лечения минимальной остаточной болезни. Недавние клинические испытания фазы III с рандомизацией были проведены, чтобы ответить на эти вопросы, чтобы улучшить выживаемость при заболеваниях высокого риска:
Рефрактерная и рецидивирующая нейробластома
Химиотерапия топотеканом и циклофосфамидом часто используется при рефрактерной терапии и после рецидива.
Гаплоидентичная трансплантация стволовых клеток , то есть донорские клетки, полученные от родителей, изучается у пациентов с рефрактерной или рецидивирующей нейробластомой, поскольку стволовые клетки от самого человека бесполезны.
использованная литература
внешние ссылки
| Классификация | |
|---|---|
| Внешние ресурсы |