Молекулярный датчик - Molecular sensor
Молекулярный датчик или хемосенсорный представляет собой молекулярную структуру (органические или неорганические комплексы) , который используется для измерения из анализируемого вещества для получения выявляемого изменения или сигнала . Действие хемосенсора зависит от взаимодействия, происходящего на молекулярном уровне, обычно включает непрерывный мониторинг активности химических веществ в данной матрице, такой как раствор, воздух, кровь, ткань, сточные воды, питьевая вода и т. Д. Применение хемосенсоров называется хемосенсингом, который представляет собой форму молекулярного распознавания . Все хемосенсоры сконструированы так, чтобы содержать сигнальный фрагмент и фрагмент распознавания , которые связаны либо непосредственно друг с другом, либо через какой-либо соединитель или спейсер. Передача сигналов часто основана на оптическом электромагнитном излучении , вызывающем изменения либо (или обоих) ультрафиолетового и видимого поглощения или эмиссионных свойств датчиков. Хемосенсоры также могут иметь электрохимическую основу. Сенсоры на малых молекулах относятся к хемосенсорам. Однако они традиционно считаются структурно простыми молекулами и отражают необходимость образования хелатирующих молекул для комплексообразования ионов в аналитической химии . Хемосенсоры являются синтетическими аналогами биосенсоров , разница в том, что биосенсоры включают в себя биологические рецепторы, такие как антитела, аптамеры или большие биополимеры.
Хемосенсоры описывают молекулы синтетического происхождения, которые сигнализируют о наличии вещества или энергии. Хемосенсор можно рассматривать как разновидность аналитического прибора. Хемосенсоры используются в повседневной жизни и применяются в различных областях, таких как химия, биохимия, иммунология, физиология и т. Д., И в медицине в целом, например, при анализе образцов крови в отделениях неотложной помощи. Хемосенсоры могут быть разработаны для обнаружения / передачи сигналов отдельного аналита или смеси таких веществ в растворе. Это может быть достигнуто либо за счет однократного измерения, либо за счет использования непрерывного мониторинга. Сигнальный фрагмент действует как преобразователь сигнала , преобразуя информацию (событие распознавания между хемосенсором и анализируемым веществом) в оптический ответ ясным и воспроизводимым образом.
Чаще всего изменение (сигнал) наблюдается путем измерения различных физических свойств хемосенсора, таких как фотофизические свойства, наблюдаемые в поглощении или излучении , где используются разные длины волн электромагнитного спектра . Следовательно, большинство хемосенсоров описываются как колориметрические ( основное состояние ) или люминесцентные ( возбужденное состояние , флуоресцентные или фосфоресцентные ). Колориметрические хемосенсоры вызывают изменения в их абсорбционных свойствах (регистрируемых с помощью ультрафиолетовой и видимой спектроскопии ), таких как интенсивность поглощения и длина волны или хиральность (с использованием циркулярно поляризованного света и спектроскопии КД ).
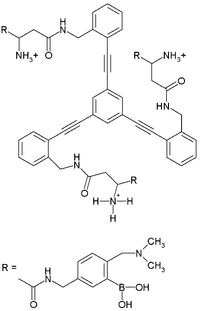 |
 |
|||
| Связывание гепарина | Связывание дубильной кислоты | Связывание сакситоксина |
Напротив, тогда в случае люминесцентных хемосенсоров обнаружение аналита с использованием флуоресцентной спектроскопии вызывает спектральные изменения в возбуждении флуоресценции или в спектрах излучения, которые регистрируются с помощью флуориметра . Такие изменения могут также происходить в других свойствах возбужденного состояния, таких как время жизни (с) возбужденного состояния, квантовый выход флуоресценции, поляризации и т. Д. Хемосенсора. Детектирование флуоресценции может быть достигнуто при низкой концентрации (ниже ~ 10-6 М) с помощью большинства флуоресцентных спектрометров. Это дает преимущество использования датчиков непосредственно в волоконно-оптических системах. Примерами использования хемосенсоров являются контроль содержания в крови, концентрации лекарств и т. Д., А также в пробах окружающей среды. Ионы и молекулы в изобилии встречаются в биологических и экологических системах, где они участвуют / влияют на биологические и химические процессы. Разработка молекулярных хемосенсоров в качестве зондов для таких аналитов - это ежегодный многомиллиардный бизнес, в котором участвуют как небольшие МСП, так и крупные фармацевтические и химические компании.

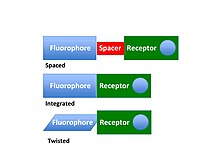
Хемосенсоры впервые были использованы для описания комбинации молекулярного распознавания с некоторой формой репортера, чтобы можно было наблюдать присутствие гостя (также называемого аналитом, см. Выше). Хемосенсоры предназначены для того, чтобы содержать сигнальный фрагмент и фрагмент молекулярного распознавания (также называемый сайтом связывания или рецептором). Комбинирование обоих этих компонентов может быть достигнуто несколькими способами, например интегрированными, скрученными или разнесенными. Хемосенсоры считаются основным компонентом области молекулярной диагностики в рамках дисциплины супрамолекулярной химии , которая основана на молекулярном распознавании . С точки зрения супрамолекулярной химии, хемосенсинг является примером химии хозяин-гость , где присутствие гостя (аналита) на участке хозяина (сенсор) вызывает событие распознавания (например, зондирование), которое можно отслеживать в режиме реального времени. . Это требует связывания анализируемого вещества с рецептором с использованием всех видов связывающих взаимодействий, таких как водородные связи , дипольные и электростатические взаимодействия , сольвофобный эффект, хелатирование металлов и т. Д. Фрагмент распознавания / связывания отвечает за селективность и эффективное связывание гость / аналит, которые зависят от топологии лиганда, характеристик мишени (ионный радиус, размер молекулы, хиральность, заряд, координационное число и жесткость и т. д.) и природы растворителя (pH, ионная сила, полярность). Хемосенсоры обычно разрабатываются так, чтобы иметь возможность обратимого взаимодействия с целевыми видами, что является предпосылкой для непрерывного мониторинга.

Методы оптической сигнализации (такие как флуоресценция ) чувствительны и селективны и обеспечивают платформу для ответа в реальном времени и местного наблюдения. Поскольку хемосенсоры предназначены как для нацеливания (т.е. могут распознавать и связывать определенные виды), так и для чувствительности к различным диапазонам концентраций, их можно использовать для наблюдаемых реальных событий на клеточном уровне. Поскольку каждая молекула может вызывать сигнал / считывание, которое может быть выборочно измерено, хемосенсоры часто называют неинвазивными и, следовательно, привлекают значительное внимание своим применением в биологической материи, например, в живых клетках. Было разработано множество примеров хемосенсоров для наблюдения за клеточными функциями и свойствами, включая мониторинг концентраций ионного потока и транспорта внутри клеток, таких как Ca (II), Zn (II), Cu (II) и другие физиологически важные катионы и анионы, а также биомолекулы.
Дизайн лигандов для селективного распознавания подходящих гостей, таких как катионы и анионы металлов , является важной целью супрамолекулярной химии. Термин супрамолекулярная аналитическая химия недавно был придуман для описания применения молекулярных сенсоров в аналитической химии. Сенсоры на малых молекулах относятся к хемосенсорам. Однако они традиционно считаются структурно простыми молекулами и отражают необходимость образования хелатирующих молекул для комплексообразования ионов в аналитической химии.
История
Хотя хемосенсоры были впервые определены в 1980-х годах, первым примером такого флуоресцентного хемосенсора может быть документ Фридриха Гоппельсродера , который в 1867 году разработал метод определения / восприятия иона алюминия с использованием флуоресцентного лиганда / хелата. Эта и последующие работы других авторов породили то, что считается современной аналитической химией.
В 1980-х годах разработка хемосенсинга была достигнута Энтони В. Чарник, А. Прасанна де Сильва и Роджер Циен , которые разработали различные типы люминесцентных зондов для ионов и молекул в растворах и внутри биологических клеток для приложений в реальном времени. Цзянь продолжал изучать и развивать эту область исследований, разрабатывая и изучая флуоресцентные белки для применения в биологии, такие как зеленые флуоресцентные белки (GFP), за что он был удостоен Нобелевской премии по химии в 2008 году. Работа Линн Соуза в в конце 1970-х годов, по обнаружению ионов щелочных металлов, что, возможно, привело к одному из первых примеров использования супрамолекулярной химии в дизайне флуоресцентных датчиков, а также у Ж.-М. Лен , Х. Буа-Лоран и его сотрудники из Университета Бордо I, Франция. Разработка ПЭТ-зондирования ионов переходных металлов была разработана, в частности, Л. Фаббрицци.
В хемосенсинге использование флуорофора, связанного с рецептором через ковалентный спейсер, теперь обычно называют принципом флуорофор-спейсер-рецептор. В таких системах событие восприятия обычно описывается как происходящее из-за изменений фотофизических свойств хемосенсорных систем из-за механизмов повышенной флуоресценции, индуцированной хелатированием (CHEF), и фотоиндуцированного переноса электронов (PET). В принципе, эти два механизма основаны на одной идее; Путь коммуникации представляет собой передачу электронов через пространство от рецепторов, богатых электронами, к флуорофорам с дефицитом электронов (через пространство). Это приводит к тушению флуоресценции (активный перенос электронов), и излучение хемосенсора «отключается» для обоих механизмов в отсутствие аналитов. Однако при образовании комплекса хозяин-гость между анализируемым веществом и рецептором коммуникационный путь нарушается, и эмиссия флуоресценции флуорофоров усиливается или «включается». Другими словами, интенсивность флуоресценции и квантовый выход увеличиваются при распознавании аналита.

Рецептор флуорофоров также может быть интегрирован в хемосенсор. Это приводит к изменению длины волны излучения, что часто приводит к изменению цвета. Когда событие восприятия приводит к формированию сигнала, видимого невооруженным глазом, такие датчики обычно называют колориметрическими . Было разработано множество примеров колориметрических хемосенсоров для таких ионов, как фторид . Индикатор pH можно рассматривать как колориметрические хемосенсоры для протонов. Такие сенсоры были разработаны для других катионов, а также для анионов и более крупных органических и биологических молекул, таких как белки и углеводы.
Принципы дизайна
Хемосенсоры представляют собой молекулы наноразмеров и для применения in vivo должны быть нетоксичными. Хемосенсор должен быть способен подавать измеримый сигнал в прямом ответе на распознавание аналита. Следовательно, реакция на сигнал напрямую связана с величиной события восприятия (и, в свою очередь, концентрацией аналита). В то время как сигнальный фрагмент действует как преобразователь сигнала, преобразовывая событие распознавания в оптический ответ. Фрагмент распознавания отвечает за связывание с аналитом селективным и обратимым образом. Если сайты связывания представляют собой «необратимые химические реакции», индикаторы описываются как флуоресцентные хемодозиметры или флуоресцентные зонды .
Чтобы датчик работал, между двумя частями должен быть открыт активный канал связи. В колориметрических хемосенсорах это обычно зависит от структурной интеграции рецептора и преобразователя. При люминесцентном / флуоресцентном химиочувствении эти две части могут быть «разнесены» или соединены ковалентным спейсером. Для таких флуоресцентных хемосенсоров связь осуществляется посредством переноса электронов или энергии . Эффективность распознавания хозяина и гостя между рецептором и аналитом зависит от нескольких факторов, включая дизайн рецепторного фрагмента, цель которого состоит в том, чтобы максимально соответствовать природе структурной природы целевого аналита, а также природа среды, в которой происходит событие зондирования (например, тип среды, например, кровь, слюна, моча и т. д. в биологических образцах). Расширением этого подхода является разработка молекулярных маяков , которые представляют собой зонды гибридизации олигонуклеотидов, основанные на передаче сигналов флуоресценции, где событие распознавания или восприятия передается через усиление или уменьшение люминесценции за счет использования механизма резонансной передачи энергии Ферстера (FRET).
Флуоресцентный химиочувствительный
Все хемосенсоры сконструированы так, чтобы содержать сигнальный фрагмент и фрагмент распознавания. Они интегрированы напрямую или связаны с коротким ковалентным спейсером в зависимости от механизма, участвующего в сигнальном событии. Хемосенсор может быть основан на самосборке сенсора и анализируемого вещества. Примером такой конструкции являются (индикаторные) тесты смещения IDA. Датчик IDA для анионов, таких как ионы цитрата или фосфата, был разработан, посредством чего эти ионы могут вытеснять флуоресцентный индикатор в комплексе индикатор-хозяин. Так называемый вкусный чип UT (Техасский университет) представляет собой прототип электронного языка и сочетает в себе супрамолекулярную химию с устройствами с зарядовой связью на основе кремниевых пластин и иммобилизованных рецепторных молекул.
Большинство примеров хемосенсоров для ионов , таких как ионы щелочных металлов (Li +, Na +, K + и т. Д.) И ионов щелочноземельных металлов (Mg2 +, Ca2 + и т. Д.), Спроектированы таким образом, что возбужденное состояние флуорофорного компонента хемосенсор подавляется переносом электронов, когда сенсор не образует комплекс с этими ионами. Таким образом, эмиссии не наблюдается, и датчик иногда называют «выключенным». Путем объединения сенсора с катионом условия переноса электронов изменяются так, что процесс гашения блокируется, и флуоресцентная эмиссия «включается». Вероятность ПЭТ определяется общей свободной энергией системы ( свободная энергия Гиббса ΔG). Движущая сила для ПЭТ представлена ΔGET, общие изменения свободной энергии для переноса электронов можно оценить с помощью уравнения Рема-Веллера. Перенос электронов зависит от расстояния и уменьшается с увеличением длины спейсера. Тушение переносом электрона между незаряженными частицами приводит к образованию ион-радикальной пары. Иногда это называют первичным переносом электрона. Возможный перенос электронов, который происходит после ПЭТ, называется «вторичным переносом электронов». Тушение усиления хелатирования (CHEQ) - это противоположный эффект, наблюдаемый для CHEF. В CHEQ наблюдается снижение флуоресцентного излучения хемосенсора по сравнению с тем, которое наблюдалось первоначально для «свободного» сенсора при образовании хозяин-гость. Поскольку перенос электронов является направленным, такие системы также были описаны с помощью принципа ПЭТ, описываемого как усиление ПЭТ от рецептора к флуорофору с повышенной степенью тушения. Такой эффект был продемонстрирован для определения анионов, таких как карбоксилаты и фториды.
Большое количество примеров хемосенсоров было разработано учеными в области физических наук, наук о жизни и окружающей среды. Преимущества того, что флуоресцентное излучение «включается» или «выключается» после события распознавания, позволяет сравнивать хемосенсоры с «ночными маяками». Поскольку процесс обратим, увеличение выбросов зависит от концентрации и становится «насыщенным» только при высоких концентрациях (полностью связанный рецептор). Следовательно, можно установить корреляцию между люминесценцией (интенсивностью, квантовым выходом и в некоторых случаях временем жизни) и концентрацией аналита. Благодаря тщательному проектированию и оценке характера канала связи были разработаны аналогичные датчики, основанные на использовании переключения «вкл-выкл», «вкл-выкл-вкл» или «выкл-вкл-выкл». Встраивание хемосенсоров на поверхности, такие как квантовые точки , наночастицы или в полимеры , также является быстрорастущей областью исследований. Другие примеры хемосенсоров, которые работают по принципу включения или выключения флуоресцентного излучения, включают резонансный перенос энергии Фёрстера (FRET), внутренний перенос заряда (ICT), скрученный внутренний перенос заряда (TICT), излучение на основе металлов (например, в люминесценция лантаноидов), эксимерная и эксиплексная эмиссия и эмиссия, индуцированная агрегацией (AIE). Хемосенсоры были одним из первых примеров молекул, которые могли переключаться между состояниями `` включено '' и `` выключено '' с помощью внешних стимулов, и как таковые могут быть классифицированы как синтетическая молекулярная машина , которой была присуждена Нобелевская премия по химии. в 2016 году Жан-Пьеру Соважу , Фрейзеру Стоддарту и Бернару Л. Феринге .
Применение тех же принципов проектирования, которые использовались в хемосенсинге, также проложило путь для разработки имитаторов молекулярных логических вентилей (MLGM), которые были впервые предложены с использованием флуоресцентных хемосенсоров на основе ПЭТ де Сильва и его коллегами в 1993 году. Молекулы были созданы для работы в соответствии с булевой алгеброй, которая выполняет логическую операцию на основе одного или нескольких физических или химических входов. Эта область продвинулась от разработки простых логических систем, основанных на одном химическом вводе, до молекул, способных выполнять сложные и последовательные операции.
Применение хемосенсоров

Хемосенсоры были включены посредством функционализации поверхности в частицы и шарики, такие как наночастицы на основе металлов , квантовые точки , частицы на основе углерода, а также в мягкие материалы, такие как полимеры, для облегчения их различных применений.
Другие рецепторы чувствительны не к конкретной молекуле, а к классу молекулярных соединений, эти хемосенсоры используются в сенсорах на основе матрицы (или микроматрицы). Датчики на основе матриц используют связывание аналита дифференциальными рецепторами. Одним из примеров является групповой анализ нескольких дубильных кислот, которые накапливаются при выдерживании шотландского виски в дубовых бочках. Сгруппированные результаты продемонстрировали корреляцию с возрастом, но отдельные компоненты - нет. Аналогичный рецептор можно использовать для анализа тартратов в вине.
Применение хемосенсоров в визуализации клеток особенно многообещающе, так как большинство биологических процессов в настоящее время контролируется с помощью таких технологий визуализации, как конфокальная флуоресценция и микроскопия сверхвысокого разрешения , среди прочих.
Составной сакситоксин - это нейротоксин, содержащийся в моллюсках, и химическое оружие. Экспериментальный датчик для этого соединения снова основан на ПЭТ. Взаимодействие сакситоксина с краун-эфирным фрагментом сенсора убивает его ПЭТ-процесс в направлении флуорофора, и флуоресценция переключается с выключенной на включенную. Необычный фрагмент бора гарантирует, что флуоресценция происходит в видимой световой части электромагнитного спектра.
Смотрите также
- Бороновые кислоты в супрамолекулярной химии: распознавание сахаридов
- Химия между хозяином и гостем
- Молекулярная машина
- Молекулярное распознавание