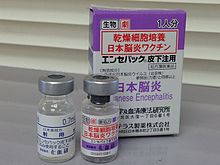
Японский энцефалит - Japanese encephalitis
| японский энцефалит | |
|---|---|
| Другие имена | Японский энцефалит типа B |
 | |
| Географическое распространение японского энцефалита (темно-зеленый) | |
| Специальность | Инфекционное заболевание |
| Симптомы | Головная боль, лихорадка, рвота, спутанность сознания, судороги |
| Обычное начало | От 5 до 15 дней после заражения |
| Причины | Вирус японского энцефалита (распространяется комарами) |
| Диагностический метод | Кровь или спинномозговой жидкости тестирование |
| Профилактика | Вакцина против японского энцефалита , предотвращающая укусы комаров |
| Уход | Поддерживающая терапия |
| Прогноз | Постоянные неврологические проблемы возникают почти у половины выживших. |
| Частота | 68 000 |
| Летальные исходы | 17 000 |
Японский энцефалит ( ЯЭ ) - это инфекция головного мозга, вызываемая вирусом японского энцефалита (ЯЭ). В то время как большинство инфекций практически не проявляются или не проявляются никакими симптомами, время от времени возникает воспаление головного мозга . В этих случаях симптомы могут включать головную боль, рвоту, лихорадку, спутанность сознания и судороги . Это происходит примерно через 5-15 дней после заражения.
ЯВЭ обычно передается комарами , особенно комарами типа Culex . Свиньи и дикие птицы служат резервуаром для вируса. Заболевание чаще всего встречается за пределами городов. Диагноз ставится на основании анализа крови или спинномозговой жидкости .
Профилактика обычно осуществляется с помощью вакцины против японского энцефалита , которая одновременно безопасна и эффективна. Другие меры включают предотвращение укусов комаров. В случае заражения специфического лечения не существует, только с осторожностью . Обычно это проводится в больнице. Постоянные проблемы возникают почти у половины людей, выздоравливающих от ЯЭ.
Заболевание встречается в Юго-Восточной Азии и Западной части Тихого океана . Около 3 миллиардов человек проживают в районах, где наблюдается заболевание. Ежегодно происходит около 68 000 симптоматических случаев, из которых около 17 000 умирают. Часто случаи заболевания возникают в виде вспышек . Заболевание впервые было описано в Японии в 1871 году . Несмотря на свое название, в настоящее время это заболевание относительно редко встречается в Японии в результате широкомасштабных усилий по иммунизации.
Признаки и симптомы
Инкубационный период вируса японского энцефалита (JEV) составляет от 2 до 26 дней. Подавляющее большинство инфекций протекает бессимптомно : только 1 из 250 случаев перерастает в энцефалит.
Тяжелое озноб может означать начало этого заболевания у людей. Лихорадка, головная боль и недомогание - другие неспецифические симптомы этого заболевания, которые могут длиться от 1 до 6 дней. Признаки, которые развиваются во время острой стадии энцефалита, включают ригидность шеи, кахексию , гемипарез , судороги и повышение температуры тела между 38–41 ° C (100,4–105,8 ° F). Обычно развивается умственная отсталость . Смертность от этого заболевания варьируется, но обычно выше у детей. Отмечено трансплацентарное распространение. У пациентов с поражением центральной нервной системы могут возникать пожизненные неврологические дефекты, такие как глухота, эмоциональная лабильность и гемипарез . В известных случаях некоторые эффекты также включают тошноту, головную боль, лихорадку и рвоту.
Было обнаружено, что повышенная активация микроглии после инфекции японского энцефалита влияет на исход вирусного патогенеза. Микроглия - это резидентные иммунные клетки центральной нервной системы (ЦНС), которые играют решающую роль в защите хозяина от вторжения микроорганизмов. Активированная микроглия секретирует цитокины, такие как интерлейкин-1 (IL-1) и фактор некроза опухоли альфа (TNF-α) , которые могут вызывать токсические эффекты в головном мозге. Кроме того, другие растворимые факторы, такие как нейротоксины , возбуждающие нейротрансмиттеры , простагландин , реактивный кислород и азот, секретируются активированной микроглией.
В мышиной модели JE, было обнаружено , что в гиппокампе и стриатуме , количество активированных микроглии было больше , чем где - либо в мозге, внимательно следили за тем , что в таламус . В коре количество активированной микроглии было значительно меньше по сравнению с другими областями мозга мыши . Также наблюдалась общая индукция дифференциальной экспрессии провоспалительных цитокинов и хемокинов из разных областей мозга во время прогрессирующей инфекции японского энцефалита.
Хотя чистым эффектом провоспалительных медиаторов является уничтожение инфекционных организмов и инфицированных клеток, а также стимуляция выработки молекул, которые усиливают нарастающую реакцию на повреждение, также очевидно, что в нерегенерирующем органе, таком как мозг, нарушается регуляция врожденного иммунный ответ был бы вредным. При ЯЭ, по-видимому, нарушается жесткая регуляция активации микроглии, что приводит к аутотоксической петле активации микроглии, которая, возможно, приводит к случайному повреждению нейронов. У животных ключевые признаки включают бесплодие и аборт у свиней, неврологические заболевания у лошадей и системные признаки, включая лихорадку, летаргию и анорексию.
Причина
Это заболевание , вызываемое комары -borne вирусом японского энцефалита (JEV).
Вирусология
| Вирус японского энцефалита | |
|---|---|

|
|
| Структура и геном флавивируса | |
|
Классификация вирусов |
|
| (без рейтинга): | Вирус |
| Царство : | Рибовирия |
| Королевство: | Орторнавиры |
| Тип: | Kitrinoviricota |
| Класс: | Flasuviricetes |
| Порядок: | Амарилловиралес |
| Семья: | Flaviviridae |
| Род: | Флавивирус |
| Разновидность: |
Вирус японского энцефалита
|
JEV представляет собой вирус из семейства Flaviviridae , часть серокомплекса японского энцефалита из 9 генетически и антигенно связанных вирусов, некоторые из которых особенно опасны для лошадей , а четыре, как известно, заражают людей, включая вирус Западного Нила . Окутанный вирус тесно связан с вирусом Западного Нила и в Сент - Луисе энцефалит вируса. Геном одноцепочечной РНК с положительным смыслом упакован в капсид, который образован капсидным белком. Внешняя оболочка образована белком оболочки и является защитным антигеном. Это способствует проникновению вируса в клетку. Геном также кодирует несколько неструктурных белков (NS1, NS2a, NS2b, NS3, N4a, NS4b, NS5). NS1 также производится в виде секреторной формы. NS3 - это предполагаемая геликаза , а NS5 - вирусная полимераза . Было отмечено , что японский энцефалит заражает просвет на эндоплазматический ретикулум (ER) и быстро накапливает значительное количество вирусных белков.
На основе гена оболочки различают пять генотипов (I – V). Штамм Muar, выделенный от пациента в Малайе в 1952 году, является прототипом штамма генотипа V. Генотип IV, по-видимому, является наследственным штаммом, и вирус, по-видимому, развился в индонезийско-малазийском регионе. Первые клинические отчеты датируются 1870 годом, но вирус, по-видимому, эволюционировал в середине 16 века. К 2010 году было секвенировано более шестидесяти полных геномов этого вируса.
Диагностика
Японский энцефалит диагностируется с помощью имеющихся в продаже тестов, выявляющих специфические IgM-антитела к вирусу JE в сыворотке и / или спинномозговой жидкости , например, с помощью ELISA с захватом IgM .
Антитела IgM к вирусу ЯЭ обычно обнаруживаются через 3–8 дней после начала заболевания и сохраняются в течение 30–90 дней, но документально подтверждено более длительное их существование. Следовательно, положительные антитела IgM иногда могут отражать перенесенную инфекцию или вакцинацию. Сыворотка, собранная в течение 10 дней после начала заболевания, может не содержать определяемых IgM, и тест следует повторить на образце выздоравливающего. Пациентам с антителами IgM к вирусу ЯЭ необходимо провести подтверждающее тестирование на нейтрализующие антитела. Подтверждающее тестирование в США доступно только в CDC и нескольких специализированных справочных лабораториях. В смертельных случаях могут быть полезны амплификация нуклеиновых кислот и культивирование вирусов из тканей аутопсии. Вирусный антиген может быть обнаружен в тканях путем непрямого флуоресцентного окрашивания антител .
Профилактика
Заражение японским энцефалитом дает пожизненный иммунитет . В настоящее время доступны три вакцины : SA14-14-2, IXIARO (IC51, также продается в Австралии, Новой Зеландии как JESPECT и в Индии как JEEV) и ChimeriVax-JE (продается как IMOJEV). Все современные вакцины основаны на вирусе генотипа III.
Формалина -inactivated мыши мозг , полученная вакцина впервые была выпущена в Японии в 1930 - х годах и была утверждена для использования в Тайване в 1960 - х и в Таиланде в 1980 - х годах. Широкое использование вакцины и урбанизация привели к борьбе с болезнью в Японии, Корее, Тайване и Сингапуре. Высокая стоимость этой вакцины, выращиваемой на живых мышах, означает, что более бедные страны не могут позволить себе вводить вакцину в рамках плановой программы иммунизации.
Наиболее частые побочные эффекты - покраснение и боль в месте укола. В редких случаях крапивница может развиться примерно через четыре дня после инъекции. Вакцины, произведенные из мозга мышей, имеют риск аутоиммунных неврологических осложнений около 1 на миллион вакцинаций. Однако там, где вакцина производится не в мозге мышей, а in vitro с использованием клеточных культур , побочных эффектов мало по сравнению с плацебо , основными побочными эффектами являются головная боль и миалгия .
Нейтрализующее антитело сохраняется в кровотоке не менее двух-трех лет, а возможно и дольше. Общая продолжительность защиты неизвестна, но поскольку нет убедительных доказательств того, что защита превышает три года, ревакцинации рекомендуется каждые три года для людей, которые остаются в группе риска. Кроме того, отсутствуют данные относительно взаимозаменяемости других вакцин против ЯЭ и IXIARO.
Уход
Специфического лечения японского энцефалита не существует, и лечение является поддерживающим, с помощью, при необходимости, для кормления , дыхания или контроля судорог . Повышенное внутричерепное давление можно контролировать с помощью маннита . Передача от человека к человеку не передается, поэтому нет необходимости изолировать пациентов.
Прорыв в области лечения японского энцефалита - это идентификация участия рецепторов макрофагов в степени тяжести заболевания. Недавний отчет индийской группы демонстрирует участие моноцитарного и макрофагального рецептора CLEC5A в тяжелой воспалительной реакции при инфекции мозга японским энцефалитом. Это транскриптомное исследование дает гипотезу о нейровоспалении и является новым лидером в разработке подходящих методов лечения японского энцефалита.
Эффективность внутривенного иммуноглобулина для лечения энцефалита неясна из-за отсутствия доказательств. Внутривенный иммуноглобулин при японском энцефалите не принес никакой пользы.
Эпидемиология
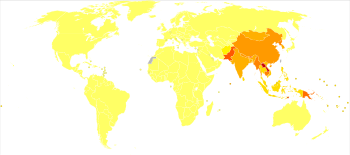
Японский энцефалит (ЯЭ) является основной причиной вирусного энцефалита в Азии , ежегодно регистрируется до 70 000 случаев. Летальность составляет от 0,3% до 60% и зависит от населения и возраста. Также имели место редкие вспышки на территориях США в западной части Тихого океана. Жители сельской местности в эндемичных регионах подвергаются наибольшему риску; Японский энцефалит обычно не встречается в городских районах.
Страны, в которых в прошлом были крупные эпидемии, но которые контролировали болезнь в основном с помощью вакцинации, включают Китай , Южную Корею , Японию , Тайвань и Таиланд . Другие страны, в которых все еще наблюдаются периодические эпидемии, включают Вьетнам , Камбоджу , Мьянму , Индию , Непал и Малайзию . Японский энцефалит был зарегистрирован на островах Торресова пролива , и два смертельных случая были зарегистрированы на материковой части северной Австралии в 1998 году. В 2013 году были зарегистрированы случаи заболевания в штате Качин , Мьянма. Распространение вируса в Австралии вызывает особую озабоченность в области здравоохранения Австралии. чиновников из-за незапланированного завоза Culex gelidus , потенциального переносчика вируса, из Азии. Однако в настоящее время присутствие на материковой части Австралии минимально. В 2016 году в отсталом районе Малкангири в Индии было зарегистрировано 116 смертей .
Человек, крупный рогатый скот и лошади являются тупиковыми хозяевами, поскольку болезнь проявляется как фатальный энцефалит. Свиньи действуют как усиливающийся хозяин и играют очень важную роль в эпидемиологии болезни. Инфекция у свиней протекает бессимптомно, за исключением беременных свиноматок, когда частыми последствиями являются аборт и аномалии развития плода. Наиболее важным переносчиком является Culex tritaeniorhynchus , который питается крупным рогатым скотом, а не человеком. Естественными хозяевами вируса японского энцефалита являются птицы, а не люди, и многие считают, что вирус никогда не будет полностью уничтожен. В ноябре 2011 г. вирус японского энцефалита был зарегистрирован у Culex bitaeniorhynchus в Южной Корее .
Недавно исследование полногеномных микрочипов нейронов, инфицированных вирусом японского энцефалита, показало, что нейроны играют важную роль в их собственной защите от инфекции японского энцефалита. Хотя это ставит под сомнение устоявшееся убеждение, что нейроны иммунологически неактивны, улучшенное понимание провоспалительных эффектов, ответственных за иммуноопосредованный контроль вирусной инфекции и повреждение нейронов во время инфекции японского энцефалита, является важным шагом для разработки стратегий ограничения тяжести поражения ЦНС. болезнь.
Был исследован ряд лекарств для уменьшения репликации вирусов или обеспечения нейрозащиты в клеточных линиях или исследованиях на мышах. В настоящее время ни один из них не рекомендуется для лечения пациентов-людей.
- Использование розмариновой кислоты , арктигенина и олигосахаридов со степенью полимеризации 6 из Gracilaria sp. или Monostroma nitidum, как было показано, эффективен на мышиной модели японского энцефалита.
- В исследовании in vitro было показано, что куркумин оказывает нейрозащитное действие против инфекции японского энцефалита. Куркумин, возможно, действует, снижая уровень активных форм кислорода в клетках, восстанавливая целостность клеточной мембраны , уменьшая проапоптотические сигнальные молекулы и модулируя клеточные уровни белков, связанных со стрессом. Также было показано, что продукция инфекционных вирусных частиц из ранее инфицированных клеток нейробластомы снижается, что достигается за счет ингибирования системы убиквитин-протеасома .
- Миноциклин у мышей приводил к заметному снижению уровней некоторых маркеров, вирусного титра и уровня провоспалительных медиаторов, а также предотвращал повреждение гематоэнцефалического барьера .
Эволюция
Вирус, по-видимому, произошел от своего предкового вируса в середине 1500-х годов в регионе Индонезия-Малайзия и развился там в пять различных генотипов, которые распространились по Азии. Средняя скорость эволюции была оценена как 4,35 × 10 -4 (диапазон: от 3,49 × 10 -4 до 5,30 × 10 -4 ) нуклеотидных замен на сайт в год.
использованная литература
внешние ссылки
- «Вопросы и ответы о японском энцефалите» . Центры по контролю и профилактике заболеваний.
- «Японский энцефалит» . Департамент здравоохранения и старения правительства Австралии. 2012 г.
- Рамзи, Мэри, изд. (2020). «20. Японский энцефалит» . Иммунизация против инфекционного заболевания . Зеленая книга. Общественное здравоохранение Англии.
- «Библиотека ресурсов по японскому энцефалиту» .
- Heffelfinger JD, Li X, Batmunkh N, Grabovac V, Diorditsa S, Liyanage JB, Pattamadilok S, Bahl S, Vannice KS, Hyde TB, Chu SY, Fox KK, Hills SL, Marfin AA (9 июня 2017 г.). «Эпиднадзор за японским энцефалитом и иммунизация - регионы Азии и Западной части Тихого океана, 2016 г.» . MMWR Morb Mortal Wkly Rep . 66 (22): 579–583. DOI : 10,15585 / mmwr.mm6622a3 . PMC 5720240 . PMID 28594790 . Ошибка в: MMWR Morb Mortal Wkly Rep. 23 июня 2017 г .; 66 (24): 653.
- Саймон, LV; Крузе, Б. (январь 2018 г.). Энцефалит, японский . FL: StatPearls Publishing. PMID 29262148 . NBK470423.
| Классификация | |
|---|---|
| Внешние ресурсы |