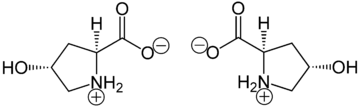
Гидроксипролин - Hydroxyproline
|
|
| Имена | |
|---|---|
|
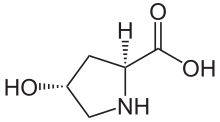
Название ИЮПАК
(2 S , 4 R ) -4-гидроксипирролидин-2-карбоновая кислота
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.000.084 |
| MeSH | Гидроксипролин |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| C 5 H 9 N O 3 | |
| Молярная масса | 131,131 г · моль -1 |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
(2 S , 4 R ) -4-гидроксипролин или L- гидроксипролин ( C 5 H 9 O 3 N ) представляет собой аминокислоту , сокращенно Hyp или O , например , в банке данных по белкам .
Структура и открытие
В 1902 году Герман Эмиль Фишер выделил гидроксипролин из гидролизованного желатина . В 1905 году Герман Лейкс синтезировал рацемическую смесь 4-гидроксипролина.
Гидроксипролин отличается от пролина наличием гидроксильной (ОН) группы, присоединенной к гамма-атому углерода.
Производство и функции
Гидроксипролин продуцируется путем гидроксилирования аминокислоты пролина ферментом пролилгидроксилазой после синтеза белка (как посттрансляционная модификация ). Фермента катализируемой реакция происходит в просвет в эндоплазматический ретикулум . Хотя гидроксипролин непосредственно не включается в белки, он составляет примерно 4% всех аминокислот, обнаруженных в тканях животных, то есть больше, чем семь других аминокислот, которые включены трансляционно.
Животные
Коллаген
Гидроксипролин является основным компонентом белкового коллагена , составляющего примерно 13,5% коллагена млекопитающих. Гидроксипролин и пролин играют ключевую роль в стабильности коллагена. Они позволяют резкое закручивание спирали коллагена. В канонической триаде коллагена Xaa-Yaa-Gly (где Xaa и Yaa - любая аминокислота) пролин, занимающий положение Yaa, гидроксилируется с образованием последовательности Xaa-Hyp-Gly. Эта модификация остатка пролина увеличивает стабильность тройной спирали коллагена . Первоначально предполагалось, что стабилизация происходит из-за молекул воды, образующих сеть водородных связей, связывающую пролильные гидроксильные группы и карбонильные группы основной цепи. Впоследствии было показано, что повышение стабильности происходит, прежде всего, за счет стереоэлектронных эффектов и что гидратация остатков гидроксипролина обеспечивает небольшую дополнительную стабильность или ее отсутствие.
Без коллагена
Помимо коллагена белки млекопитающих эластин и аргонавт 2 имеют коллагеноподобные домены, в которых образуется гидроксипролин. Некоторые яды улиток, конотоксины , содержат гидроксипролин, но не имеют коллагеноподобных последовательностей.
Было показано, что гидроксилирование пролина участвует в нацеливании на альфа-субъединицу гипоксии-индуцируемого фактора (HIF) (HIF-1 альфа) для деградации путем протеолиза . Под нормоксии (нормальные условия кислорода) EGLN1 [1] Белок гидроксилаты пролин на 564 позиции HIF-1 альфа, который позволяет убиквитилирование по супрессора фон Хиппель-Линдау опухоли (pVHL) и последующего нацеливания для протеасомы деградации.
Гидроксипролин содержится в немногих белках, кроме коллагена. По этой причине содержание гидроксипролина использовалось в качестве индикатора для определения количества коллагена и / или желатина .
Растения
Гликопротеины, богатые гидроксипролином (HRGP), также обнаруживаются в стенках растительных клеток . Эти гидроксипролины служат точками присоединения гликановых цепей, которые добавляются в качестве посттрансляционных модификаций .
Клиническое значение
Для гидроксилирования пролина требуется аскорбиновая кислота ( витамин С ). Наиболее очевидные первые эффекты (проблемы с деснами и волосами) отсутствия аскорбиновой кислоты у людей возникают из-за возникающего в результате нарушения гидроксилирования пролиновых остатков коллагена с пониженной стабильностью молекулы коллагена, что приводит к цинге .
Повышенные уровни гидроксипролина в сыворотке и моче также были продемонстрированы при болезни Педжета .
Другие гидроксипролины
Другие гидроксипролины также существуют в природе. Наиболее заметными из них являются 2,3- цис- , 3,4- транс- и 3,4-дигидроксипролин, который встречается в клеточных стенках диатомовых водорослей и, как предполагается, играет роль в отложении кремнезема . Гидроксипролин также содержится в стенках оомицетов , грибовидных протистов, относящихся к диатомовым водорослям. (2 S , 4 S ) - цис- 4-гидроксипролин содержится в токсичных циклических пептидах грибов Amanita ( например , фаллоидине ).