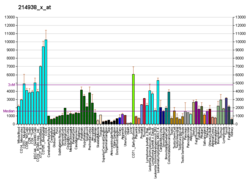
HMGB1 - HMGB1
Высокая мобильность группа коробка 1 белок, также известный как высокая мобильность группы белок 1 (ГМГ-1) и amphoterin , является белком , который в организме человека кодируется HMGB1 геном .
HMG-1 принадлежит к группе высокой мобильности и содержит домен HMG-бокса .
Функция
Как и гистоны , HMGB1 является одним из наиболее важных белков хроматина. В ядре HMGB1 взаимодействует с нуклеосомами , факторами транскрипции и гистонами . Этот ядерный белок организует ДНК и регулирует транскрипцию. После связывания HMGB1 изгибает ДНК , что облегчает связывание других белков. HMGB1 поддерживает транскрипцию многих генов во взаимодействии со многими факторами транскрипции. Он также взаимодействует с нуклеосомами, чтобы ослабить упакованную ДНК и реконструировать хроматин. Контакт с коровыми гистонами изменяет структуру нуклеосом.
Присутствие HMGB1 в ядре зависит от посттрансляционных модификаций. Когда белок не ацетилирован, он остается в ядре, но гиперацетилирование остатков лизина заставляет его перемещаться в цитозоль.
HMGB1 было показано, играет важную роль в оказании помощи эндонуклеазы RAG образует комплекс в паре во время V (D) J рекомбинация .
Роль в воспалении
HMGB1 секретируется иммунными клетками (такими как макрофаги , моноциты и дендритные клетки ) через секреторный путь без лидера . Активированные макрофаги и моноциты секретируют HMGB1 как цитокиновый медиатор воспаления . Антитела, нейтрализующие HMGB1, обеспечивают защиту от повреждения и повреждения тканей при артрите , колите , ишемии , сепсисе , эндотоксемии и системной красной волчанке . Механизм воспаления и повреждения заключается в связывании с TLR2 и TLR4 , которое опосредует HMGB1-зависимую активацию высвобождения цитокинов макрофагами. Это позиционирует HMGB1 на пересечении стерильных и инфекционных воспалительных реакций.
АДФ-рибозилирование HMGB1 с помощью PARP1 ингибирует удаление апоптотических клеток, тем самым поддерживая воспаление. Связывание TLR4 с помощью HMGB1 или LPS ( липополисахарида ) поддерживает ADP-рибозилирование HMGB1 с помощью PARP1, тем самым служа петлей амплификации для воспаления.
HMGB1 был предложен в качестве адъюванта ДНК-вакцины . Было продемонстрировано, что HMGB1, высвобождаемый из опухолевых клеток, опосредует противоопухолевые иммунные ответы путем активации передачи сигналов Toll-подобного рецептора 2 (TLR2) на полученных из костного мозга GBM-инфильтрирующих DC.
Взаимодействия
HMGB1 должен взаимодействовать с p53 .
HMGB1 - это ядерный белок, который связывается с ДНК и действует как архитектурный фактор связывания хроматина. Он также может высвобождаться из клеток, в внеклеточной форме которых он может связывать воспалительный рецептор RAGE (рецептор конечных продуктов гликозилирования) и Toll-подобные рецепторы (TLR). Выделение из клеток, по-видимому, связано с двумя различными процессами: некрозом, когда клеточные мембраны проницаемы, и внутриклеточные составляющие могут диффундировать из клетки; и некоторая форма активной или облегченной секреции, индуцированной передачей сигналов через NF-κB . HMGB1 также перемещается в цитозоль в стрессовых условиях, таких как повышенное содержание АФК внутри клеток. В таких условиях HMGB1 способствует выживанию клеток, поддерживая аутофагию за счет взаимодействия с беклином-1. Он в значительной степени считается антиапоптотическим белком.
HMGB1 может взаимодействовать с лигандами и цитокинами TLR и активирует клетки через множество поверхностных рецепторов, включая TLR2 , TLR4 и RAGE.
Взаимодействие через TLR4
Некоторые действия HMGB1 опосредуются toll-подобными рецепторами (TLR) . Взаимодействие между HMGB1 и TLR4 приводит к усилению регуляции NF-κB , что приводит к увеличению продукции и высвобождения цитокинов . HMGB1 также способен взаимодействовать с TLR4 на нейтрофилах, чтобы стимулировать производство активных форм кислорода NADPH-оксидазой. Комплекс HMGB1-LPS активирует TLR4 и вызывает связывание адаптерных белков (MyD88 и другие), что приводит к передаче сигнала и активации различных сигнальных каскадов. Последующий эффект этой передачи сигналов состоит в том, чтобы активировать MAPK и NF-κB и, таким образом, вызвать продукцию воспалительных молекул, таких как цитокины.
Клиническое значение
HMGB1 был предложен в качестве мишени для лечения рака и в качестве вектора для уменьшения воспаления от инфекции SARS-CoV-2 .
Нейродегенеративный заболевание спиноцеребеллярного типа атаксии 1 (СЦА1) обусловлен мутацией в атаксине 1 ген. В мышиной модели СЦА1, мутантного белка атаксина 1 опосредованного снижение или ингибирование HMGB1 в митохондриях из нейронов . HMGB1 регулирует архитектурные изменения ДНК, необходимые для восстановления повреждений ДНК . В модели мыши SCA1 сверхэкспрессия белка HMGB1 посредством введенного вирусного вектора, несущего ген HMGB1, способствовала восстановлению повреждений митохондриальной ДНК, уменьшала невропатологию и двигательные дефекты мышей SCA1, а также увеличивала продолжительность их жизни. Таким образом, нарушение функции HMGB1, по-видимому, играет ключевую роль в патогенезе SCA1.
Недавно проведенное исследование предоставило доказательства связи между повышенным уровнем HMGB1 и вниманием к деталям и систематизацией у детей с высокофункциональным расстройством аутистического спектра (РАС), не получавшим медикаментозное лечение, предполагая, что воспалительные процессы, опосредованные HMGB1, могут играть роль в нарушении нейробиологических заболеваний. механизмы, регулирующие когнитивные процессы при РАС. В этом исследовании было обнаружено, что сывороточные концентрации HMGB1 у детей с РАС значительно выше, чем у типично развивающихся детей. Кроме того, концентрации HMGB1 в сыворотке положительно коррелировали с коэффициентом внимания к деталям (AQ) и общим баллом систематизирующего коэффициента (SQ) в группе ASD. Однако исчерпывающие данные о детях ограничены, что подчеркивает необходимость углубленных исследований для понимания возможных механизмов, связывающих HMGB1 с основными характеристиками РАС. Тем не менее было высказано предположение, что HMGB1 может быть надежным маркером воспаления, объясняющим связь между воспалительными процессами и некоторыми аутистическими чертами, и, следовательно, возможной терапевтической мишенью при этом расстройстве нервного развития.
использованная литература
дальнейшее чтение
- Томас Дж. О., Трэверс А. А. (март 2001 г.). «HMG1 и 2 и родственные« архитектурные »ДНК-связывающие белки». Направления биохимических наук . 26 (3): 167–74. DOI : 10.1016 / S0968-0004 (01) 01801-1 . PMID 11246022 .
- Андерссон У., Эрландссон-Харрис Х., Ян Х., Трейси К.Дж. (декабрь 2002 г.). «HMGB1 как ДНК-связывающий цитокин». Журнал биологии лейкоцитов . 72 (6): 1084–91. PMID 12488489 .
- Wu H, Wu T, Hua W, Dong X, Gao Y, Zhao X, Chen W, Cao W, Yang Q, Qi J, Zhou J, Wang J (март 2015 г.). «Мизопростол, агонист рецепторов PGE2, защищает мозг от внутримозгового кровоизлияния у мышей» . Нейробиология старения . 36 (3): 1439–50. DOI : 10.1016 / j.neurobiolaging.2014.12.029 . PMC 4417504 . PMID 25623334 .
- Эрландссон Харрис Х, Андерссон Ю (июнь 2004 г.). «Мини-обзор: ядерный белок HMGB1 как провоспалительный медиатор» . Европейский журнал иммунологии . 34 (6): 1503–12. DOI : 10.1002 / eji.200424916 . PMID 15162419 .
- Цзян В., Писецкий Д.С. (январь 2007 г.). «Механизмы заболевания: роль белка 1 группы высокой подвижности в патогенезе воспалительного артрита». Клиническая практика природы. Ревматология . 3 (1): 52–8. DOI : 10.1038 / ncprheum0379 . PMID 17203009 . S2CID 428632 .
- Эллерман Дж. Э., Браун С. К., де Вера М., Зе Х. Дж., Биллиар Т., Рубартелли А., Лотце М. Т. (май 2007 г.). «Маскарад: бокс-1 группы высокой мобильности и рак» . Клинические исследования рака . 13 (10): 2836–48. DOI : 10.1158 / 1078-0432.CCR-06-1953 . PMID 17504981 .
- Фоссати С., Кьяруги А. (2007). «Актуальность белкового бокса 1 группы высокой мобильности для нейродегенерации». Международный обзор нейробиологии . 82 : 137–48. DOI : 10.1016 / S0074-7742 (07) 82007-1 . ISBN 9780123739896. PMID 17678959 .
- Парккинен Дж., Раувала Х. (сентябрь 1991 г.). «Взаимодействие плазминогена и тканевого активатора плазминогена (t-PA) с амфотерином. Усиление активации плазминогена, катализируемого t-PA, амфотерином» . Журнал биологической химии . 266 (25): 16730–5. DOI : 10.1016 / S0021-9258 (18) 55362-X . PMID 1909331 .
- Вен Л., Хуанг Дж. К., Джонсон Б. Х., Рик Г. Р. (февраль 1989 г.). «Клон кДНК плаценты человека, кодирующий негистоновый хромосомный белок HMG-1» . Исследования нуклеиновых кислот . 17 (3): 1197–214. DOI : 10.1093 / NAR / 17.3.1197 . PMC 331735 . PMID 2922262 .
- Бернуес Дж., Эспель Э., Кероль Э. (май 1986 г.). «Идентификация основных связывающих гистонов доменов HMG1 и HMG2». Biochimica et Biophysica Acta (BBA) - Структура и экспрессия гена . 866 (4): 242–51. DOI : 10.1016 / 0167-4781 (86) 90049-7 . PMID 3697355 .
- Ge H, Roeder RG (июнь 1994 г.). «Белок группы высокой подвижности HMG1 может обратимо ингибировать транскрипцию гена класса II за счет взаимодействия с ТАТА-связывающим белком» . Журнал биологической химии . 269 (25): 17136–40. DOI : 10.1016 / S0021-9258 (17) 32531-0 . PMID 8006019 .
- Parkkinen J, Raulo E, Merenmies J, Nolo R, Kajander EO, Baumann M, Rauvala H (сентябрь 1993 г.). «Амфотерин, белок массой 30 кДа в семействе полипептидов HMG1-типа. Повышенная экспрессия в трансформированных клетках, передняя локализация и взаимодействие с активацией плазминогена» . Журнал биологической химии . 268 (26): 19726–38. DOI : 10.1016 / S0021-9258 (19) 36575-5 . PMID 8366113 .
- Заппавинья В., Фальциола Л., Хельмер-Читтерих М., Мавилио Ф., Бьянки М.Э. (сентябрь 1996 г.). «HMG1 взаимодействует с белками HOX и усиливает их связывание с ДНК и активацию транскрипции» . Журнал EMBO . 15 (18): 4981–91. DOI : 10.1002 / j.1460-2075.1996.tb00878.x . PMC 452236 . PMID 8890171 .
- Xiang YY, Wang DY, Tanaka M, Suzuki M, Kiyokawa E, Igarashi H, Naito Y, Shen Q, Sugimura H (февраль 1997 г.). «Экспрессия мРНК группы 1 с высокой подвижностью в аденокарциноме желудочно-кишечного тракта человека и соответствующей доброкачественной слизистой оболочке» . Международный журнал рака . 74 (1): 1–6. DOI : 10.1002 / (SICI) 1097-0215 (19970220) 74: 1 <1 :: AID-IJC1> 3.0.CO; 2-6 . PMID 9036861 .
- Расмуссен Р.К., Джи Х., Эддес Дж.С., Мориц Р.Л., Рид Г.Е., Симпсон Р.Дж., Доров Д.С. (1997). «Двумерный электрофоретический анализ белков карциномы молочной железы человека: картирование белков, которые связываются с доменом SH3 киназы смешанного происхождения MLK2». Электрофорез . 18 (3–4): 588–98. DOI : 10.1002 / elps.1150180342 . PMID 9150946 . S2CID 37336552 .
- Джаяраман Л., Мурти Н. С., Мурти К. Г., Мэнли Д. Л., Бастин М., Привес С. (февраль 1998 г.). «Белок группы высокой подвижности-1 (HMG-1) является уникальным активатором р53» . Гены и развитие . 12 (4): 462–72. DOI : 10,1101 / gad.12.4.462 . PMC 316524 . PMID 9472015 .
- Милев П., Чиба А., Херинг М., Раувала Х., Шахнер М., Ранчт Б., Марголис Р.К., Марголис РУ (март 1998 г.). «Связывание с высоким сродством и перекрывающаяся локализация нейрокана и фосфакана / протеин-тирозинфосфатазы-дзета / бета с тенасцином-R, амфотерином и связывающей гепарин молекулой, связанной с ростом» . Журнал биологической химии . 273 (12): 6998–7005. DOI : 10.1074 / jbc.273.12.6998 . PMID 9507007 .
- Нагаки С., Ямамото М., Юмото Ю., Сиракава Х., Йошида М., Тераока Х. (май 1998 г.). «Негистоновые хромосомные белки HMG1 и 2 усиливают реакцию лигирования двухцепочечных разрывов ДНК». Сообщения о биохимических и биофизических исследованиях . 246 (1): 137–41. DOI : 10.1006 / bbrc.1998.8589 . PMID 9600082 .
- Клаудио Дж.О., Лью С.К., Демпси А.А., Цукерман Э., Стюарт А.К., На Э., Аткинс Х.Л., Исков Н.Н., Хоули Р.Г. (май 1998 г.). «Идентификация меченых последовательностью транскриптов, дифференциально экспрессируемых в иерархии кроветворения человека». Геномика . 50 (1): 44–52. DOI : 10.1006 / geno.1998.5308 . PMID 9628821 .
- Буньяратанакорнкит В., Мелвин В., Прендергаст П., Альтманн М., Ронфани Л., Бьянки М.Э., Тарасевичене Л., Нордин С.К., Аллегретто Е.А., Эдвардс Д.П. (август 1998 г.). «Белки хроматина 1 и 2 группы с высокой подвижностью функционально взаимодействуют с рецепторами стероидных гормонов для усиления их связывания с ДНК in vitro и транскрипционной активности в клетках млекопитающих» . Молекулярная и клеточная биология . 18 (8): 4471–87. DOI : 10.1128 / mcb.18.8.4471 . PMC 109033 . PMID 9671457 .
- Wu H, Wu T, Han X, Wan J, Jiang C, Chen W, Lu H, Yang Q, Wang J (январь 2017 г.). «Церебропротекция нейрональным рецептором PGE2 EP2 после внутримозгового кровоизлияния у мышей среднего возраста» . Журнал мозгового кровотока и метаболизма . 37 (1): 39–51. DOI : 10.1177 / 0271678X15625351 . PMC 5363749 . PMID 26746866 .
- Цзяо И, Ван ХК, Фань СДж (декабрь 2007 г.). «Подавление роста и повышение радиочувствительности с помощью HMGB1 при раке груди» . Acta Pharmacologica Sinica . 28 (12): 1957–67. DOI : 10.1111 / j.1745-7254.2007.00669.x . PMID 18031610 .
- Андерссон Ю., Оттестад В., Трейси К.Дж. (май 2020 г.). «Внеклеточный HMGB1: терапевтическая мишень при тяжелом воспалении легких, включая COVID-19?» . Mol Med . 26 (1): 42 (2020). DOI : 10,1186 / s10020-020-00172-4 . PMC 7203545 . PMID 32380958 .
внешние ссылки
- HMGB1 + белок, + человек по медицинским предметным рубрикам Национальной медицинской библиотеки США (MeSH)
- Исследование рака поджелудочной железы и сигнальный путь HMGB1
- PDBe-KB предоставляет обзор всей структурной информации, доступной в PDB для человеческого белка группы высокой мобильности B1 (HMGB1)
- PDBe-KB предоставляет обзор всей структурной информации, доступной в PDB для белка B1 группы высокой мобильности крыс (HMGB1)