Фтор -Fluorine
 Жидкий фтор (при экстремально низких температурах )
| ||||||||||||||||||
| Фтор | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | ||||||||||||||||||
| Аллотропы | альфа, бета (см. Аллотропы фтора ) | |||||||||||||||||
| вид | газ: очень бледно-желтый жидкость: ярко-желтый твердый продукт: альфа непрозрачный, бета прозрачный |
|||||||||||||||||
| Стандартный атомный вес A r °(F) | ||||||||||||||||||
| Фтор в периодической таблице | ||||||||||||||||||
| ||||||||||||||||||
| Атомный номер ( Z ) | 9 | |||||||||||||||||
| Группа | группа 17 (галогены) | |||||||||||||||||
| Период | период 2 | |||||||||||||||||
| Блокировать | p-блок | |||||||||||||||||
| Электронная конфигурация | [ Он ] 2с 2 2п 5 | |||||||||||||||||
| Электроны на оболочку | 2, 7 | |||||||||||||||||
| Физические свойства | ||||||||||||||||||
| Фаза на СТП | газ | |||||||||||||||||
| Температура плавления | (F 2 ) 53,48 К (-219,67 ° С, -363,41 ° F) | |||||||||||||||||
| Точка кипения | (F 2 ) 85,03 К (-188,11 ° С, -306,60 ° F) | |||||||||||||||||
| Плотность (при стандартных условиях) | 1,696 г/л | |||||||||||||||||
| в жидком состоянии (при к.п. ) | 1,505 г/см 3 | |||||||||||||||||
| Тройная точка | 53,48 К, 90 кПа | |||||||||||||||||
| Критическая точка | 144,41 К, 5,1724 МПа | |||||||||||||||||
| Теплота парообразования | 6,51 кДж/моль | |||||||||||||||||
| Молярная теплоемкость | C p : 31 Дж/(моль·K) (при 21,1 °C) C v : 23 Дж/(моль·K) (при 21,1 °C) |
|||||||||||||||||
Давление газа
| ||||||||||||||||||
| Атомные свойства | ||||||||||||||||||
| Степени окисления | −1 , 0 (окисляет кислород) | |||||||||||||||||
| электроотрицательность | Шкала Полинга: 3,98 | |||||||||||||||||
| Энергии ионизации | ||||||||||||||||||
| Ковалентный радиус | 64 вечера | |||||||||||||||||
| Радиус Ван-дер-Ваальса | 135 часов | |||||||||||||||||
| Спектральные линии фтора | ||||||||||||||||||
| Другие свойства | ||||||||||||||||||
| Естественное явление | изначальный | |||||||||||||||||
| Кристальная структура | кубический | |||||||||||||||||
| Теплопроводность | 0,02591 Вт/(м⋅К) | |||||||||||||||||
| Магнитный порядок | диамагнитный (-1,2 × 10 -4 ) | |||||||||||||||||
| Количество CAS | 7782-41-4 | |||||||||||||||||
| История | ||||||||||||||||||
| Именование | в честь минерала флюорита , названного в честь латинского fluo (течь, плавиться) | |||||||||||||||||
| Открытие | Андре-Мари Ампер (1810 г.) | |||||||||||||||||
| Первая изоляция | Анри Муассан (26 июня 1886 г.) | |||||||||||||||||
| Назван | ||||||||||||||||||
| Основные изотопы фтора | ||||||||||||||||||
| ||||||||||||||||||
Фтор — это химический элемент с символом F и атомным номером 9. Это самый легкий галоген , существующий при стандартных условиях в виде высокотоксичного двухатомного газа бледно-желтого цвета. Как самый электроотрицательный элемент, он чрезвычайно реактивен, так как реагирует со всеми другими элементами, кроме аргона , неона и гелия .
Среди элементов фтор занимает 24-е место по повсеместному распространению и 13-е место по земному распространению . Флюорит , первичный минеральный источник фтора, давший название элементу, был впервые описан в 1529 году; поскольку его добавляли в металлические руды , чтобы понизить их температуру плавления при плавке , латинский глагол fluo , означающий «течь», дал название минералу. Предложенный в качестве элемента в 1810 году фтор оказалось трудно и опасно отделять от его соединений, и несколько первых экспериментаторов умерли или получили травмы в результате своих попыток. Только в 1886 году французский химик Анри Муассан выделил элементарный фтор с помощью низкотемпературного электролиза , процесса, который до сих пор используется в современном производстве. Промышленное производство газообразного фтора для обогащения урана , его крупнейшее применение, началось во время Манхэттенского проекта во время Второй мировой войны .
Из-за затрат на очистку чистого фтора в большинстве коммерческих приложений используются соединения фтора, при этом около половины добытого флюорита используется в сталеплавильном производстве . Остальной флюорит превращается в агрессивный фтористый водород на пути к различным органическим фторидам или в криолит , играющий ключевую роль в рафинировании алюминия . Молекулы, содержащие связь углерод-фтор , часто обладают очень высокой химической и термической стабильностью; в основном они используются в качестве хладагентов , электроизоляции и кухонной посуды, а последнее — в качестве ПТФЭ (тефлона). Фармацевтические препараты, такие как аторвастатин и флуоксетин , содержат связи C-F. Ион фтора из растворенных солей фтора препятствует образованию кариеса и поэтому находит применение при фторировании зубной пасты и воды . Мировые продажи фторсодержащих химикатов составляют более 69 миллиардов долларов США в год.
Фторуглеродные газы, как правило, представляют собой парниковые газы с потенциалом глобального потепления в 100–23 500 раз больше, чем у двуокиси углерода , а SF 6 обладает самым высоким потенциалом глобального потепления среди всех известных веществ. Фторорганические соединения часто сохраняются в окружающей среде из-за прочности связи углерод-фтор . Фтор не играет известной метаболической роли у млекопитающих; некоторые растения и морские губки синтезируют фторорганические яды (чаще всего монофторацетаты ), помогающие отпугивать хищников.
Характеристики
Электронная конфигурация
Атомы фтора имеют девять электронов, на один меньше, чем у неона , и электронную конфигурацию 1s 2 2s 2 2p 5 : два электрона на заполненной внутренней оболочке и семь на внешней оболочке, требующей заполнения еще одного. Внешние электроны неэффективны при ядерной защите и имеют высокий эффективный ядерный заряд 9 - 2 = 7; это влияет на физические свойства атома.
Первая энергия ионизации фтора является третьей по величине среди всех элементов после гелия и неона, что усложняет удаление электронов из нейтральных атомов фтора. Он также имеет высокое сродство к электрону , уступая только хлору , и имеет тенденцию захватывать электрон, чтобы стать изоэлектронным с благородным газом неоном; он имеет самую высокую электроотрицательность любого элемента. Атомы фтора имеют небольшой ковалентный радиус около 60 пикометров , аналогичный радиусу его ближайших соседей кислорода и неона.
Реактивность
| Внешнее видео | |
|---|---|
|
| |
|
|
Энергия связи дифтора намного ниже, чем у любого Cl
2или бр
2и аналогична легко расщепляемой перекисной связи; это, наряду с высокой электроотрицательностью, объясняет легкую диссоциацию фтора, высокую реакционную способность и прочные связи с атомами, не относящимися к фтору. И наоборот, связи с другими атомами очень прочны из-за высокой электроотрицательности фтора. Нереакционноспособные вещества, такие как порошковая сталь, осколки стекла и волокна асбеста , быстро реагируют с холодным газообразным фтором; дерево и вода самовозгораются под струей фтора.
Реакции элементарного фтора с металлами требуют различных условий. Щелочные металлы вызывают взрывы, а щелочноземельные металлы проявляют активную активность в массе; чтобы предотвратить пассивацию от образования слоев фторида металла, большинство других металлов, таких как алюминий и железо, необходимо измельчать в порошок, а для благородных металлов требуется чистый газообразный фтор при температуре 300–450 ° C (575–850 ° F). Некоторые твердые неметаллы (сера, фосфор) бурно реагируют с жидким фтором. Сероводород и двуокись серы легко соединяются с фтором, последний иногда взрывоопасен; серная кислота проявляет гораздо меньшую активность, требуя повышенных температур.
Водород , как и некоторые щелочные металлы, взрывоопасно реагирует с фтором. Углерод в виде ламповой сажи реагирует при комнатной температуре с образованием фторметана . Графит соединяется с фтором при температуре выше 400 ° C (750 ° F) с образованием нестехиометрического монофторида углерода ; при более высоких температурах образуются газообразные фторуглероды , иногда со взрывом. Углекислый газ и монооксид углерода реагируют при комнатной температуре или выше, тогда как парафины и другие органические химические вещества вызывают сильные реакции: даже полностью замещенные галогеналканы , такие как четыреххлористый углерод , обычно негорючие, могут взорваться. Хотя трифторид азота стабилен, азот требует электрического разряда при повышенных температурах для реакции с фтором из-за очень сильной тройной связи в элементарном азоте; аммиак может вступить в реакцию со взрывом. Кислород не соединяется с фтором в условиях окружающей среды, но его можно заставить реагировать с помощью электрического разряда при низких температурах и давлениях; продукты имеют тенденцию распадаться на составные элементы при нагревании. Более тяжелые галогены легко реагируют с фтором, как и благородный газ радон ; из других благородных газов реагируют только ксенон и криптон , и только при особых условиях.
Фазы
При комнатной температуре фтор представляет собой газ из двухатомных молекул , бледно-желтый в чистом виде (иногда описываемый как желто-зеленый). Он имеет характерный галогеноподобный резкий и резкий запах, обнаруживаемый при концентрации 20 частей на миллиард . Фтор конденсируется в ярко-желтую жидкость при температуре -188 ° C (-306 ° F), температуре перехода, аналогичной температуре перехода кислорода и азота.
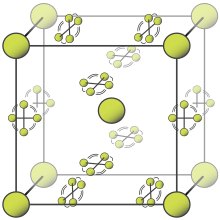
Фтор имеет две твердые формы: α- и β-фтор. Последний кристаллизуется при -220 ° C (-364 ° F), прозрачен и мягок, с такой же неупорядоченной кубической структурой свежекристаллизованного твердого кислорода, в отличие от орторомбических систем других твердых галогенов. Дальнейшее охлаждение до -228 ° C (-378 ° F) вызывает фазовый переход в непрозрачный и твердый α-фтор, который имеет моноклинную структуру с плотными наклонными слоями молекул. Переход от β- к α-фтору более экзотермичен , чем конденсация фтора, и может быть бурным.
Изотопы
В природе в изобилии встречается только один изотоп фтора, стабильный изотоп19
Ф . Обладает высоким магнитогирическим коэффициентом и исключительной чувствительностью к магнитным полям; поскольку это также единственный стабильный изотоп , он используется в магнитно-резонансной томографии . Синтезировано восемнадцать радиоизотопов с массовыми числами от 13 до 31, из них18
F является наиболее стабильным с периодом полураспада 109,77 минут. Другие радиоизотопы имеют период полураспада менее 70 секунд; большинство распадается менее чем за полсекунды. Изотопы17
Ф и18
F претерпевают β + -распад и электронный захват , более легкие изотопы распадаются с испусканием протонов , а более тяжелые , чем19
F претерпевают β - распад (самые тяжелые с испусканием запаздывающих нейтронов ). Известны два метастабильных изомера фтора,18м
F с периодом полураспада 162(7) наносекунд и26м
F с периодом полураспада 2,2 (1) миллисекунды.
Вхождение
Вселенная
| Атомный номер |
Элемент | Относительная сумма |
|---|---|---|
| 6 | Углерод | 4800 |
| 7 | Азот | 1500 |
| 8 | Кислород | 8800 |
| 9 | Фтор | 1 |
| 10 | Неон | 1400 |
| 11 | натрий | 24 |
| 12 | Магний | 430 |
Среди более легких элементов значение содержания фтора в 400 частей на миллиард (частей на миллиард) — 24-е место среди элементов во Вселенной — является исключительно низким: другие элементы от углерода до магния встречаются в двадцать или более раз чаще. Это связано с тем, что звездные процессы нуклеосинтеза обходят фтор, а любые атомы фтора, созданные в противном случае, имеют высокие ядерные сечения , что позволяет при столкновениях с водородом или гелием генерировать кислород или неон соответственно.
Помимо этого временного существования, было предложено три объяснения присутствия фтора:
- во время сверхновых типа II бомбардировка атомов неона нейтрино могла превратить их во фтор;
- солнечный ветер звезд Вольфа-Райе мог сдуть фтор с любых атомов водорода или гелия; или же
- фтор подтверждается конвекционными токами, возникающими при слиянии асимптотических звезд гигантской ветви.
Земля
Фтор является тринадцатым наиболее распространенным элементом в земной коре в концентрации 600–700 ppm (частей на миллион) по массе. Хотя считается, что он не встречается в природе, было показано, что элементарный фтор присутствует в виде окклюзии в антозоните, варианте флюорита. Большая часть фтора существует в виде фторсодержащих минералов. Наиболее промышленно значимыми являются флюорит , фторапатит и криолит . Флюорит ( CaF
2), также известный как плавиковый шпат, широко распространенный во всем мире, является основным источником фтора и, следовательно, фтора. Китай и Мексика являются основными поставщиками. Фторапатит (Ca 5 (PO 4 ) 3 F), который содержит большую часть фтора в мире, является непреднамеренным источником фтора в качестве побочного продукта производства удобрений. Криолит ( Na
3АльФ
6), используемый в производстве алюминия, является наиболее богатым фтором минералом. Экономически жизнеспособные природные источники криолита были исчерпаны, и большая его часть в настоящее время синтезируется в коммерческих целях.
Другие минералы, такие как топаз , содержат фтор. Фториды, в отличие от других галогенидов, нерастворимы и не встречаются в коммерчески выгодных концентрациях в соленых водах. Следовые количества фторорганических соединений неопределенного происхождения были обнаружены при извержениях вулканов и геотермальных источниках. Существование газообразного фтора в кристаллах, на которое указывает запах измельченного антозонита , является спорным; исследование 2012 года сообщило о наличии 0,04% F
2по весу в антозоните, приписывая эти включения излучению из-за присутствия крошечных количеств урана .
История
Ранние открытия

В 1529 году Георгиус Агрикола описал флюорит как добавку, используемую для понижения температуры плавления металлов при плавке . Он придумал латинское слово fluorēs ( fluor , поток) для обозначения флюоритовых пород. Название позже превратилось в плавиковый шпат (все еще широко используемый), а затем в флюорит . Позднее было установлено, что состав флюорита представляет собой дифторид кальция .
Плавиковая кислота использовалась для травления стекла с 1720 года. Андреас Сигизмунд Маргграф впервые охарактеризовал его в 1764 году, когда он нагрел флюорит с серной кислотой, и полученный раствор разъел его стеклянный сосуд. Шведский химик Карл Вильгельм Шееле повторил эксперимент в 1771 году и назвал кислотный продукт флюс-спатс-сиран (плавиковый шпат). В 1810 году французский физик Андре-Мари Ампер предположил, что водород и элемент, аналогичный хлору, составляют плавиковую кислоту. Он также предложил в письме сэру Хамфри Дэви от 26 августа 1812 г. назвать это тогда неизвестное вещество фтором от плавиковой кислоты и суффикса -ine других галогенов. Это слово, часто с изменениями, используется в большинстве европейских языков; однако греческий, русский и некоторые другие, следуя более позднему предложению Ампера, используют имя фтор или производные от греческого φθόριος ( фториос , разрушительный). Новое латинское название fluorum дало элементу его нынешний символ F ; Fl использовался в ранних статьях.
Изоляция
Первоначальные исследования фтора были настолько опасны, что несколько экспериментаторов 19 века были признаны «фтористыми мучениками» после неудач с плавиковой кислотой. Выделению элементарного фтора мешала крайняя коррозионная активность как самого элементарного фтора, так и фтористого водорода, а также отсутствие простого и подходящего электролита . Эдмон Фреми постулировал, что электролиз чистого фтористого водорода для получения фтора возможен, и разработал метод получения безводных образцов из подкисленного бифторида калия ; вместо этого он обнаружил, что полученный (сухой) фтористый водород не проводит электричество. Бывший ученик Фреми Анри Муассан проявил настойчивость и после долгих проб и ошибок обнаружил, что смесь бифторида калия и сухого фтористого водорода является проводником, позволяющим проводить электролиз. Чтобы предотвратить быструю коррозию платины в своих электрохимических элементах , он охладил реакцию до чрезвычайно низких температур в специальной ванне и выковал элементы из более стойкой смеси платины и иридия , а также использовал флюоритовые пробки. В 1886 году, после 74 лет усилий многих химиков, Муассан выделил элементарный фтор.
В 1906 году, за два месяца до смерти, Муассан получил Нобелевскую премию по химии со следующей цитатой:
[В] знак признания больших заслуг, оказанных им в его исследовании и выделении элемента фтора ... Весь мир восхищался большим экспериментальным мастерством, с которым вы изучали этого дикого зверя среди элементов.
Позже использует

Подразделение Frigidaire компании General Motors (GM) экспериментировало с хлорфторуглеродными хладагентами в конце 1920-х годов, а Kinetic Chemicals была создана как совместное предприятие GM и DuPont в 1930 году в надежде продавать фреон-12 ( CCl
2Ф
2) в качестве одного из таких хладагентов . Он заменил более ранние и более токсичные соединения, увеличил спрос на кухонные холодильники и стал прибыльным; к 1949 году DuPont выкупила Kinetic и продала несколько других соединений фреона . Политетрафторэтилен (тефлон) был случайно открыт в 1938 году Роем Дж. Планкеттом во время работы над хладагентами в Kinetic, и его превосходная химическая и термическая стойкость позволила ускорить коммерциализацию и массовое производство к 1941 году.
Крупномасштабное производство элементарного фтора началось во время Второй мировой войны. Германия использовала высокотемпературный электролиз для производства тонн запланированного зажигательного трифторида хлора , а Манхэттенский проект использовал огромные количества для производства гексафторида урана для обогащения урана. Так как УФ
6так же агрессивен, как фтор, газодиффузионным установкам требовались специальные материалы: никель для мембран, фторполимеры для уплотнений и жидкие фторуглероды в качестве охлаждающих и смазочных материалов. Эта бурно развивающаяся атомная промышленность позже стала движущей силой послевоенного развития фторохимии.
Соединения
Фтор имеет богатую химию, охватывающую органические и неорганические домены. Он соединяется с металлами, неметаллами, металлоидами и большинством благородных газов и почти исключительно принимает степень окисления -1. Высокое сродство фтора к электрону приводит к предпочтительности ионной связи ; когда он образует ковалентные связи , они полярны и почти всегда одинарны .
Металлы
Щелочные металлы образуют ионные и хорошо растворимые монофториды ; они имеют кубическое расположение хлорида натрия и аналогичных хлоридов. Дифториды щелочноземельных металлов обладают сильными ионными связями, но нерастворимы в воде, за исключением дифторида бериллия , который также проявляет некоторый ковалентный характер и имеет структуру, подобную кварцу . Редкоземельные элементы и многие другие металлы образуют в основном ионные трифториды .
Ковалентная связь впервые проявляется в тетрафторидах : цирконий , гафний и некоторые актиниды являются ионными с высокими температурами плавления, тогда как соединения титана , ванадия и ниобия являются полимерными, плавятся или разлагаются не выше 350°С (660°С). Ф). Пентафториды продолжают эту тенденцию со своими линейными полимерами и олигомерными комплексами. Известно тринадцать гексафторидов металлов, все октаэдрические, и в основном это летучие твердые вещества, за исключением жидкого MoF.
6и ReF
6, и газообразный ВФ
6. Гептафторид рения , единственный охарактеризованный гептафторид металла , представляет собой низкоплавкое молекулярное твердое вещество с пентагональной бипирамидальной молекулярной геометрией . Фториды металлов с большим количеством атомов фтора особенно реакционноспособны.
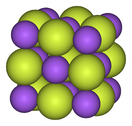
| Структурная прогрессия фторидов металлов | ||
|
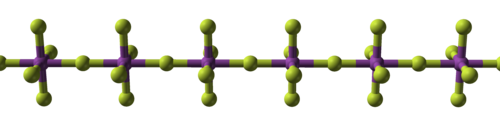
|

|
| Фторид натрия , ионный | Пентафторид висмута , полимерный | Гептафторид рения , молекулярный |
Водород
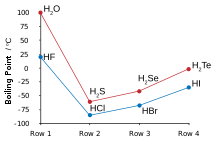
Водород и фтор объединяются с образованием фтористого водорода, в котором дискретные молекулы образуют кластеры посредством водородных связей, больше напоминающие воду, чем хлористый водород . Он кипит при гораздо более высокой температуре, чем более тяжелые галогеноводороды, и в отличие от них смешивается с водой. Фтористый водород легко гидратируется при контакте с водой с образованием водного фтористого водорода, также известного как фтористоводородная кислота. В отличие от других галогеноводородных кислот, которые являются сильными , фтористоводородная кислота является слабой кислотой при низких концентрациях. Однако он может разъедать стекло, чего не могут сделать другие кислоты.
Другие химически активные неметаллы

Бинарные фториды металлоидов и неметаллов p-блока обычно ковалентны и летучи, с различной реакционной способностью. Неметаллы периода 3 и более тяжелые могут образовывать гипервалентные фториды.
Трифторид бора является плоским и имеет неполный октет. Он действует как кислота Льюиса и соединяется с основаниями Льюиса, такими как аммиак, с образованием аддуктов . Четырехфтористый углерод имеет тетраэдрическую форму и инертен; его групповые аналоги, тетрафторид кремния и германия, также являются тетраэдрическими, но ведут себя как кислоты Льюиса. Пниктогены образуют трифториды, реакционная способность и основность которых увеличиваются с увеличением молекулярной массы, хотя трифторид азота устойчив к гидролизу и не является основным. Пентафториды фосфора, мышьяка и сурьмы более реакционноспособны, чем их соответствующие трифториды, при этом пентафторид сурьмы является самой сильной из известных нейтральных кислот Льюиса.
Халькогены имеют разнообразные фториды: сообщалось о нестабильных дифторидах кислорода (единственное известное соединение с кислородом в степени окисления +2), серы и селена; тетрафториды и гексафториды существуют для серы, селена и теллура. Последние стабилизированы большим количеством атомов фтора и более легкими центральными атомами, поэтому гексафторид серы особенно инертен. Хлор, бром и йод могут образовывать моно-, три- и пентафториды, но только гептафторид йода был охарактеризован среди возможных межгалогенных гептафторидов. Многие из них являются мощными источниками атомов фтора, и промышленное применение трифторида хлора требует мер предосторожности, аналогичных тем, которые применяются при использовании фтора.
благородные газы
Благородные газы , имеющие полные электронные оболочки, не реагировали с другими элементами до 1962 года, когда Нил Бартлетт сообщил о синтезе гексафтороплатината ксенона ; С тех пор были выделены дифторид ксенона , тетрафторид , гексафторид и несколько оксифторидов. Среди других благородных газов криптон образует дифторид , а радон и фтор образуют твердое вещество, предположительно являющееся дифторидом радона . Бинарные фториды более легких благородных газов исключительно нестабильны: аргон и фтористый водород в экстремальных условиях соединяются с образованием фторгидрида аргона . Гелий и неон не имеют долгоживущих фторидов, а фторид неона никогда не наблюдался; фторгидрид гелия был обнаружен за миллисекунды при высоких давлениях и низких температурах.
Органические соединения


Связь углерод-фтор является самой прочной в органической химии и придает стабильность фторорганическим соединениям. Его почти не существует в природе, но он используется в искусственных соединениях. Исследования в этой области обычно проводятся в коммерческих целях; вовлеченные соединения разнообразны и отражают сложность, присущую органической химии.
Дискретные молекулы
Замена атомов водорода в алкане все большим количеством атомов фтора постепенно изменяет некоторые свойства: температуры плавления и кипения снижаются, плотность увеличивается, растворимость в углеводородах уменьшается, а общая стабильность увеличивается. Перфторуглероды, в которых замещены все атомы водорода, нерастворимы в большинстве органических растворителей, реагируя в условиях окружающей среды только с натрием в жидком аммиаке.
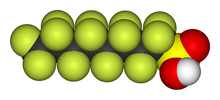
Термин перфторированное соединение используется для того, что в противном случае было бы перфторуглеродом, если бы не присутствие функциональной группы , часто карбоновой кислоты . Эти соединения имеют много общих свойств с перфторуглеродами, таких как стабильность и гидрофобность , в то время как функциональная группа увеличивает их реакционную способность, позволяя им прилипать к поверхностям или действовать как поверхностно- активные вещества ; В частности, фторсодержащие поверхностно-активные вещества могут снижать поверхностное натяжение воды в большей степени, чем их аналоги на углеводородной основе. Фтортеломеры , которые имеют некоторые нефторированные атомы углерода вблизи функциональной группы, также считаются перфторированными.
полимеры
Полимеры демонстрируют такое же повышение стабильности, как и замещение фтором (водорода) в дискретных молекулах; их точки плавления обычно также увеличиваются. Политетрафторэтилен (ПТФЭ), простейший фторполимер и перфтораналог полиэтилена со структурным звеном – CF.
2–, демонстрирует это изменение, как и ожидалось, но его очень высокая температура плавления затрудняет формование. Различные производные ПТФЭ менее устойчивы к температуре, но их легче формовать: фторированный этиленпропилен заменяет некоторые атомы фтора трифторметильными группами, перфторалкоксиалканы делают то же самое с трифторметоксигруппами , а нафион содержит боковые цепи перфторэфира , закрытые группами сульфоновой кислоты . Другие фторполимеры сохраняют некоторые атомы водорода; поливинилиденфторид содержит половину атомов фтора, чем ПТФЭ, а поливинилфторид - четверть, но оба ведут себя как перфторированные полимеры.
Производство
Элементарный фтор и практически все соединения фтора получают из фтористого водорода или его водных растворов, плавиковой кислоты . Фторид водорода получают в печах эндотермической реакцией флюорита ( CaF 2 ) с серной кислотой:
- CaF 2 + H 2 SO 4 → 2 HF(г) + CaSO 4
Затем газообразный HF может быть абсорбирован водой или сжижен.
Около 20% произведенного HF является побочным продуктом производства удобрений, при котором образуется гексафторкремниевая кислота (H 2 SiF 6 ), которая может быть разложена с выделением HF термически и путем гидролиза:
- H 2 SiF 6 → 2 HF + SiF 4
- SiF 4 + 2 H 2 O → 4 HF + SiO 2
Промышленные маршруты к F 2

Метод Муассан используется для производства промышленных количеств фтора путем электролиза смеси фторида калия и фтористого водорода : ионы водорода и фтора восстанавливаются и окисляются на катоде из стального контейнера и аноде из углеродного блока при напряжении 8–12 вольт для получения водород и газообразный фтор соответственно. Температура повышается, KF • 2HF плавится при 70 ° C (158 ° F) и подвергается электролизу при 70–130 ° C (158–266 ° F). KF, который действует для обеспечения электропроводности, необходим, поскольку чистый HF не может подвергаться электролизу, поскольку он практически не проводит электропроводность. Фтор можно хранить в стальных баллонах с пассивированной внутренней частью при температуре ниже 200 ° C (392 ° F); в противном случае можно использовать никель. Клапаны регулятора и трубопроводы изготовлены из никеля, в последнем, возможно, вместо него используется монель . Необходимо проводить частую пассивацию при строгом исключении воды и жиров. В лаборатории стеклянная посуда может содержать газообразный фтор при низком давлении и безводных условиях; некоторые источники вместо этого рекомендуют системы никель-монель-ПТФЭ.
Лабораторные маршруты
Готовясь к конференции 1986 года, посвященной столетию достижений Муассан, Карл О. Кристе пришел к выводу, что химическое производство фтора должно быть осуществимо, поскольку анионы фторидов некоторых металлов не имеют стабильных нейтральных аналогов; вместо этого их подкисление потенциально вызывает окисление. Он разработал метод выделения фтора с высоким выходом и атмосферным давлением:
- 2 KMnO 4 + 2 KF + 10 HF + 3 H 2 O 2 → 2 K 2 MnF 6 + 8 H 2 O + 3 O 2 ↑
- 2 К 2 МнФ 6 + 4 СбФ 5 → 4 КСбФ 6 + 2 МнФ 3 + Ф 2 ↑
Позже Кристе заметил, что реагенты «были известны более 100 лет, и даже Муассан мог придумать эту схему». Еще в 2008 году в некоторых источниках все еще утверждалось, что фтор слишком реактивен для любого химического выделения.
Промышленное применение
Добыча флюорита, который поставляет большую часть фтора в мире, достигла пика в 1989 году, когда было добыто 5,6 миллиона метрических тонн руды. Ограничения по хлорфторуглероду снизили его до 3,6 миллиона тонн в 1994 году; производство с тех пор увеличивается. В 2003 г. было добыто около 4,5 млн тонн руды и получен доход в размере 550 млн долл. США; в более поздних отчетах глобальные продажи фторсодержащих химикатов оцениваются в 2011 году в 15 миллиардов долларов, прогнозируются объемы производства в 2016–2018 годах от 3,5 до 5,9 миллионов тонн, а выручка - не менее 20 миллиардов долларов. Пенная флотация разделяет добытый флюорит на два основных металлургических сорта в равной пропорции: почти весь метшпат с чистотой 60–85% используется в выплавке чугуна, тогда как кислотный шпат с чистотой 97%+ в основном превращается в ключевой промышленный промежуточный фтористый водород.
Ежегодно производится не менее 17 000 метрических тонн фтора. Он стоит всего 5–8 долларов за килограмм в виде гексафторида урана или серы, но во много раз дороже в качестве элемента из-за проблем с обработкой. В большинстве процессов, использующих свободный фтор в больших количествах, используется генерация на месте при вертикальной интеграции .
Наибольшее применение газообразного фтора, потребляющего до 7000 метрических тонн в год, приходится на приготовление UF .
6для ядерного топливного цикла . Фтор используется для фторирования тетрафторида урана , который сам образуется из диоксида урана и плавиковой кислоты. Фтор является моноизотопным, поэтому любые различия в массе между UF
6молекулы обусловлены наличием235
U или238
U , что позволяет обогащать уран методом газовой диффузии или газовой центрифуги . На производство инертного диэлектрика SF уходит около 6000 метрических тонн в год.
6для высоковольтных трансформаторов и автоматических выключателей, устраняя необходимость в опасных полихлорированных дифенилах , связанных с маслонаполненными устройствами. Несколько соединений фтора используются в электронике: гексафторид рения и вольфрама в химическом осаждении из газовой фазы , тетрафторметан в плазменном травлении и трифторид азота в очистном оборудовании. Фтор также используется в синтезе органических фторидов, но его реакционная способность часто требует преобразования сначала в более мягкий ClF .
3, БрФ
3или ЕСЛИ
5, которые в совокупности обеспечивают калиброванное фторирование. Вместо этого во фторированных фармацевтических препаратах используется тетрафторид серы .
Неорганические фториды
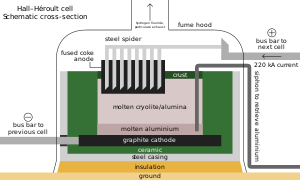
Как и в случае с другими сплавами железа, к каждой метрической тонне стали добавляется около 3 кг (6,5 фунтов) метшпата; ионы фтора снижают его температуру плавления и вязкость . Наряду с ролью добавок в таких материалах, как эмали и покрытия сварочных электродов, большинство кислотных шпатов вступают в реакцию с серной кислотой с образованием плавиковой кислоты, которая используется при травлении стали , травлении стекла и крекинге алканов . Одна треть HF идет на синтез криолита и трифторида алюминия , оба флюса в процессе Холла-Эру для извлечения алюминия; пополнение необходимо из-за их случайных реакций с плавильным аппаратом. На каждую метрическую тонну алюминия требуется около 23 кг (51 фунт) флюса. Фторосиликаты потребляют вторую по величине долю, а фторсиликат натрия используется при фторировании воды и очистке сточных вод от прачечных, а также в качестве промежуточного продукта на пути к криолиту и тетрафториду кремния. Другие важные неорганические фториды включают фториды кобальта , никеля и аммония .
Органические фториды
Фторорганические соединения потребляют более 20% добываемого флюорита и более 40% плавиковой кислоты, при этом преобладают газообразные хладагенты , а доля рынка фторполимеров увеличивается. Поверхностно -активные вещества являются второстепенным приложением, но приносят более 1 миллиарда долларов годового дохода. Из-за опасности прямых реакций углеводород-фтор при температуре выше -150 ° C (-240 ° F) промышленное производство фторуглеродов является косвенным, в основном за счет реакций обмена галогенов , таких как фторирование Свортса , в которых хлорхлоруглеродные хлоры замещаются фтористым фтористым водородом при катализаторы. Электрохимическое фторирование подвергает углеводороды электролизу во фтористом водороде, а процесс Фаулера обрабатывает их твердыми носителями фтора, такими как трифторид кобальта .
Хладагенты
Галогенированные хладагенты, называемые в неофициальном контексте фреонами, обозначаются R-числами , обозначающими количество присутствующих фтора, хлора, углерода и водорода. Хлорфторуглероды (ХФУ), такие как R-11 , R-12 и R-114 , когда- то доминировали над фторорганическими соединениями, пик производства которых пришелся на 1980-е годы. Используемые для систем кондиционирования воздуха, пропеллентов и растворителей, их производство было ниже одной десятой от этого пика к началу 2000-х годов после широко распространенного международного запрета. Гидрохлорфторуглероды (ГХФУ) и гидрофторуглероды (ГФУ) были разработаны в качестве замены; на их синтез расходуется более 90% фтора в органической промышленности. Важные ГХФУ включают R-22, хлордифторметан и R-141b . Основным ГФУ является R-134a с новым типом молекулы HFO-1234yf , гидрофторолефином (HFO), получившим известность из-за его потенциала глобального потепления , составляющего менее 1% от потенциала ГФУ-134a.
полимеры

В 2006 и 2007 годах было произведено около 180 000 метрических тонн фторполимеров, что принесло более 3,5 миллиардов долларов дохода в год. В 2011 году мировой рынок оценивался чуть менее чем в 6 миллиардов долларов, и прогнозировалось, что он будет расти на 6,5% в год до 2016 года. Фторполимеры могут быть образованы только путем полимеризации свободных радикалов.
Политетрафторэтилен (ПТФЭ), иногда называемый по названию DuPont тефлон, составляет 60–80% по массе мирового производства фторполимеров. Наибольшее применение в электроизоляции , так как PTFE является отличным диэлектриком . Он также используется в химической промышленности, где требуется коррозионная стойкость, для покрытия труб, трубопроводов и прокладок. Еще одним важным применением является стекловолоконная ткань с покрытием из ПТФЭ для крыш стадионов. Основное потребительское применение – посуда с антипригарным покрытием . Сорванная пленка ПТФЭ становится расширенным ПТФЭ (ePTFE), мелкопористой мембраной , иногда называемой торговой маркой Gore-Tex и используемой для непромокаемой одежды, защитной одежды и фильтров ; Волокна из эПТФЭ могут быть использованы для изготовления уплотнений и пылеулавливающих фильтров . Другие фторполимеры, в том числе фторированный этиленпропилен , имитируют свойства ПТФЭ и могут его заменить; они более формуемы, но также более дороги и имеют более низкую термическую стабильность. Пленки из двух разных фторполимеров заменяют стекло в солнечных батареях.
Химически стойкие (но дорогие) фторированные иономеры используются в качестве электрохимических клеточных мембран, первым и наиболее ярким примером которых является нафион . Разработанный в 1960-х годах, он первоначально использовался в качестве материала топливных элементов в космических кораблях, а затем заменил хлорщелочные технологические элементы на ртутной основе. В последнее время применение топливных элементов возродилось в связи с усилиями по установке топливных элементов с протонообменной мембраной в автомобили. Фторэластомеры , такие как витон , представляют собой сшитые смеси фторполимеров, в основном используемые в уплотнительных кольцах ; перфторбутан (C 4 F 10 ) используется в качестве огнетушащего вещества.
ПАВ
Фторсодержащие поверхностно-активные вещества представляют собой небольшие фторорганические молекулы, используемые для отталкивания воды и пятен. Хотя они дороги (сопоставимы с фармацевтическими препаратами по цене 200–2000 долларов за килограмм), к 2006 году они принесли годовой доход более 1 миллиарда долларов; Только компания Scotchgard заработала более 300 миллионов долларов в 2000 году. Фторсодержащие поверхностно-активные вещества составляют меньшинство на общем рынке поверхностно-активных веществ, большая часть которого занята гораздо более дешевыми продуктами на основе углеводородов. Применение красок обременено затратами на приготовление смеси ; это использование было оценено всего в 100 миллионов долларов в 2006 году.
Агрохимикаты
Около 30% агрохимикатов содержат фтор, большинство из них гербициды и фунгициды с небольшим количеством регуляторов урожая . Замена фтором, обычно одного атома или, самое большее, трифторметильной группы, является надежной модификацией с эффектами, аналогичными фторированным фармацевтическим препаратам: увеличение времени биологического пребывания, пересечение мембраны и изменение молекулярного распознавания. Ярким примером является трифлуралин, широко используемый в США в качестве средства от сорняков, но он считается канцерогеном и запрещен во многих европейских странах . Монофторацетат натрия (1080) представляет собой яд для млекопитающих, в котором два атома водорода уксусной кислоты заменены фтором и натрием; он нарушает клеточный метаболизм, заменяя ацетат в цикле лимонной кислоты . Впервые синтезированный в конце 19 века, он был признан инсектицидом в начале 20-го века, а позже был использован в его нынешнем использовании. Новая Зеландия, крупнейший потребитель из 1080 видов, использует его для защиты киви от инвазивного австралийского опоссума . Европа и США запретили 1080.
Лекарственные применения
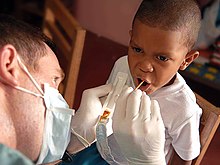
Стоматологическая уход
Популяционные исследования, проведенные с середины 20-го века, показывают, что местное применение фтора уменьшает кариес зубов . Сначала это было связано с превращением гидроксиапатита зубной эмали в более прочный фторапатит, но исследования предварительно фторированных зубов опровергли эту гипотезу, и современные теории предполагают, что фтор способствует росту эмали при небольшом кариесе. После исследований детей в районах, где фторид естественным образом присутствовал в питьевой воде, в 1940-х годах началось контролируемое фторирование общественного водоснабжения для борьбы с кариесом, и в настоящее время оно применяется к воде, снабжающей водой 6 процентов населения мира, включая две трети американцев. Обзоры научной литературы 2000 и 2007 годов связывают фторирование воды со значительным уменьшением кариеса у детей. Несмотря на такое одобрение и доказательства отсутствия побочных эффектов, кроме в основном доброкачественного флюороза зубов , возражения по-прежнему существуют по этическим соображениям и соображениям безопасности. Преимущества фторирования уменьшились, возможно, из-за других источников фтора, но все еще измеримы в группах с низким доходом. Монофторфосфат натрия и иногда фторид натрия или олова (II) часто встречаются во фторидных зубных пастах , впервые представленных в США в 1955 году и теперь широко распространенных в развитых странах, наряду с фторированными ополаскивателями для рта, гелями, пенами и лаками.
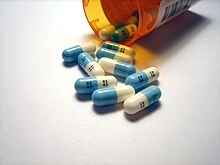
Фармацевтика
Двадцать процентов современных фармацевтических препаратов содержат фтор. Один из них, препарат для снижения уровня холестерина аторвастатин (Липитор), приносил больше доходов, чем любой другой препарат, пока не стал универсальным в 2011 году. Комбинированный препарат от астмы Серетид , входящий в десятку самых прибыльных препаратов в середине 2000-х годов, содержит два активных ингредиента: один из которых – флутиказон – фторирован. Многие лекарства фторируют, чтобы отсрочить инактивацию и продлить период приема, поскольку связь углерод-фтор очень стабильна. Фторирование также увеличивает липофильность , поскольку связь более гидрофобна, чем связь углерод-водород , и это часто способствует проникновению через клеточную мембрану и, следовательно, биодоступности .
Трициклические препараты и другие антидепрессанты до 1980-х годов имели несколько побочных эффектов из-за их неизбирательного воздействия на нейротрансмиттеры , отличные от мишени серотонина ; фторированный флуоксетин был селективным и одним из первых, чтобы избежать этой проблемы. Многие современные антидепрессанты подвергаются такому же лечению, включая селективные ингибиторы обратного захвата серотонина : циталопрам , его изомер эсциталопрам , а также флувоксамин и пароксетин . Хинолоны — это искусственные антибиотики широкого спектра действия , которые часто фторируют для усиления их действия. К ним относятся ципрофлоксацин и левофлоксацин . Фтор также находит применение в стероидах: флудрокортизон — минералокортикоид , повышающий артериальное давление , а триамцинолон и дексаметазон — сильные глюкокортикоиды . Большинство ингаляционных анестетиков сильно фторированы; прототип галотана гораздо более инертен и эффективен, чем его современники. Более поздние соединения, такие как фторированные эфиры севофлюран и десфлуран , лучше, чем галотан, и почти нерастворимы в крови, что позволяет быстрее просыпаться.
ПЭТ-сканирование
Фтор-18 часто встречается в радиоактивных трассерах для позитронно-эмиссионной томографии, поскольку его период полураспада, составляющий почти два часа, достаточно велик, чтобы его можно было транспортировать с производственных объектов в центры визуализации. Наиболее распространенным индикатором является фтордезоксиглюкоза , которая после внутривенной инъекции поглощается тканями, нуждающимися в глюкозе, такими как мозг и большинство злокачественных опухолей; затем компьютерная томография может быть использована для детальной визуализации.
Кислородоносцы
Жидкие фторуглероды могут удерживать большие объемы кислорода или углекислого газа, больше, чем кровь, и привлекли внимание к их возможному использованию в искусственной крови и жидкостном дыхании. Поскольку фторуглероды обычно не смешиваются с водой, их необходимо смешивать в эмульсии (маленькие капли перфторуглерода, взвешенные в воде), чтобы использовать их в качестве крови. Один из таких продуктов, Oxycyte , прошел первые клинические испытания. Эти вещества могут помочь спортсменам, занимающимся выносливостью, и запрещены для занятий спортом; близкая смерть одного велосипедиста в 1998 году побудила к расследованию жестокого обращения с ними. Применение чистого перфторуглеродного жидкостного дыхания (при котором используется чистая перфторуглеродная жидкость, а не водная эмульсия) включает помощь пострадавшим от ожогов и недоношенным детям с недостаточностью легких. Рассматривалось частичное и полное заполнение легких, хотя только первое имело какие-либо серьезные испытания на людях. Усилия Alliance Pharmaceuticals дошли до клинических испытаний, но от них отказались, поскольку результаты были не лучше, чем у обычных методов лечения.
Биологическая роль

Фтор не является необходимым для человека и других млекопитающих, но известно, что небольшие количества фтора полезны для укрепления зубной эмали (где образование фторапатита делает эмаль более устойчивой к воздействию кислот, образующихся при бактериальной ферментации сахаров). Небольшие количества фтора могут быть полезны для прочности костей, но последнее окончательно не установлено. И ВОЗ, и Институт медицины Национальной академии США публикуют рекомендуемую суточную норму (RDA) и верхнюю допустимую норму потребления фтора, которая зависит от возраста и пола.
Природные фторорганические соединения обнаружены в микроорганизмах и растениях, но не в животных. Наиболее распространенным является фторацетат , который используется в качестве защиты от травоядных как минимум на 40 растениях в Африке, Австралии и Бразилии. Другие примеры включают концевые фторированные жирные кислоты , фторацетон и 2-фторцитрат. В 2002 году у бактерий был обнаружен фермент, связывающий фтор с углеродом – аденозилфторидсинтаза .
Токсичность
Элементарный фтор очень токсичен для живых организмов. Его воздействие на человека начинается при концентрациях ниже 50 частей на миллион цианистого водорода и аналогично воздействию хлора: значительное раздражение глаз и дыхательной системы, а также повреждение печени и почек возникает при концентрациях выше 25 частей на миллион, что представляет непосредственную опасность для жизни . и значение для здоровья фтора. Глаза и нос серьезно повреждены при концентрации 100 частей на миллион, а вдыхание 1000 частей на миллион фтора приведет к смерти в течение нескольких минут по сравнению с 270 частями на миллион цианистого водорода.
| Опасности | |
|---|---|
| Маркировка СГС : | |
   
|
|
| Опасность | |
| Х270 , Х314 , Х330 | |
| NFPA 704 (огненный алмаз) | |
Плавиковая кислота
Плавиковая кислота является самой слабой из галоидоводородных кислот, ее pKa составляет 3,2 при 25 °C. Это летучая жидкость из-за наличия водородных связей (в то время как другие галогеноводородные кислоты являются газами). Он способен атаковать стекло, бетон, металлы, органику.
Плавиковая кислота представляет собой контактный яд с большей опасностью, чем многие сильные кислоты, такие как серная кислота, хотя она и слабая: она остается нейтральной в водном растворе и, таким образом, быстрее проникает в ткани при вдыхании, приеме внутрь или через кожу, и по меньшей мере девять американских рабочих погибли. в таких авариях с 1984 по 1994 год. Он реагирует с кальцием и магнием в крови, что приводит к гипокальциемии и возможной смерти от сердечной аритмии . Образование нерастворимого фторида кальция вызывает сильную боль, а ожоги площадью более 160 см 2 (25 дюймов 2 ) могут вызвать серьезную системную токсичность.
Воздействие может быть незаметным в течение восьми часов для 50% HF, увеличиваясь до 24 часов для более низких концентраций, а ожог может сначала быть безболезненным, поскольку фтористый водород влияет на нервную функцию. Если кожа подвергалась воздействию HF, повреждение можно уменьшить, промыв ее под струей воды в течение 10–15 минут и сняв загрязненную одежду. Следующим часто применяется глюконат кальция , обеспечивающий связывание ионов кальция с фторидом; ожоги кожи можно лечить 2,5% гелем глюконата кальция или специальными растворами для полоскания. Поглощение плавиковой кислоты требует дальнейшего лечения; глюконат кальция можно вводить инъекционно или внутривенно. Использование хлорида кальция — распространенного лабораторного реагента — вместо глюконата кальция противопоказано и может привести к серьезным осложнениям. Может потребоваться иссечение или ампутация пораженных частей.
Ион фтора
Растворимые фториды умеренно токсичны: 5–10 г фторида натрия или 32–64 мг ионов фтора на килограмм массы тела представляют собой смертельную дозу для взрослых. Пятая часть смертельной дозы может вызвать неблагоприятные последствия для здоровья, а хроническое избыточное потребление может привести к флюорозу скелета , от которого страдают миллионы людей в Азии и Африке. Проглоченный фтор образует в желудке фтористоводородную кислоту, которая легко всасывается в кишечнике, где она проникает через клеточные мембраны, связывается с кальцием и взаимодействует с различными ферментами до экскреции с мочой . Пределы воздействия определяются анализом мочи на способность организма выводить ионы фтора.
Исторически сложилось так, что большинство случаев отравления фтором было вызвано случайным приемом внутрь инсектицидов, содержащих неорганические фториды. Большинство текущих обращений в токсикологические центры по поводу возможного отравления фтором исходят от приема зубной пасты, содержащей фтор. Еще одной причиной является неисправное оборудование для фторирования воды: один инцидент на Аляске затронул почти 300 человек и один человек погиб. Опасности от зубной пасты усугубляются для маленьких детей, и Центры по контролю и профилактике заболеваний рекомендуют следить за чисткой зубов детьми младше шести лет, чтобы они не глотали зубную пасту. Одно региональное исследование изучило годовые сообщения об отравлении фтором до подросткового возраста, в общей сложности 87 случаев, в том числе один случай смерти от приема инсектицидов. У большинства не было никаких симптомов, но около 30% испытывали боли в животе. Более крупное исследование, проведенное в США, дало аналогичные результаты: 80% случаев касались детей в возрасте до шести лет, а серьезных случаев было немного.
Проблемы окружающей среды
Атмосфера
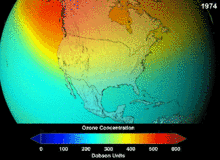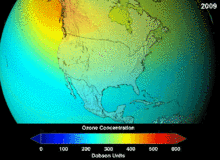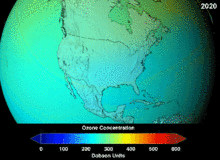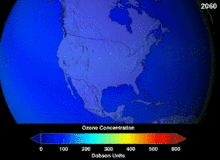
Монреальский протокол , подписанный в 1987 году , устанавливает строгие правила в отношении хлорфторуглеродов (ХФУ) и бромфторуглеродов из-за их способности разрушать озоновый слой (ОРФ). Высокая стабильность, которая подходила им для их первоначального применения, также означала, что они не разлагались до тех пор, пока не достигали больших высот, где высвобожденные атомы хлора и брома атаковали молекулы озона. Прогнозы предупреждали, что даже с учетом запрета и первых признаков его эффективности пройдет несколько поколений до полного восстановления. Имея одну десятую ОРС ХФУ, гидрохлорфторуглероды (ГХФУ) являются текущими заменителями, и к 2030–2040 гг. они сами должны быть заменены гидрофторуглеродами (ГФУ) без хлора и с нулевым ОРС. В 2007 году эта дата была перенесена на 2020 год для развитых стран; Агентство по охране окружающей среды уже запретило производство одного ГХФУ и ограничило производство двух других в 2003 году. Фторуглеродные газы обычно представляют собой парниковые газы с потенциалом глобального потепления (ПГП) примерно от 100 до 10 000; гексафторид серы имеет стоимость около 20 000. Исключением является HFO-1234yf , который представляет собой новый тип хладагента, называемый гидрофторолефином (HFO), и привлек глобальный спрос благодаря своему ПГП менее 1 по сравнению с 1430 для текущего стандарта хладагента HFC-134a .
Биостойкость
Фторорганические соединения проявляют биостойкость из-за прочности связи углерод-фтор. Перфторалкильные кислоты (PFAA), которые мало растворимы в воде из-за их кислотных функциональных групп, считаются стойкими органическими загрязнителями ; Наиболее часто исследуются перфтороктансульфокислота (ПФОС) и перфтороктановая кислота ( ПФОК ) . ПФАА были обнаружены в следовых количествах по всему миру от белых медведей до человека, при этом известно, что ПФОС и ПФОК находятся в грудном молоке и крови новорожденных. Обзор 2013 года показал небольшую корреляцию между уровнями PFAA в грунтовых водах и почве и деятельностью человека; не было четкой картины преобладания одного химического вещества, и более высокие количества ПФОС коррелировали с более высокими количествами ПФОК. В организме PFAA связываются с белками, такими как сывороточный альбумин ; они, как правило, концентрируются в организме человека в печени и крови перед выделением через почки. Время пребывания в организме сильно различается в зависимости от вида: период полураспада составляет дни у грызунов и годы у людей. Высокие дозы ПФОС и ПФОК вызывают рак и смерть новорожденных грызунов, но исследования на людях не установили эффекта при нынешних уровнях воздействия.
Смотрите также
- Аргонфторидный лазер
- Электрофильное фторирование
- Селективный электрод для фтора , который измеряет концентрацию фтора.
- Датирование поглощения фтора
- Фтористая химия , процесс, используемый для отделения реагентов от органических растворителей .
- Криптонфторидный лазер
- Радикальное фторирование
Заметки
Источники
Цитаты
Индексированные ссылки
- Агрикола, Георгиус ; Гувер, Герберт Кларк; Гувер, Лу Генри (1912). Де Ре Металлика . Лондон: Горный журнал.
- Эгеперс, Дж.; Моллард, П.; Девилье, Д.; Чемла, М .; Фарон, Р.; Романо, RE; Кью, JP (2000). «Соединения фтора, неорганические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. стр. 397–441. дои : 10.1002/14356007 .
- Воздушные продукты и химикаты (2004 г.). «График безопасности № 39 Трифторид хлора» (PDF) . Воздушные продукты и химикаты. Архивировано из оригинала (PDF) 18 марта 2006 г .. Проверено 16 февраля 2014 г.
- Алави, Аббас; Хуанг, Стив С. (2007). «Позитронно-эмиссионная томография в медицине: обзор». В Хаят, Массачусетс (ред.). Визуализация рака, том 1: карциномы легких и молочной железы . Берлингтон: Академическая пресса. стр. 39–44. ISBN 978-0-12-370468-9.
- Ампер, Андре-Мари (1816 г.). «Сюита естественной классификации для простого корпуса» . Annales de chimie et de physique (на французском языке). 2 : 1–5.
- Арана, LR; Мас, Н .; Шмидт, Р.; Франц, А.Дж.; Шмидт, Массачусетс; Дженсен, К.Ф. (2007). «Изотропное травление кремния в газообразном фторе для микрообработки MEMS». Журнал микромеханики и микротехники . 17 (2): 384–392. Бибкод : 2007JMiMi..17..384A . doi : 10.1088/0960-1317/17/2/026 .
- Армфилд, Дж. М. (2007). «Когда общественные действия подрывают общественное здоровье: критический анализ литературы, выступающей против фторирования» . Политика здравоохранения Австралии и Новой Зеландии . 4 : 25. doi : 10.1186/1743-8462-4-25 . ПМЦ 2222595 . PMID 18067684 .
- Азимов, Исаак (1966). Благородные газы . Нью-Йорк: Основные книги. ISBN 978-0-465-05129-8.
- Аткинс, Питер ; Джонс, Лоретта (2007). Химические принципы: В поисках понимания (4-е изд.). Нью-Йорк: WH Freeman. ISBN 978-1-4292-0965-6.
- Окамп, Питер Дж.; Бьорн, Ларс Улоф (2010). «Вопросы и ответы об экологических последствиях истощения озонового слоя и изменения климата: обновление 2010 г.» (PDF) . Программа ООН по окружающей среде. Архивировано из оригинала (PDF) 3 сентября 2013 г .. Проверено 14 октября 2013 г.
- Ауди, Г.; Кондев, Ф.Г.; Ван, М .; Хуанг, WJ; Наими, С. (2017). «Оценка ядерных свойств NUBASE2016» (PDF) . Китайская физика С. 41 (3): 030001. Бибкод : 2017ChPhC..41c0001A . дои : 10.1088/1674-1137/41/3/030001 ..
- Аугенштейн, WL; и другие. (1991). «Проглатывание фтора детьми: обзор 87 случаев» . Педиатрия . 88 (5): 907–912. doi : 10.1542/peds.88.5.907 . PMID 1945630 . S2CID 22106466 .
- Бабель, Дитрих; Трессо, Ален (1985). «Кристаллохимия фторидов». В Hagenmuller, Пол (ред.). Неорганические твердые фториды: химия и физика . Орландо: Академическая пресса. стр. 78–203. ISBN 978-0-12-412490-5.
- Баэлум, Вибеке; Шейхэм, Обри; Берт, Брайан (2008). «Контроль кариеса для населения». Ин Фейерсков, Оле; Кидд, Эдвина (ред.). Кариес зубов: болезнь и ее клиническое лечение (2-е изд.). Оксфорд: Блэквелл Манксгаард. стр. 505–526. ISBN 978-1-4051-3889-5.
- Баэз, Рамон Дж.; Баэз, Марта X .; Марталер, Томас М. (2000). «Выделение фтора с мочой у детей 4–6 лет в сообществе Южного Техаса» . Revista Panamericana de Salud Pública . 7 (4): 242–248. doi : 10.1590/S1020-49892000000400005 . PMID 10846927 .
- Бэнкс, RE (1986). «Выделение фтора Муассаном: обстановка». Журнал химии фтора . 33 (1–4): 3–26. doi : 10.1016/S0022-1139(00)85269-0 .
- Барби, К.; Маккормак, К.; Вартанян, В. (2000). «Проблемы EHS с обработкой распылением озонированной воды». В Mendicino, L. (ред.). Экологические проблемы в электронной и полупроводниковой промышленности . Пеннингтон, Нью-Джерси: Электрохимическое общество. стр. 108–121. ISBN 978-1-56677-230-3.
- Барретт, CS; Мейер, Л.; Вассерман, Дж. (1967). «Фазовая диаграмма аргон-фтор». Журнал химической физики . 47 (2): 740–743. Бибкод : 1967JChPh..47..740B . дои : 10.1063/1.1711946 .
- Барри, Патрик Л.; Филлипс, Тони (26 мая 2006 г.). «Хорошие новости и загадка» . Национальное управление по аэронавтике и исследованию космического пространства . Проверено 6 января 2012 г.
- Бартлетт, Н. (1962). «Гексафторплатинат ксенона (V) Xe + [PtF 6 ] - ». Труды Химического общества (6): 218. doi : 10.1039/PS9620000197 .
- Бизли, Майкл (август 2002 г.). Руководство по безопасному использованию фторацетата натрия (1080) (PDF) . Веллингтон: Служба безопасности и гигиены труда, Министерство труда (Новая Зеландия). ISBN 0-477-03664-3. Архивировано из оригинала (PDF) 11 ноября 2013 г .. Проверено 11 ноября 2013 г.
- Бек, Джефферсон; Ньюман, Пол; Шиндлер, Трент Л.; Перкинс, Лори (2011). «Что случилось бы с озоновым слоем, если бы хлорфторуглероды (ХФУ) не регулировались?» . Национальное управление по аэронавтике и исследованию космического пространства . Проверено 15 октября 2013 г.
- Беккер, С.; Мюллер, Б.Г. (1990). «Тетрафторид ванадия». Международное издание Angewandte Chemie на английском языке . 29 (4): 406–407. doi : 10.1002/anie.199004061 .
- Беге, Жан-Пьер; Бонне-Дельпон, Даниэль (2008). Биоорганическая и медицинская химия фтора . Хобокен: Джон Уайли и сыновья. ISBN 978-0-470-27830-7.
- Беттс, Канзас (2007). «Перфторалкильные кислоты: о чем нам говорят доказательства?» . Перспективы гигиены окружающей среды . 115 (5): А250–А256. doi : 10.1289/ehp.115-a250 . ПВК 1867999 . PMID 17520044 .
- Бихари, З .; Чабан, гроссмейстер; Гербер, РБ (2002). «Стабильность химически связанного соединения гелия в твердом гелии высокого давления». Журнал химической физики . 117 (11): 5105–5108. Бибкод : 2002JChPh.117.5105B . дои : 10.1063/1.1506150 .
- Биллер, Хосе (2007). Интерфейс неврологии и внутренней медицины (иллюстрированное издание). Филадельфия: Липпинкотт Уильямс и Уилкинс. ISBN 978-0-7817-7906-7.
- Блоджетт, Д. У.; Суруда, А.Дж.; Крауч, Б.И. (2001). «Непреднамеренные профессиональные отравления плавиковой кислотой со смертельным исходом в США» (PDF) . Американский журнал промышленной медицины . 40 (2): 215–220. дои : 10.1002/аджим.1090 . PMID 11494350 . Архивировано из оригинала (PDF) 17 июля 2012 г.
- Бомбург, Николя (4 июля 2012 г.). «Мировой рынок фторохимикатов, Фридония» . Репортерлинкер . Проверено 20 октября 2013 г.
- Брантли, Л.Р. (1949). Сквайрс, Рой; Кларк, Артур С. (ред.). "Фтор". Pacific Rockets: журнал Тихоокеанского ракетного общества . Южная Пасадена: Sawyer Publishing / Историческая библиотека Тихоокеанского ракетного общества. 3 (1): 11–18. ISBN 978-0-9794418-5-1.
- Броуди, Джейн Э. (10 сентября 2012 г.). «Популярные антибиотики могут иметь серьезные побочные эффекты» . Блог The New York Times Well . Проверено 18 октября 2013 г.
- Браун, Пол Л.; Момпин, Федерико Дж .; Перроне, Джейн; Иллемассен, Мириам (2005). Химическая термодинамика циркония . Амстердам: Elsevier BV ISBN 978-0-444-51803-3.
- Бердон, Дж.; Эмсон, Б.; Эдвардс, Эй Джей (1987). «Действительно ли газообразный фтор желтый?» Журнал химии фтора . 34 (3–4): 471–474. doi : 10.1016/S0022-1139(00)85188-X .
- Бюрги, HB (2000). «Движение и беспорядок в анализе кристаллической структуры: их измерение и различение». Ежегодный обзор физической химии . 51 : 275–296. Бибкод : 2000ARPC...51..275B . doi : 10.1146/annurev.physchem.51.1.275 . PMID 11031283 .
- Берни, Х. (1999). «Прошлое, настоящее и будущее хлорно-щелочной промышленности». В Берни, HS; Фуруя, Н .; Хайн, Ф.; Ота, К.-И. (ред.). Хлорно-щелочные и хлоратные технологии: Мемориальный симпозиум Р.Б. Макмаллина . Пеннингтон: Электрохимическое общество. стр. 105–126. ISBN 1-56677-244-3.
- Бустаманте, Э.; Педерсен, PL (1977). «Высокий аэробный гликолиз клеток гепатомы крыс в культуре: роль митохондриальной гексокиназы» . Труды Национальной академии наук . 74 (9): 3735–3739. Бибкод : 1977PNAS...74.3735B . doi : 10.1073/pnas.74.9.3735 . ПВК 431708 . PMID 198801 .
- Бузник, В.М. (2009). «Химия фторполимеров в России: состояние и перспективы». Российский журнал общей химии . 79 (3): 520–526. дои : 10.1134/S1070363209030335 . S2CID 97518401 .
- Кэмерон, АГВ (1973). «Изобилие элементов в Солнечной системе» (PDF) . Обзоры космической науки . 15 (1): 121–146. Бибкод : 1973SSRv...15..121C . DOI : 10.1007/ BF00172440 . S2CID 120201972 . Архивировано из оригинала (PDF) 21 октября 2011 г.
- Кэри, Чарльз В. (2008). Афроамериканцы в науке . Санта-Барбара: ABC-CLIO. ISBN 978-1-85109-998-6.
- Карлсон, Д.П.; Шмигель, В. (2000). «Фторполимеры органические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. стр. 495–533. дои : 10.1002/14356007.a11_393 .
- Центры по контролю и профилактике заболеваний (2001 г.). «Рекомендации по использованию фтора для профилактики и контроля кариеса зубов в Соединенных Штатах» . Рекомендации и отчеты MMWR . 50 (RR–14): 1–42. PMID 11521913 . Проверено 14 октября 2013 г.
- Центры по контролю и профилактике заболеваний (10 июля 2013 г.). «Общественное фторирование воды» . Проверено 25 октября 2013 г.
- Чемберс, К.; Холлидей, Аляска (1975). Современная неорганическая химия: промежуточный текст (PDF) . Лондон: Butterworth & Co. ISBN 978-0-408-70663-6. Архивировано из оригинала (PDF) 23 марта 2013 г.
- Чанг, Раймонд ; Голдсби, Кеннет А. (2013). Химия (11-е изд.). Нью-Йорк: Макгроу-Хилл. ISBN 978-0-07-131787-0.
- Ченг, Х .; Фаулер, Делавэр; Хендерсон, ПБ; Хоббс, JP; Пасколини, М. Р. (1999). «О магнитной восприимчивости фтора». Журнал физической химии А . 103 (15): 2861–2866. Бибкод : 1999JPCA..103.2861C . дои : 10.1021/jp9844720 .
- Ченг, К.К.; Чалмерс, И.; Шелдон, Т. А. (2007). «Добавление фтора в воду» (PDF) . БМЖ . 335 (7622): 699–702. doi : 10.1136/bmj.39318.562951.BE . ПМС 2001050 . PMID 17916854 . Архивировано из оригинала (PDF) 3 марта 2016 года . Проверено 26 марта 2012 г.
- Чисте, В.; Бе, ММ (2011). "Ф-18" (PDF) . В Бе, мм; Курсоль, Н.; Дюшемен, Б.; Лагутин, Ф.; и другие. (ред.). Таблица радионуклидов (отчет). CEA (Комиссариат по атомной энергии и альтернативным источникам энергии), LIST, LNE-LNHB (Национальная лаборатория Анри Беккереля/Комиссариат по атомной энергии) . Проверено 15 июня 2011 г.
- Кристе, Карл О. (1986). «Химический синтез элементарного фтора». Неорганическая химия . 25 (21): 3721–3722. doi : 10.1021/ic00241a001 .
- Исследовательская группа Christe (nd). «Химический синтез элементарного фтора» . Архивировано из оригинала 4 марта 2016 года . Проверено 12 января 2013 г.
- Кларк, Джим (2002). «Кислотность галогеноводородов» . chemguide.co.uk . Проверено 15 октября 2013 г.
- Клейтон, Дональд (2003). Справочник по изотопам в космосе: от водорода до галлия . Нью-Йорк: Издательство Кембриджского университета. ISBN 978-0-521-82381-4.
- Ассоциация сжатого газа (1999). Справочник по сжатым газам (4-е изд.). Бостон: Kluwer Academic Publishers. ISBN 978-0-412-78230-5.
- Кордеро, Б.; Гомес, В .; Платеро-Пратс, А.Е.; Ревес, М .; Эчеверрия, Дж.; Кремадес, Э.; Барраган, Ф .; Альварес, С. (2008). «Возвращение ковалентных радиусов». Сделки Далтона (21): 2832–2838. дои : 10.1039/b801115j . PMID 18478144 .
- Крачер, Конни М. (2012). «Современные концепции профилактической стоматологии» (PDF) . www.dentalcare.com. Архивировано из оригинала (PDF) 14 октября 2013 года . Проверено 14 октября 2013 г.
- Кросвелл, Кен (сентябрь 2003 г.). «Фтор: элементарная тайна» . Небо и телескоп . Проверено 17 октября 2013 г.
- Митчелл Кроу, Джеймс (2011). «Обнаружены первые признаки восстановления озоновой дыры» . Природа . doi : 10.1038/news.2011.293 .
- Дэвис, Николь (ноябрь 2006 г.). «Лучше, чем кровь» . Популярная наука . Архивировано из оригинала 4 июня 2011 года . Проверено 20 октября 2013 г.
- Дэви, Хамфри (1813 г.). «Некоторые эксперименты и наблюдения над веществами, образующимися в различных химических процессах на плавиковом шпате» . Философские труды Королевского общества . 103 : 263–279. doi : 10.1098/rstl.1813.0034 .
- Дин, Джон А. (1999). Справочник Ланге по химии (15-е изд.). Нью-Йорк: Макгроу-Хилл. ISBN 0-07-016190-9.
- ДеБергалис, Майкл (2004). «Фторполимерные пленки в фотоэлектрической промышленности». Журнал химии фтора . 125 (8): 1255–1257. doi : 10.1016/j.jfluchem.2004.05.013 .
- Главное управление по окружающей среде (Европейская комиссия) (2007 г.). Трифлуралин (PDF) (Отчет). Европейская комиссия . Проверено 14 октября 2013 г.
- Дрюс, Т .; Супел, Дж.; Хагенбах, А .; Сеппельт, К. (2006). «Твердотельные молекулярные структуры гексафторидов переходных металлов». Неорганическая химия . 45 (9): 3782–3788. doi : 10.1021/ic052029f . PMID 16634614 .
- Дюпон (2013а). «Фреон» . Проверено 17 октября 2013 г.
- Дюпон (2013b). «Понимание номенклатуры хладагентов «R»» . Проверено 17 октября 2013 г.
- Итон, Чарльз (1997). "Рисунок hfl" . E-Hand.com: Электронный учебник хирургии кисти . Центр рук (бывшая практика доктора Итона) . Проверено 28 сентября 2013 г.
- Эдвардс, Филип Нил (1994). «Использование фтора в химиотерапии». В банках, RE; Смарт, БЫТЬ; Татлоу, Дж. К. (ред.). Фторорганическая химия: принципы и коммерческое применение . Нью-Йорк: Пленум Пресс. стр. 501–542. ISBN 978-0-306-44610-8.
- Эйнштейн, FWB; Рао, PR; Троттер, Дж.; Бартлетт, Н. (1967). «Кристаллическая структура трифторида золота». Журнал Химического общества A: неорганический, физический, теоретический . 4 : 478–482. doi : 10.1039/J19670000478 .
- Эйслер, Рональд (1995). Монофторацетат натрия (1080) Опасность для рыб, диких животных и беспозвоночных: сводный обзор (PDF) (отчет). Патаксентский экологический научный центр (Национальная биологическая служба США) . Проверено 5 июня 2011 г.
- Эллис, Брайан (2001). Научный эссенциализм . Кембридж: Издательство Кембриджского университета. ISBN 978-0-521-80094-5.
- Эль-Карех, Бади (1994). Основы технологии обработки полупроводников . Норвелл и Дордрехт: Kluwer Academic Publishers. ISBN 978-0-7923-9534-8.
- Эль Саади, MS; Холл, А.Х.; Холл, ПК; Риггс, бакалавр наук; Аугенштейн, WL; Румак, Б.Х. (1989). «Воздействие фтористоводородной кислоты на кожу». Ветеринарная и человеческая токсикология . 31 (3): 243–247. PMID 2741315 .
- Эмелеус, HJ; Шарп, А. Г. (1974). Успехи неорганической химии и радиохимии . Том. 16. Нью-Йорк: Академик Пресс. ISBN 978-0-08-057865-1.
- Эмелеус, HJ; Шарп, А. Г. (1983). Успехи неорганической химии и радиохимии . Том. 27. Академическая пресса. ISBN 0-12-023627-3.
- Эмсли, Джон (1981). «Скрытая сила водорода» . Новый ученый . 91 (1264): 291–292.
- Эмсли, Джон (2011). Строительные блоки природы: Путеводитель по элементам от А до Я (2-е изд.). Оксфорд: Издательство Оксфордского университета. ISBN 978-0-19-960563-7.
- Энергетика, Инк. (1997). Энергетический и экологический профиль алюминиевой промышленности США (PDF) (отчет) . Проверено 15 октября 2013 г.
- Филлер, Р.; Саха, Р. (2009). «Фтор в медицинской химии: век прогресса и 60-летняя ретроспектива избранных моментов» (PDF) . Медицинская химия будущего . 1 (5): 777–791. doi : 10.4155/fmc.09.65 . PMID 21426080 . Архивировано из оригинала (PDF) 22 октября 2013 г.
- Фишман, Майкл Л. (2001). «Опасности производства полупроводников». В Салливане, Джон Б.; Кригер, Гэри Р. (ред.). Клиническая гигиена окружающей среды и токсическое воздействие (2-е изд.). Филадельфия: Липпинкотт Уильямс и Уилкинс. стр. 431–465. ISBN 978-0-683-08027-8.
- Совет по продовольствию и питанию. «Справочные нормы потребления пищи (DRI): рекомендуемые пищевые нормы и адекватные нормы потребления, элементы» (PDF) . Институт медицины, Национальная академия. Архивировано из оригинала (PDF) 13 ноября 2018 года . Проверено 2 января 2019 г. .
- Форстер, П.; Рамасвами, В.; Артаксо, П.; Бернтсен, Т .; Беттс, Р.; Фэйи, Д. У.; Хейвуд, Дж.; Лин, Дж.; Лоу, округ Колумбия; Мире, Г.; Нганга, Дж.; Принн, Р.; Рага, Г.; Шульц, М.; Ван Дорланд, Р. (2007). «Изменения в составе атмосферы и в радиационном воздействии». В Соломоне, С.; Мэннинг, М.; Чен, З .; Маркиз, М .; Аверит, КБ; Тигнор, М .; Миллер, HL (ред.). Изменение климата 2007: Физическая научная основа. Вклад Рабочей группы I в Четвертый оценочный отчет Межправительственной группы экспертов по изменению климата . Кембридж: Кембриджский университет. стр. 129–234. ISBN 978-0-521-70596-7.
- Фултон, Роберт Б.; Миллер, М. Майкл (2006). «Плавиковый шпат». В Когеле Джессика Эльзеа; Триведи, Нихил С .; Баркер, Джеймс М .; Круковски, Стэнли Т. (ред.). Промышленные минералы и горные породы: товары, рынки и использование . Литтлтон: Общество горнодобывающей промышленности, металлургии и разведки (США). стр. 461–473. ISBN 978-0-87335-233-8.
- Габриэль, JL; Миллер-младший, TF; Вольфсон, М.Р.; Шаффер, TH (1996). «Количественные отношения структура-активность перфторированных гетероуглеводородов как потенциальных респираторных сред». Журнал АСАИО . 42 (6): 968–973. doi : 10.1097/00002480-199642060-00009 . PMID 8959271 . S2CID 31161098 .
- Гейнс, Пол (18 октября 1998 г.). «Новая угроза допинга крови» . Нью-Йорк Таймс . Проверено 18 октября 2013 г.
- Гесснер, Б.Д.; Беллер, М.; Миддо, JP; Уитфорд, GM (1994). «Острое отравление фтором из системы общественного водоснабжения». Медицинский журнал Новой Англии . 330 (2): 95–99. doi : 10.1056/NEJM199401133300203 . PMID 8259189 .
- Гизи, JP; Каннан, К. (2002). «Перфторхимические поверхностно-активные вещества в окружающей среде» . Экологические науки и технологии . 36 (7): 146А–152А. Бибкод : 2002EnST...36..146G . doi : 10.1021/es022253t . PMID 11999053 .
- Годфри, С.М.; Маколифф, Калифорния; Маки, АГ; Причард, Р.Г. (1998). «Неорганические производные элементов». В Нормане, Николас К. (ред.). Химия мышьяка, сурьмы и висмута . Лондон: Blackie Academic & Professional. стр. 67–158. ISBN 978-0-7514-0389-3.
- Зеленый, ЮЗ; Слинн, DSL; Симпсон, РНФ; Войтек, А. Дж. (1994). «Перфторуглеродные жидкости». В банках, RE; Смарт, БЫТЬ; Татлоу, Дж. К. (ред.). Фторорганическая химия: принципы и приложения . Нью-Йорк: Пленум Пресс. стр. 89–119. ISBN 978-0-306-44610-8.
- Гринвуд, Северная Каролина; Эрншоу, А. (1998). Химия элементов (2-е изд.). Оксфорд: Баттерворт Хайнеманн. ISBN 0-7506-3365-4.
- Гриббл, ГВ (2002). «Природные фторорганические соединения». В Neison, AH (ред.). Фторорганические соединения . Справочник по химии окружающей среды. Том. 3н. Берлин: Спрингер. стр. 121–136. дои : 10.1007/10721878_5 . ISBN 3-540-42064-9.
- Грот, Уолтер (2011). Фторированные иономеры (2-е изд.). Оксфорд и Уолтем: Эльзевир. ISBN 978-1-4377-4457-6.
- Хагманн, ВК (2008). «Многие роли фтора в медицинской химии». Журнал медицинской химии . 51 (15): 4359–4369. дои : 10.1021/jm800219f . PMID 18570365 .
- Харбисон, Г.С. (2002). «Электрическая дипольная полярность наземных и низколежащих метастабильных возбужденных состояний НФ». Журнал Американского химического общества . 124 (3): 366–367. дои : 10.1021/ja0159261 . PMID 11792193 .
- Хасэгава, Ю.; Отани, Р.; Йонезава, С .; Такашима, М. (2007). «Реакция между углекислым газом и элементарным фтором». Журнал химии фтора . 128 (1): 17–28. doi : 10.1016/j.jfluchem.2006.09.002 . hdl : 10098/1665 . S2CID 95754841 .
- Хаксель, Великобритания; Хедрик, Дж. Б.; Оррис, Г.Дж. (2005). Штауффер, PH; Хендли II, JW (ред.). Редкоземельные элементы — критически важные ресурсы для высоких технологий, информационный бюллетень 087-02 (отчет). Геологическая служба США . Проверено 31 января 2014 г.
- Хейнс, Уильям М., изд. (2011). Справочник по химии и физике (92-е изд.). Бока-Ратон: CRC Press. ISBN 978-1-4398-5511-9.
- Хоффман, Роберт; Нельсон, Льюис; Хауленд, Мэри; Левин, Нил; Фломенбаум, Нил; Голдфранк, Льюис (2007). Руководство Голдфранка по неотложной токсикологической помощи . Нью-Йорк: McGraw-Hill Professional. ISBN 978-0-07-144310-4.
- Ханивелл (2006). Рекомендуемое лечение при воздействии плавиковой кислоты (PDF) . Морристаун: Honeywell International. Архивировано из оригинала (PDF) 8 октября 2013 г .. Проверено 9 января 2014 г.
- Хугерс, Г. (2002). «Компоненты топливных элементов и их влияние на производительность». В Hoogers, G. (ред.). Справочник по технологии топливных элементов . Бока-Ратон: CRC Press. стр. 4-1–4-27. ISBN 0-8493-0877-1.
- Хауншелл, Дэвид А .; Смит, Джон Келли (1988). Наука и корпоративная стратегия: исследования и разработки DuPont, 1902–1980 гг . Кембридж: Издательство Кембриджского университета. ISBN 0-521-32767-9.
- Хультен, П.; Хёйер, Дж.; Людвигс, У .; Янсон, А. (2004). «Гексафторин по сравнению со стандартным обеззараживанием для снижения системной токсичности после воздействия на кожу плавиковой кислоты». Клиническая токсикология . 42 (4): 355–361. doi : 10.1081/CLT-120039541 . PMID 15461243 . S2CID 27090208 .
- ICIS (2 октября 2006 г.). «Сокровищница фтора» . Рид Деловая информация . Проверено 24 октября 2013 г.
- Жакко, М.; Фарон, Р.; Девилье, Д.; Романо, Р. (2000). "Фтор". Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. стр. 381–395. дои : 10.1002/14356007.a11_293 .
- Джонсон, Линда А. (28 декабря 2011 г.). «Несмотря ни на что, Lipitor стал мировым лидером продаж» . Бостонский глобус . Проверено 24 октября 2013 г.
- Качмарек, Роберт М .; Видеманн, Герберт П .; Лавин, Филип Т .; Ведель, Марк К.; Тютюнджю, Ахмет С.; Слуцкий, Артур С. (2006). «Частичная жидкостная вентиляция у взрослых пациентов с острым респираторным дистресс-синдромом». Американский журнал респираторной и интенсивной терапии . 173 (8): 882–89. doi : 10.1164/rccm.200508-1196OC . PMID 16254269 .
- Катакусе, Ицуо; Ичихара, Тошио; Ито, Хироюки; Сакурай, Тору; Мацуо, Такекиё (1999). «Эксперимент SIMS». Ин Араи, Т .; Михама, К.; Ямамото, К.; Сугано, С. (ред.). Мезоскопические материалы и кластеры: их физические и химические свойства . Токио: Коданша. стр. 259–273. ISBN 4-06-208635-2.
- Келли, ТД; Миллер, М.М. (2005). «Историческая статистика плавикового шпата» . Геологическая служба США . Проверено 10 февраля 2014 г.
- Кеплингер, М.Л.; Суисса, LW (1968). «Токсичность кратковременного вдыхания фтора». Журнал Американской ассоциации промышленной гигиены . 29 (1): 10–18. дои : 10.1080/00028896809342975 . PMID 5667185 .
- Керн, С .; Хейворд, Дж.; Робертс, С.; Ричардсон, Дж. В.; Ротелла, Ф.Дж.; Содерхольм, Л.; Корт, Б.; Тинкл, М .; Уэст, М.; Хойзингтон, Д.; Ландер, Джорджия (1994). «Температурное изменение структурных параметров актинидных тетрафторидов» . Журнал химической физики . 101 (11): 9333–9337. Бибкод : 1994JChPh.101.9333K . дои : 10.1063/1.467963 .<
- Хрящев, Л.; Петтерссон, М .; Рунеберг, Н.; Лунделл, Дж.; Расанен, М. (2000). «Стабильное соединение аргона» . Природа . 406 (6798): 874–876. Бибкод : 2000Natur.406..874K . дои : 10.1038/35022551 . PMID 10972285 . S2CID 4382128 .
- Кинг, Делавэр; Мэлоун, Р .; Лилли, С.Х. (2000). «Новая классификация и обновление хинолоновых антибиотиков» . Американский семейный врач . 61 (9): 2741–2748. PMID 10821154 . Проверено 8 октября 2013 г.
- Кирш, Пер (2004). Современная фторорганическая химия: синтез, реакционная способность, приложения . Вайнхайм: Wiley-VCH. ISBN 978-3-527-30691-6.
- Кисса, Эрик (2001). Фторированные поверхностно-активные вещества и репелленты (2-е изд.). Нью-Йорк: Марсель Деккер. ISBN 978-0-8247-0472-8.
- Куриакосе, А.К.; Маргрейв, Дж. Л. (1965). «Кинетика реакций элементарного фтора. IV. Фторирование графита». Журнал физической химии . 69 (8): 2772–2775. дои : 10.1021/j100892a049 .
- Лагов, Р. Дж. (1970). Реакции элементарного фтора; Новый подход к химии фтора (PDF) (доктор философии, Университет Райса, Техас). Анн-Арбор: UMI.
- Лау, К.; Анитол, К.; Ходс, К.; Проложенный.; Пфалес-Хатченс, А.; Сид, Дж. (2007). «Перфторалкильные кислоты: обзор мониторинга и токсикологических данных» . Токсикологические науки . 99 (2): 366–394. doi : 10.1093/toxsci/kfm128 . PMID 17519394 .
- Ли, Стивен; и другие. (2014). «Монофторацетатсодержащие растения, потенциально токсичные для домашнего скота». Журнал сельскохозяйственной и пищевой химии . Публикации АСС. 62 (30): 7345–7354. дои : 10.1021/jf500563h . PMID 24724702 .
- Леварс, Эррол Г. (2008). Моделирование чудес: вычислительное предсказание новых молекул . Дордрехт: Спрингер. ISBN 978-1-4020-6972-7.
- Лиде, Дэвид Р. (2004). Справочник по химии и физике (84-е изд.). Бока-Ратон: CRC Press. ISBN 0-8493-0566-7.
- Лидин Р.; Молочко, В.А.; Андреева Л.Л. (2000). Химические свойства неорганических веществ [ Химические свойства неорганических веществ ] (на русском языке). Москва: Химия. ISBN 5-7245-1163-0.
- Литепло, Р .; Гомес, Р.; Хоу, П.; Малкольм, Х. (2002). Критерии гигиены окружающей среды 227 (фторид) . Женева: Программа Организации Объединенных Наций по окружающей среде; Международная организация труда; Всемирная организация здравоохранения. ISBN 92-4-157227-2. Проверено 14 октября 2013 г.
- Ласти, PAJ; Браун, Т.Дж.; Уорд, Дж.; Блумфилд, С. (2008). «Необходимость местного производства плавикового шпата в Англии» . Британская геологическая служба . Проверено 13 октября 2013 г.
- Маккей, Кеннет Малкольм; Маккей, Розмари Энн; Хендерсон, В. (2002). Введение в современную неорганическую химию (6-е изд.). Челтнем: Нельсон Торнс. ISBN 0-7487-6420-8.
- Макомбер, Роджер (1996). Органическая химия . Том. 1. Саусалито: Университетские научные книги. ISBN 978-0-935702-90-3.
- Маргграф, Андреас Сигизмун (1770 г.). «Наблюдение, касающееся испаряемости, замечательной в отношении одной из сторон espece de pierre, à laquelle on donne les noms de flosse, flüsse, flus-spaht, et aussi celui d’hesperos; laquelle volatilisation a été effectuée au moyen des acides» [ Наблюдение замечательного улетучивания части камня, которому дали название flosse, flüsse, flus-spaht, а также hesperos; улетучивание которых осуществлялось с помощью кислот]. Mémoires de l'Académie royale des Sciences et belles-lettres (на французском языке). XXIV : 3–11.
- Мартин, Джон В., изд. (2007). Краткая энциклопедия строения материалов . Оксфорд и Амстердам: Эльзевир. ISBN 978-0-08-045127-5.
- Мария, см (2011). Учебник стоматологии общественного здравоохранения . Нью-Дели: Медицинское издательство Jaypee Brothers. ISBN 978-93-5025-216-1.
- Мацуи, М. (2006). «Фторсодержащие красители». Ин Ким, Сон-Хун (ред.). Функциональные красители . Орландо: Академическая пресса. стр. 257–266. ISBN 978-0-12-412490-5.
- Мейзингер, Рейнхард; Чиппендейл, А. Маргарет; Фэрхерст, Ширли А. (2012). «Ядерный магнитный резонанс и спектроскопия электронного спинового резонанса». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. стр. 609–660. дои : 10.1002/14356007.b05_471 .
- Мейер, Юджин (1977). Химия опасных материалов . Энглвудские скалы: Прентис-холл. ISBN 978-0-13-129239-0.
- Миллер, М. Майкл (2003a). «Плавиковый шпат» (PDF) . Ежегодник полезных ископаемых Геологической службы США . Геологическая служба США. С. 27.1–27.12.
- Миллер, М. Майкл (2003b). «Минеральные ресурсы месяца, плавиковый шпат» (PDF) . Геологическая служба США . Проверено 24 октября 2013 г.
- Митчелл, Э. Шивон (2004). Антидепрессанты . Нью-Йорк: Издательство Chelsea House. ISBN 978-1-4381-0192-7.
- Меллер, Т .; Байлар, Дж. К.; Клейнберг (1980). Химия с неорганическим качественным анализом (3-е изд.). Нью-Йорк: Академическая пресса. ISBN 0-12-503350-8.
- Муассан, Анри (1886 г.). "Action d'un courant électrique sur l'acide fluorhydrique anhydre" . Comptes rendus hebdomadaires des séances de l'Académie des Sciences (на французском языке). 102 : 1543–1544 . Проверено 9 октября 2013 г.
- Маккой, М. (2007). «ПРОБЛЕМЫ РЫНКА ОПРОСА ПОДрывают доверие руководителей мировых химических компаний». Новости химии и техники . 85 (23): 11. doi : 10.1021/cen-v085n023.p011a .
- Мур, Джон В.; Станицкий, Конрад Л.; Юрс, Питер С. (2010). Принципы химии: молекулярная наука . Бельмонт: Брукс/Коул. ISBN 978-0-495-39079-4.
- Морроу, SI; Перри, Д. Д.; Коэн, MS (1959). «Образование тетрафторида диазота в реакции фтора и аммиака». Журнал Американского химического общества . 81 (23): 6338–6339. дои : 10.1021/ja01532a066 .
- Мюллер, Питер (2009). «5.067 Уточнение кристаллической структуры» (PDF) . Кембридж: MIT OpenCourseWare . Проверено 13 октября 2013 г.
- Мерфи, компакт-диск; Шаффрат, К.; О'Хаган, Д. (2003). «Фторированные натуральные продукты: биосинтез фторацетата и 4-фтортреонина в Streptomyces Cattleya ». Хемосфера . 52 (2): 455–461. Бибкод : 2003Чмсп..52..455М . doi : 10.1016/S0045-6535(03)00191-7 . PMID 12738270 .
- Мурти, К. Парамешвара; Мехди Али, Сан-Франциско; Ашок, Д. (1995). Университетская химия . Том. I. Нью-Дели: New Age International. ISBN 978-81-224-0742-6.
- Национальный совет по здравоохранению и медицинским исследованиям (2007 г.). Систематический обзор эффективности и безопасности фторирования, часть A: обзор методологии и результатов (PDF) . Канберра: правительство Австралии. ISBN 978-1-86496-421-9. Архивировано из оригинала (PDF) 13 января 2012 года . Проверено 8 октября 2013 г.
- Национальный институт охраны труда и здоровья (1994 г.). «Фтор» . Документация по концентрациям, непосредственно опасным для жизни или здоровья (IDLH) . Проверено 15 января 2014 г.
- Национальный институт охраны труда и здоровья (1994 г.). «Хлор» . Документация по концентрациям, непосредственно опасным для жизни или здоровья (IDLH) . Проверено 13 июля 2014 г.
- Национальный центр ядерных данных . «База данных NuDat 2.1» . Брукхейвенская национальная лаборатория . Проверено 25 октября 2013 г.
- Национальное управление океанических и атмосферных исследований. «UN / NA 1045 (Информационный бюллетень Организации Объединенных Наций / Северной Америки по фтору)» . Проверено 15 октября 2013 г.
- Наваррини, Вальтер; Вентурини, Франческо; Тортелли, Вито; Басак, Субир; Пимпаркар, Кетан П.; Адамо, Андреа; Дженсен, Клавс Ф. (2012). «Прямое фторирование монооксида углерода в микрореакторах». Журнал химии фтора . 142 : 19–23. doi : 10.1016/j.jfluchem.2012.06.006 .
- Нельсон, Юджин В. (1947). "«Плохой человек» из «Элементов» . Популярная механика . 88 (2): 106–108, 260.
- Нельсон, Дж. М.; Чиллер, ТМ; Пауэрс, Дж. Х.; Ангуло, Ф.Дж. (2007). «Безопасность пищевых продуктов: виды Campylobacter, устойчивые к фторхинолонам, и изъятие фторхинолонов из использования в птицеводстве: история успеха общественного здравоохранения» (PDF) . Клинические инфекционные заболевания . 44 (7): 977–980. дои : 10.1086/512369 . PMID 17342653 .
- Нильсен, Форрест Х. (2009). «Микроэлементы в парентеральном питании: бор, кремний и фтор» . Гастроэнтерология . 137 (5): С55–60. doi : 10.1053/j.gastro.2009.07.072 . PMID 19874950 . Проверено 29 апреля 2018 г.
- Норвуд, Чарльз Дж.; Фос, Ф. Юлиус (1907). Геологическая служба Кентукки, Бюллетень № 9: Месторождения плавикового шпата в Кентукки . Геологическая служба Кентукки.
- Нури, С.; Сильви, Б.; Гиллеспи, Р. Дж. (2002). «Химическая связь в гипервалентных молекулах: актуально ли правило октета?» (PDF) . Неорганическая химия . 41 (8): 2164–2172. дои : 10.1021/ic011003v . PMID 11952370 . Проверено 23 мая 2012 г.
- О'Хаган, Д. (2008). «Понимание химии фторорганических соединений. Введение в связь C – F». Обзоры химического общества . 37 (2): 308–319. дои : 10.1039/b711844a . PMID 18197347 .
- О'Хаган, Д.; Шаффрат, К.; Кобб, С.Л.; Гамильтон, JTG; Мерфи, компакт-диск (2002). «Биохимия: биосинтез фторорганической молекулы» . Природа . 416 (6878): 279. Бибкод : 2002Natur.416..279O . дои : 10.1038/416279a . PMID 11907567 . S2CID 4415511 .
- Окада, Т .; Се, Г.; Горсет, О .; Кьелструп, С .; Накамура, Н .; Аримура, Т. (1998). «Характеристики переноса ионов и воды нафионовых мембран как электролитов». Электрохимика Акта . 43 (24): 3741–3747. doi : 10.1016/S0013-4686(98)00132-7 .
- Оказое, Т. (2009). «Обзор истории фторорганической химии с точки зрения материальной промышленности» . Труды Японской академии, серия B. 85 (8): 276–289. Бибкод : 2009PJAB...85..276O . doi : 10.2183/pjab.85.276 . ПВК 3621566 . PMID 19838009 .
- Оливарес, М.; Уауи, Р. (2004). Основные питательные вещества в питьевой воде (черновик) (PDF) (отчет). Всемирная организация здравоохранения (ВОЗ). Архивировано из оригинала (PDF) 19 октября 2012 года . Проверено 14 октября 2013 г.
- Паренте, Лука (2001). «Разработка синтетических глюкокортикоидов». В Гулдинге, Николас Дж .; Цветок, Род Дж. (ред.). Глюкокортикоиды . Базель: Биркхойзер. стр. 35–53. ISBN 978-3-7643-6059-7.
- Партингтон, младший (1923). «Ранняя история плавиковой кислоты». Воспоминания и труды Манчестерского литературно-философского общества . 67 (6): 73–87.
- Патнаик, Прадьот (2007). Всеобъемлющее руководство по опасным свойствам химических веществ (3-е изд.). Хобокен: Джон Уайли и сыновья. ISBN 978-0-471-71458-3.
- Полинг, Линус (1960). Природа химической связи (3-е изд.). Итака: Издательство Корнельского университета. ISBN 978-0-8014-0333-0.
- Полинг, Л.; Кивени, И.; Робинсон, А.Б. (1970). «Кристаллическая структура α-фтора». Журнал химии твердого тела . 2 (2): 225–227. Бибкод : 1970JSSCh...2..225P . doi : 10.1016/0022-4596(70)90074-5 .
- Перри, Дейл Л. (2011). Справочник по неорганическим соединениям (2-е изд.). Бока-Ратон: CRC Press. ISBN 978-1-4398-1461-1.
- Питцер, Канзас (1975). «Фториды радона и элемента 118» . Журнал химического общества, Chemical Communications (18): 760b–761. дои : 10.1039/C3975000760B .
- Питцер, Кеннет С. , изд. (1993). Молекулярная структура и статистическая термодинамика: избранные статьи Кеннета С. Питцера . Сингапур: World Scientific Publishing. ISBN 978-981-02-1439-5.
- Пиццо, Г.; Пископо, штат Массачусетс; Пиццо, И.; Джулиана, Г. (2007). «Общественное фторирование воды и профилактика кариеса: критический обзор» (PDF) . Клинические исследования полости рта . 11 (3): 189–193. doi : 10.1007/s00784-007-0111-6 . PMID 17333303 . S2CID 13189520 .
- Познер, Стефан (2011). «Перфторированные соединения: присутствие и использование в продуктах». В Неппер, Томас П .; Большой, Фрэнк Т. (ред.). Полифторированные химикаты и продукты переработки . Гейдельберг: Springer Science + Business Media. стр. 25–40. ISBN 978-3-642-21871-2.
- Познер, Стефан; и другие. (2013). Пер- и полифторированные вещества в странах Северной Европы: использование и токсикология (PDF) . Копенгаген: Совет министров Северных стран. DOI : 10.6027 /TN2013-542 . ISBN 978-92-893-2562-2.
- Прескорн, Шелдон Х. (1996). Клиническая фармакология селективных ингибиторов обратного захвата серотонина . Каддо: Профессиональные коммуникации. ISBN 978-1-884735-08-0.
- Принцип, Лоуренс М. (2012). Тайны Алхимии . Чикаго: Издательство Чикагского университета. ISBN 978-0-226-68295-2.
- Праудфут, А.Т.; Брэдберри, С.М.; Вейл, Дж. А. (2006). «Отравление фторацетатом натрия». Токсикологические обзоры . 25 (4): 213–219. doi : 10.2165/00139709-200625040-00002 . PMID 17288493 . S2CID 29189551 .
- PRWeb (28 октября 2010 г.). «Глобальный рынок фторохимикатов превысит 2,6 млн тонн к 2015 году, согласно новому отчету Global Industry Analysts, Inc» . prweb.com . Проверено 24 октября 2013 г.
- PRWeb (23 февраля 2012 г.). «Глобальный рынок плавикового шпата достигнет 5,94 млн метрических тонн к 2017 году, согласно новому отчету Global Industry Analysts, Inc» . prweb.com . Проверено 24 октября 2013 г.
- PRWeb (7 апреля 2013 г.). «Рынок фторполимеров готов расти со среднегодовым темпом роста 6,5% и достичь 9 446,0 млн долларов к 2016 году — новый отчет MarketsandMarkets» . prweb.com . Проверено 24 октября 2013 г.
- Пюикко, Пекка; Ацуми, Митико (2009). «Ковалентные радиусы молекулярных двойных связей для элементов Li – E112». Химия: Европейский журнал . 15 (46): 12770–9. doi : 10.1002/chem.200901472 . PMID 19856342 .
- Рагхаван, PS (1998). Понятия и проблемы неорганической химии . Дели: Издательство Discovery. ISBN 978-81-7141-418-5.
- Радж, П. Притви; Эрдине, Сердар (2012). Обезболивающие процедуры: иллюстрированное руководство . Чичестер: Джон Вили и сыновья. ISBN 978-0-470-67038-5.
- Рамкумар, Джейшри (2012). «Перфторсульфонатная мембрана Nafion: уникальные свойства и различные применения». В Банерджи, С.; Тяги, А.К. (ред.). Функциональные материалы: подготовка, обработка и применение . Лондон и Уолтем: Эльзевир. стр. 549–578. ISBN 978-0-12-385142-0.
- Редди, Д. (2009). «Неврология эндемического флюороза скелета» . Неврология Индия . 57 (1): 7–12. doi : 10.4103/0028-3886.48793 . PMID 19305069 .
- Ренда, Агостино; Феннер, Еше; Гибсон, Брэд К.; Каракас, Аманда И.; Латтанцио, Джон К.; Кэмпбелл, Саймон; Чиффи, Алессандро; Кунья, Катя; Смит, Верн В. (2004). «О происхождении фтора в Млечном Пути». Ежемесячные уведомления Королевского астрономического общества . 354 (2): 575–580. arXiv : astro-ph/0410580 . Бибкод : 2004MNRAS.354..575R . doi : 10.1111/j.1365-2966.2004.08215.x . S2CID 12330666 .
- Реннер, Р. (2006). «Длинные и короткие перфторированные заменители» . Экологические науки и технологии . 40 (1): 12–13. Бибкод : 2006EnST...40...12R . дои : 10.1021/es062612a . PMID 16433328 .
- Роудс, Дэвид Уолтер (2008). Широкополосные исследования диэлектрической спектроскопии нафиона (докторская диссертация, Университет Южного Миссисипи, MS). Энн Арбор. ISBN 978-0-549-78540-8.
- Рихтер, М.; Хан, О .; Фукс, Р. (2001). «Пурпурный флюорит: пигмент малоизвестных художников и его использование в живописи поздней готики и раннего Возрождения в Северной Европе». Исследования в области сохранения . 46 (1): 1–13. doi : 10.1179/sic.2001.46.1.1 . JSTOR 1506878 . S2CID 191611885 .
- Ридель, Себастьян; Каупп, Мартин (2009). «Наивысшие степени окисления элементов переходных металлов». Обзоры координационной химии . 253 (5–6): 606–624. doi : 10.1016/j.ccr.2008.07.014 .
- Рипа, Л.В. (1993). «Полвека общественного фторирования воды в Соединенных Штатах: обзор и комментарии» (PDF) . Журнал стоматологии общественного здравоохранения . 53 (1): 17–44. doi : 10.1111/j.1752-7325.1993.tb02666.x . PMID 8474047 . Архивировано из оригинала (PDF) 4 марта 2009 г.
- Роблин, И.; Урбан, М .; Фликото, Д.; Мартин, К.; Прадо, Д. (2006). «Местное лечение экспериментальных ожогов кожи плавиковой кислотой 2,5% глюконатом кальция». Журнал лечения ожогов и исследований . 27 (6): 889–894. doi : 10.1097/01.BCR.0000245767.54278.09 . PMID 17091088 . S2CID 3691306 .
- Салагер, Жан-Луи (2002). Поверхностно-активные вещества: типы и использование (PDF) . Буклет FIRP № 300-A. Лаборатория составов, интерфейсов, реологии и процессов Университета Лос-Андес . Проверено 13 октября 2013 г.
- Сэндфорд, Грэм (2000). «Фторорганическая химия». Философские труды . 358 (1766): 455–471. Бибкод : 2000RSPTA.358..455S . doi : 10.1098/rsta.2000.0541 . S2CID 202574641 .
- Саркар, С. (2008). «Искусственная кровь» . Индийский журнал медицины критических состояний . 12 (3): 140–144. DOI : 10.4103 /0972-5229.43685 . ПВК 2738310 . PMID 19742251 .
- Шееле, Карл Вильгельм (1771). «Undersŏkning om fluss-spat och dess syra» [Исследование флюорита и его кислоты]. Kungliga Svenska Vetenskapsademiens Handlingar [Труды Шведской королевской академии наук] (на шведском языке). 32 : 129–138.
- Шиммейер, С. (2002). «В поисках заменителя крови» . Иллюмин . Колумбия: Университет Южной Каролины. 15 (1). Архивировано из оригинала 2 октября 2011 года . Проверено 15 октября 2013 г.
- Шледер, Т .; Ридель, С. (2012). «Исследование гетеродимерных и гомодимерных катион-радикалов ряда: [F 2 O 2 ] + , [F 2 Cl 2 ] + , [Cl 2 O 2 ] + , [F 4 ] + и [Cl 4 ] + ». РСК Прогресс . Королевское химическое общество . 2 (3): 876–881. Бибкод : 2012RSCAd...2..876S . DOI : 10.1039/ C1RA00804H .
- Шмедт Ауф Дер Гюнне, Йорн; Мангстл, Мартин; Краус, Флориан (2012). «Присутствие дифторина F2 в природе на месте, доказательство и количественная оценка с помощью ЯМР-спектроскопии». Международное издание Angewandte Chemie . 51 (31): 7847–7849. doi : 10.1002/anie.201203515 . ISSN 1521-3773 . PMID 22763992 .
- Шмитц, А .; Келике, Т .; Уиллкомм, П.; Грюнвальд, Ф.; Кандыба, Дж.; Шмитт, О. (2000). «Использование фтор-18-фтор-2-дезокси-D-глюкозы позитронно-эмиссионной томографии в оценке процесса туберкулезного спондилита» (PDF) . Журнал заболеваний позвоночника . 13 (6): 541–544. doi : 10.1097/00002517-200012000-00016 . PMID 11132989 . Проверено 8 октября 2013 г.
- Шульце-Макух, Д.; Ирвин, Л. Н. (2008). Жизнь во Вселенной: ожидания и ограничения (2-е изд.). Берлин: Springer-Verlag. ISBN 978-3-540-76816-6.
- Шварц, Джозеф А. (2004). Муха в бочке меда: 70 увлекательных комментариев о науке о повседневной жизни . Торонто: ECW Press. ISBN 1-55022-621-5.
- Сеннинг, А. (2007). Словарь хемоэтимологии Эльзевира: причины и происхождение химической номенклатуры и терминологии . Амстердам и Оксфорд: Elsevier. ISBN 978-0-444-52239-9.
- Шаффер, ТХ; Вольфсон, М.Р.; Кларк-младший, LC (1992). «Жидкостная вентиляция». Детская пульмонология . 14 (2): 102–109. doi : 10.1002/ppul.1950140208 . PMID 1437347 . S2CID 222167378 .
- Шин, Ричард Д.; Сильверберг, Марк А. (2013). «Фторидная токсичность» . Медскейп . Проверено 15 октября 2013 г.
- Шрайвер, Дювард; Аткинс, Питер (2010). Руководство по решениям для неорганической химии . Нью-Йорк: WH Freeman. ISBN 978-1-4292-5255-3.
- Шульман, JD; Уэллс, Л.М. (1997). «Острая токсичность фтора при приеме внутрь стоматологических изделий для домашнего использования у детей от рождения до 6 лет». Журнал стоматологии общественного здравоохранения . 57 (3): 150–158. doi : 10.1111/j.1752-7325.1997.tb02966.x . PMID 9383753 .
- Зигемунд, Г.Н.; Швертфегер, В.; Фейринг, А .; Смарт, Б.; Бер, Ф.; Фогель, Х .; МакКьюсик, Б. (2000). «Соединения фтора, органические». Энциклопедия промышленной химии Ульмана . Том. 15. Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a11_349 .
- Слай, Орвилл М. (2012). «Средства пожаротушения». В Ульманн, Франц (ред.). Энциклопедия промышленной химии Ульмана . Том. 15. Вайнхайм: Wiley-VCH. стр. 1–11. doi : 10.1002/14356007.a11_113.pub2 . ISBN 978-3527306732.
- Стинланд, К.; Флетчер, Т .; Савиц, Д.А. (2010). «Эпидемиологические данные о влиянии перфтороктановой кислоты (ПФОК) на здоровье» . Перспективы гигиены окружающей среды . 118 (8): 1100–1108. doi : 10.1289/ehp.0901827 . ПМК 2920088 . PMID 20423814 .
- Стиллман, Джон Мэксон (декабрь 1912 г.). «Бэзил Валентайн, розыгрыш семнадцатого века» . Ежемесячный научно-популярный журнал . 81 . Проверено 14 октября 2013 г.
- Сторер, Фрэнк Х. (1864). Первые наброски словаря растворимости химических веществ . Кембридж: Север и Фрэнсис.
- Суинсон, Джоэл (июнь 2005 г.). «Фтор - жизненно важный элемент в аптечке» (PDF) . ФармаХим . Фармацевтическая химия: 26–27. Архивировано из оригинала (PDF) 8 февраля 2012 г .. Проверено 9 октября 2013 г.
- Табер, Эндрю (22 апреля 1999 г.). «Умереть, чтобы ездить» . салон . Проверено 18 октября 2013 г.
- Таннер Индастриз (январь 2011 г.). «Безводный аммиак: (MSDS) Паспорт безопасности материала» . tannerind.com . Проверено 24 октября 2013 г.
- Теодоридис, Джордж (2006). «Фторсодержащие агрохимикаты: обзор последних разработок». В Трессо, Ален (ред.). Фтор и окружающая среда: агрохимикаты, археология, зеленая химия и вода . Амстердам и Оксфорд: Elsevier. стр. 121–176. ISBN 978-0-444-52672-4.
- Мульт, Ричард (1 сентября 2011 г.). «Открытие фтора» . Образование в области химии . Том. 48, нет. 5. Королевское химическое общество . стр. 148–151. ISSN 0013-1350 .
- Transparency Market Research (17 мая 2013 г.). «Ожидается, что к 2018 году мировой рынок фторохимикатов достигнет 21,5 миллиарда долларов США: исследование рынка Transparency» . Блог исследования рынка прозрачности. Архивировано из оригинала 22 февраля 2014 года . Проверено 15 октября 2013 г.
- Ульманн, Фриц (2008). Волокна Ульмана (2 тома). Вайнхайм: Wiley-VCH. ISBN 978-3-527-31772-1.
- Агентство по охране окружающей среды США (1996 г.). «КРАСНЫЕ факты: трифлуралин» (PDF) . Архивировано из оригинала (PDF) 18 октября 2013 года . Проверено 17 октября 2013 г.
- Агентство по охране окружающей среды США (2012 г.). «Новые загрязнители - перфтороктановый сульфонат (ПФОС) и перфтороктановая кислота (ПФОК)» (PDF) . Архивировано из оригинала (PDF) 29 октября 2013 года . Проверено 4 ноября 2013 г.
- Агентство по охране окружающей среды США (2013a). «Озоноразрушающие вещества I класса» . Архивировано из оригинала 10 декабря 2010 года . Проверено 15 октября 2013 г.
- Агентство по охране окружающей среды США (2013b). «Поэтапный отказ от ГХФУ (вещества, разрушающие озоновый слой II класса)» . Проверено 15 октября 2013 г.
- Виль, Клод; Голдуайт, Гарольд (1993). «Нобелевский лауреат 1906 года: Анри Муассан, 1852–1907». В Лейлин, К. Джеймс (ред.). Нобелевские лауреаты по химии, 1901–1992 гг . Вашингтон: Американское химическое общество; Фонд химического наследия. стр. 35–41 . ISBN 978-0-8412-2690-6.
- Вигуре, П. (1961). «Гиромагнитное отношение протона». Современная физика . 2 (5): 360–366. Бибкод : 1961ConPh...2..360V . дои : 10.1080/00107516108205282 .
- Вильяльба, Гара; Эйрес, Роберт У .; Шредер, Ганс (2008). «Учет фтора: производство, использование и потери». Журнал промышленной экологии . 11 : 85–101. doi : 10.1162/jiec.2007.1075 . S2CID 153740615 .
- Уолш, Кеннет А. (2009). Химия и обработка бериллия . Парк материалов: ASM International. ISBN 978-0-87170-721-5.
- Уолтер, П. (2013). «Honeywell инвестирует 300 миллионов долларов в экологически чистый хладагент» . Химический мир .
- Уикс, Мэн (1932). «Открытие элементов. XVII. Семейство галогенов». Журнал химического образования . 9 (11): 1915–1939. Бибкод : 1932JChEd...9.1915W . DOI : 10.1021/ ed009p1915 .
- Вернер, Нидерланды; Хекер, Монтана; Сетхи, Аляска; Донски, CJ (2011). «Ненужное использование фторхинолоновых антибиотиков у госпитализированных пациентов» . Инфекционные заболевания ВМС . 11 : 187–193. дои : 10.1186/1471-2334-11-187 . ПМС 3145580 . PMID 21729289 .
- Виберг, Эгон; Виберг, Нильс; Холлеман, Арнольд Фредерик (2001). Неорганическая химия . Сан-Диего: Академическая пресса. ISBN 978-0-12-352651-9.
- Уилли, Рональд Р. (2007). Практическое оборудование, материалы и процессы для оптических тонких пленок . Шарлевуа: Уилли Оптикал. ISBN 978-0-615-14397-2.
- Йос, Карл Л.; Брейкер, Уильям (2001). "Фтор". Книга данных Matheson Gas Data Book (7-е изд.). Парсиппани: Matheson Tri-Gas. ISBN 978-0-07-135854-5.
- Юнг, Калифорния (2008). «Систематический обзор эффективности и безопасности фторирования» . Доказательная стоматология . 9 (2): 39–43. doi : 10.1038/sj.ebd.6400578 . PMID 18584000 .
- Янг, Дэвид А. (1975). Фазовые диаграммы элементов (отчет). Ливерморская лаборатория Лоуренса . Проверено 10 июня 2011 г.
- Зарейталабад, П.; Сименс, Дж.; Хамер, М .; Амелунг, В. (2013). «Перфтороктановая кислота (ПФОК) и перфтороктансульфокислота (ПФОС) в поверхностных водах, отложениях, почвах и сточных водах - обзор концентраций и коэффициентов распределения». Хемосфера . 91 (6): 725–32. Бибкод : 2013Chmsp..91..725Z . doi : 10.1016/j.chemosphere.2013.02.024 . PMID 23498059 .
- Зорич, Роберт (1991). Справочник по качественному производству интегральных схем . Сан-Диего: Академическая пресса. ISBN 978-0-323-14055-3.
внешние ссылки
-
 СМИ, связанные с фтором , на Викискладе?
СМИ, связанные с фтором , на Викискладе?