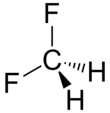
Дифторметан - Difluoromethane
|
|
|||
| Имена | |||
|---|---|---|---|
|
Предпочтительное название IUPAC
Дифторметан |
|||
| Другие имена
Гидрид фтористого углерода
Метилендифторид |
|||
| Идентификаторы | |||
|
3D модель ( JSmol )
|
|||
| Сокращения | ГФУ-32 Р-32 |
||
| 1730795 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard |
100.000.764 |
||
| Номер ЕС | |||
| 259463 | |||
| MeSH | Дифторметан | ||
|
PubChem CID
|
|||
| Номер RTECS | |||
| UNII | |||
| Номер ООН | 3252 | ||
|
Панель управления CompTox ( EPA )
|
|||
|
|||
|
|||
| Характеристики | |||
| C H 2 F 2 | |||
| Молярная масса | 52,024 г · моль -1 | ||
| Появление | Бесцветный газ | ||
| Плотность | 1,1 г см -3 (в жидкой форме) | ||
| Температура плавления | -136 ° С (-213 ° F, 137 К) | ||
| Точка кипения | -52 ° С (-62 ° F, 221 К) | ||
| журнал P | -0,611 | ||
| Давление газа | 1518,92 кПа (при 21,1 ° C) | ||
| Опасности | |||
| Паспорт безопасности |
См .: страницу данных MSDS в Оксфордском университете. |
||
| R-фразы (устаревшие) | R11 | ||
| S-фразы (устаревшие) | S9 , S16 , S33 | ||
| NFPA 704 (огненный алмаз) | |||
| 648 ° С (1198 ° F, 921 К) | |||
| Страница дополнительных данных | |||
|
Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. |
|||
|
Термодинамические
данные |
Фазовое поведение твердое тело – жидкость – газ |
||
| УФ , ИК , ЯМР , МС | |||
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|||
|
|
|||
| Ссылки на инфобоксы | |||
Дифторметана , называемые также дифторметильна, ГФ-32 Метиленовый Фтор или R-32 , представляет собой органическое соединение , из dihalogenoalkane сорта. Он имеет формулу CH 2 F 2 . В окружающей атмосфере это бесцветный газ, который слабо растворяется в воде и обладает высокой термической стабильностью. Из-за низкой температуры плавления и кипения (-136,0 ° C и -51,6 ° C соответственно) контакт с этим составом может привести к обморожению. В Соединенных Штатах в разделе 111 Закона о чистом воздухе о летучих органических соединениях (ЛОС) дифторметан перечислен в качестве исключения (с 1997 года) из определения ЛОС из-за низкого образования тропосферного озона. Дифторметан обычно используется в эндотермических процессах, таких как охлаждение или кондиционирование воздуха.
Синтез
Дифторметан в основном синтезируется с помощью периодических процессов, путем реакции дихлорметана и фтороводорода (HF) в жидкой фазе с использованием SbCl 5 в качестве катализатора. Из-за опасных свойств фтороводорода был разработан новый синтез. Новый синтез обеспечивает постоянный поток производимого дифторметана через изолированную камеру.
Приложения
Дифторметан часто используется в качестве огнетушащего вещества из-за его способности подвергаться эндотермическим процессам. Слева показаны атмосферные концентрации дифторметана на разных широтах с 2009 года.
Дифторметан - это молекула, используемая в качестве хладагента, которая обладает отличными характеристиками теплопередачи и перепада давления как при конденсации, так и при испарении. Его 100-летний потенциал глобального потепления (ПГП) в 675 раз больше, чем у углекислого газа, и время жизни в атмосфере почти 5 лет. Он классифицируется как A2L - легковоспламеняющийся по ASHRAE и имеет нулевой озоноразрушающий потенциал (ODP). Таким образом, дифторметан является выбором с относительно низким уровнем риска среди хладагентов на основе ГФУ , большинство из которых имеют более высокий ПГП и более длительную стойкость при утечках.
Обычный хладагент R-410A представляет собой зеотропную смесь 50/50 массовых процентов дифторметана и пентафторэтана ( R-125 ). Пентафторэтан - обычная замена различных хлорфторуглеродов (например, фреона ) в новых системах хладагента , особенно в системах кондиционирования воздуха. Зеотропная смесь дифторметана с пентафторэтаном ( R-125 ) и тетрафторэтаном ( R-134a ) известна как R-407a через R-407F в зависимости от состава. Аналогичным образом, R-504 представляет собой азеотропную (48,2 / 51,8 мас.%) Смесь дифторметана и хлортрифторметана (R13). В 2011 году только в США в атмосферу было выброшено 17 949 893 метрических тонны дифторметана.
Дифторметан в настоящее время используется сам по себе в бытовых и коммерческих кондиционерах в Японии, Китае и Индии в качестве замены R-410A . Чтобы снизить остаточный риск, связанный с его легкой воспламеняемостью, эту молекулу следует применять в теплообменном оборудовании с низкой заправкой хладагента, таком как паяные пластинчатые теплообменники (ППТО) или кожухотрубные теплообменники, а также трубчатые и пластинчатые теплообменники с трубкой. небольшого диаметра. Многие приложения подтвердили, что дифторметан демонстрирует более высокие коэффициенты теплопередачи, чем у R-410A при тех же рабочих условиях, но также более высокие потери давления на трение.
Другие применения дифторметана включают его использование в качестве пропеллентов для аэрозолей, вспенивающих агентов и растворителей.
Экологическая судьба
Ежегодно производится около 15 килотонн дифторметана. В газовой форме соединение будет разлагаться в атмосфере в результате реакции с гидроксильными радикалами, полученными фотохимическим путем. В результате этого процесса образуется карбонилдифторид . Полураспада этого процесса оценивается в 4 года. Дифторметан имеет тенденцию попадать в окружающую среду через газовую фазу и накапливается там чаще, чем в почве или отложениях. Период полураспада этого соединения составляет около 45 минут для рек и 69 часов для озер, что еще раз доказывает, что дифторметан плохо накапливается в водных организмах.
HFC-32, попавший в окружающую среду, распадается на CF в качестве промежуточного продукта. При этом в результате гидролиза в атмосферной воде образуются HF и CO 2 .
Дифторметан исключен из списка ЛОС, поставляемых в соответствии с Законом США о чистом воздухе, поскольку ОРС равен нулю. Следовательно, тропосферный озон вряд ли будет производиться из этой молекулы. Тропосферный озон может привести к неблагоприятным последствиям для здоровья, таким как респираторные, сердечные или неврологические нарушения. Кроме того, озон может влиять на растения и растительность, вызывая бронзовый оттенок листьев.
Токсичность
Дифторметан проявляет небольшую токсичность для матери и развития при концентрациях примерно 50 000 ppm для крыс, но не для кроликов. Ограничения воздействия, установленные для дифторметана для использования человеком, составляют 1000 ppm, что делает воздействие на опасные уровни маловероятным.