COPII - COPII
| Sec23 гомолог A | |||||||
|---|---|---|---|---|---|---|---|
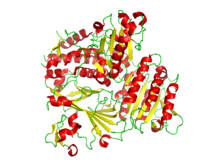 Ленточная диаграмма кристаллографической структуры гетеродимера COPII Sec23 и Sec24. Альфа-спирали - красным, а бета-листы - желтым.
| |||||||
| Идентификаторы | |||||||
| Символ | SEC23A | ||||||
| Ген NCBI | 856311 | ||||||
| HGNC | 10701 | ||||||
| OMIM | 610511 | ||||||
| PDB | 1М2В | ||||||
| RefSeq | NM_006364 | ||||||
| UniProt | Q15436 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 14 q21.1 | ||||||
| |||||||
| Семья SEC24, член A | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | SEC24A | ||||||
| Ген NCBI | 10802 | ||||||
| HGNC | 10703 | ||||||
| OMIM | 607183 | ||||||
| PDB | 1М2В | ||||||
| RefSeq | XM_001132082 | ||||||
| UniProt | O95486 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 5 q31.1 | ||||||
| |||||||
COPII представляет собой коатомер , тип белка оболочки везикул, который транспортирует белки из грубого эндоплазматического ретикулума в аппарат Гольджи . Этот процесс называется антероградным транспортом , в отличие от ретроградного транспорта, связанного с белком COPI . Название «COPII» относится к конкретному со в р rotein комплекс , который инициирует процесс многообещающий. Оболочка состоит из крупных белковых субкомплексов, состоящих из четырех различных белковых субъединиц.
Белки оболочки
Оболочка COPII состоит из пяти белков: Sar1 , Sec23 , Sec24 , Sec13 и Sec31 . Эти белки димеризуются с образованием более крупных белковых комплексов:
Важно отметить, что существует пять различных типов белков, которые составляют оболочку COPII, но несколько белков одного и того же разнообразия составляют белковые комплексы, важные для формирования оболочки COPII.
Эти белки оболочки необходимы, но недостаточны для направления или стыковки везикулы с правильной мембраной-мишенью. Для этих процессов также необходимы SNARE , груз и другие белки.
Процесс бутонизации
Сборку везикул COPII можно резюмировать как:
- Sar1-GDP взаимодействует с трансмембранным белком ER Sec12.
- Sar1-GTP рекрутирует белок оболочки Sec23 / Sec24, чтобы сформировать предварительно почкующийся комплекс.
- Предварительно отпочкованный комплекс (состоящий из Sar1-GTP, связанного с Sec23 / 24) рекрутирует Sec13 / Sec31, который формирует второй слой оболочки.
- Комплекс Sec13 / Sec31 образует подобную клетке внешнюю оболочку (подобную образованию пузырьков клатрина ).
Sar1p - это GTPase, которая действует как «переключатель», который переключает между активированной мембраной, встроенной в GTP-связанную форму, и неактивной растворимой GDP-связанной формой. Неактивный GDP-связанный Sar1p привлекается к цитозольной стороне эндоплазматического ретикулума.
Sec12, трансмембранный белок, обнаруженный в ER, действует как фактор обмена гуаниновых нуклеотидов , стимулируя высвобождение GDP, что позволяет связывать GTP в Sar1.
Связанный с GTP Sar1p претерпевает конформационное изменение, которое открывает N-концевую амфипатическую a-спираль (другие источники говорят, что гидрофобный хвост), которая вставляется в мембрану ER. Связанный с мембраной Sar1p рекрутирует комплекс Sec23p / 24p, чтобы сформировать то, что в совокупности известно как pre-budding комплекс. Sec23 / Sec24 специфически связывается со специфическими сигналами сортировки в цитозольных доменах мембранных грузовых белков, эти сигналы сортировки не разделяют простой сигнальный мотив, такой как KDEL или KKXX . Недавние исследования показывают, что несколько сигналов экспорта ER взаимодействуют для разделения и исключения несобранного груза.
Предварительно отпочкованный комплекс (состоящий из Sar1-GTP и Sec23 / 24) рекрутирует гибкий комплекс Sec13p / 31p, характеризующийся полимеризацией комплекса Sec13 / 31 с другими комплексами Sec13 / 31 с образованием кубооктаэдра с более широкой решеткой, чем его клатриновый пузырь. аналог. Образование кубооктаэдра деформирует мембрану ER и отделяет везикулу COPII (наряду с белками груза и v-SNAREs), завершая процесс отпочкования везикул COPII.
Обнаружено, что некоторые белки ответственны за избирательную упаковку грузов в везикулы COPII. Более поздние исследования показывают, что комплекс Sec23 / Sec24-Sar1 участвует в выборе груза. Например, обнаружено, что Erv29p в Saccharomyces cerevisiae необходим для упаковки гликозилированного про-α-фактора.
После образования везикул COPII белки оболочки COPII остаются собранными, чтобы позволить комплексу Sec23 / Sec24 взаимодействовать с фактором привязки на мембране Cis-Golgi. Когда везикула COPII находится в непосредственной близости от мембраны цис-Гольджи, она сбрасывает свою оболочку, и компоненты рециркулируются, чтобы функционировать для другой везикулы.
Конформационные изменения
CopII имеет три специфических сайта связывания, каждый из которых может быть комплексным. На соседнем изображении (Sed5) для связывания используется комплекс Sec22 t-SNARE. Этот сайт более сильно привязан и поэтому пользуется большим спросом. (Эмбо)
Смотрите также
- Везикулы COPI
- Клатриновые везикулы


