Аламетицин - Alamethicin

|
|
| Имена | |
|---|---|
|
Название ИЮПАК
N - ацетил-2-methylalanyl- L пролил-2-methylalanyl- л аланил-2-methylalanyl- L -аланил- L -glutaminyl-2-methylalanyl- л -valyl-2-methylalanylglycyl- л -leucyl-2- methylalanyl- L -prolyl- L -valyl-2-methylalanyl-2-methylalanyl- L -α-глутамил N 1 - [(1 S ) -1-бензил-2-гидроксиэтил] - L -glutamamide
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard |
100.121.626 |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| С 92 H 150 N 22 O 25 | |
| Молярная масса | 1964,31 г / моль |
| Появление | Не совсем белое твердое вещество |
| Температура плавления | От 255 до 270 ° C (от 491 до 518 ° F; от 528 до 543 K) |
| Нерастворимый | |
| Растворимость в ДМСО , метаноле , этаноле | Растворимый |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Аламетицин - каналообразующий пептидный антибиотик , продуцируемый грибом Trichoderma viride . Он относится к пептидам пептаибола, которые содержат непротеиногенный аминокислотный остаток Aib ( 2-аминоизомасляная кислота ). Этот остаток сильно индуцирует образование альфа-спиральной структуры. Пептидная последовательность:
Ac-Aib-Pro-Aib-Ala-Aib-Ala-Gln-Aib-Val-Aib-Gly-Leu-Aib-Pro-Val-Aib-Aib-Glu-Gln-Phl
(Ac = ацетил, Phl = фенилаланинол , Aib = 2-аминоизомасляная кислота )
В клеточных мембранах он образует потенциал- зависимые ионные каналы путем агрегации от четырех до шести молекул .
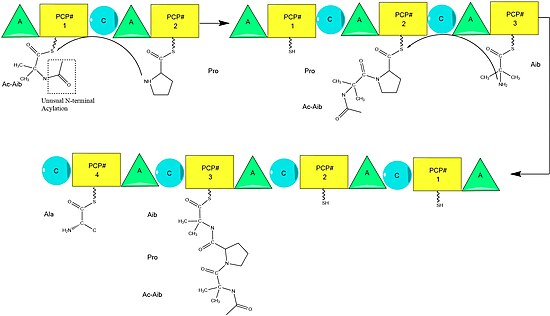
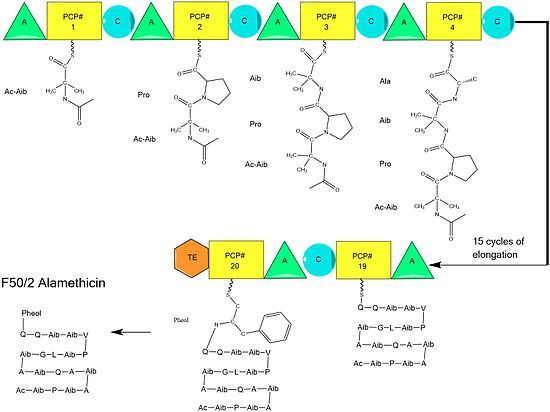
Биосинтез
Предполагается, что биосинтез аламетицина катализируется аламетицин-синтазой, нерибосомальной пептид- синтазой (NRPS), впервые выделенной в 1975 году. Хотя существует несколько принятых последовательностей пептида аламетицина, данные свидетельствуют о том, что все они следуют общему механизму NRPS с небольшими вариациями в избранных аминокислотах. . Начиная с ацилирования N-конца первой аминоизобутириновой кислоты на ферменте ALM-синтазы ацетил-КоА , за этим следует последовательная конденсация аминокислот каждой модульной единицей синтетазы. Аминокислоты первоначально adenylated с помощью « аденилирования » (А) областей прежде , чем быть прикреплено с помощью тиоэфирных св зи с белком Ацила Carrier -подобного белка - носителя пептидил. Растущая цепь присоединяется к несущему аминокислоту PCP доменом «конденсации» (C), за которым следует еще один цикл тех же реакций в следующем модуле.
Сборка завершается добавлением фенилаланинола, необычного похожего на аминокислоту субстрата. После добавления фенилаланинола завершенная пептидная цепь расщепляется тиоэстеразным доменом, разрывая тиоэфирную связь и оставляя спирт.
использованная литература
дальнейшее чтение
- Джонс, Л. Р.; Мэддок, ЮАР; Беш, HR-младший (1980). «Демаскирующий эффект аламетицина на (Na +, K +) - АТФазу, аденилатциклазу, связанную с бета-адренергическим рецептором, и активность цАМФ-зависимых протеинкиназ в сердечных сарколеммальных везикулах» . J. Biol. Chem . 255 (20): 9971–9980. DOI : 10.1016 / S0021-9258 (18) 43488-6 . PMID 6253461 .
- Изучите структуры аламетицина в банке данных по белкам
-
Аламетицин в норине
- Из «Модель потенциалзависимого ионного канала, выведенная из кристаллической структуры аламетицина с разрешением 1,5 A». Fox Jr, RO; Ричардс, FM (1982). «Модель потенциалзависимого ионного канала, выведенная из кристаллической структуры аламетицина с разрешением 1,5 A». Природа . 300 (5890): 325–30. Bibcode : 1982Natur.300..325F . DOI : 10.1038 / 300325a0 . PMID 6292726 . S2CID 4278453 .
- Лейтгеб, Балаж; Секереш, Андраш; Манцингер, Ласло; Вагвёльдьи, Чаба; Kredics, Ласло (01.06.2007). «История аламетицина: обзор наиболее широко изученного пептаибола». Химия и биоразнообразие . 4 (6): 1027–1051. DOI : 10.1002 / cbdv.200790095 . ISSN 1612-1880 . PMID 17589875 . S2CID 40886688 .